
现有短周期元素构成的3种单质甲、乙、丙,它们在一定条件下能发生如下变化,部分产物已略去。
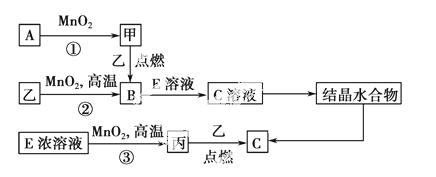
(1)若反应①可在常温下进行,则A的电子式为________。若反应①需在加热条件下进行,则反应①的化学方程式为____________________________。
(2)反应②的化学方程式为________,该反应是________(填“放热”或“吸热”)反应。
(3)从C溶液中得到C需经过两步操作:先从C溶液中得到晶体,再将得到的晶体转化为C。从C溶液中得到晶体的过程被称为________,将得到的晶体转化为C的实验条件是____________________________________。
(4)反应③中氧化剂与还原剂的物质的量之比为________。
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.pH=1的溶液中:Fe2+、NO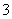 、SO
、SO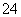 、Na+
、Na+
B.无色溶液中:K+、Fe3+、SO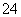 、SCN-
、SCN-
C.c (H+)/c (OH-) = 1012 的溶液中:NH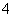 、Al3+、NO
、Al3+、NO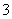 、Cl-
、Cl-
D.由水电离的c (H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO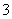
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学反应能量变化相关的叙述正确的是( )
A.放热反应的反应速率总是大于吸热反应的反应速率
B.已知一定条件下石墨转化为金刚石吸收热量,则石墨比金刚石稳定
C.对于吸热反应,生成物总能量一定低于反应物总能量
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组利用废铁屑制取FeCl3•6H2O晶体。主要操作流程如下:
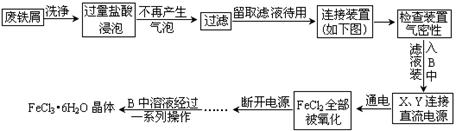
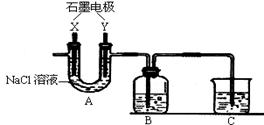
请回答下列问题:
(1)C烧杯中盛放的试剂是 。
(2)A中的X极应该连接电源的 极,A中发生反应的离子方程式为
。
(3)试剂瓶B中的溶液经过一系列操作得到FeCl3•6H2O晶体,这一系列操作由下列操作组成(操作不重复),则依次进行的操作为 (填字母序号)
A.加热浓缩 B.洗涤干燥 C.过滤 D.冷却结晶
(4)该装置有无缺陷,若有,请指出来 若无,本空可不答。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。
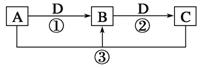
请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是__________;工业上制取A的离子方程式_________________________。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为____________________________________。
(3)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是________________________________________________________________。
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为_________________________________________________________。
某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因: _____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物被略去)
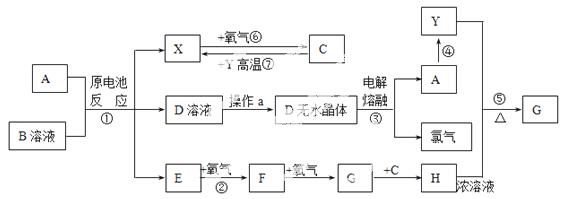
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为
____________________________________________________________________;
(2)从D溶液制备D的无水晶体的“操作a”为__________________________;
(3)E的电子式为_________________________________;
(4)反应⑤的化学方程式为_____________________________________________;
(5)原电池反应①中正极的电极反应式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A~M为中学化学的常见物质,它们之间的转化关系如图所示,部分生成物和反应条件省略。已知C、D是由元素X、Y、Z中的两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子 最外层电子数之和为10。D为无色气体且不能燃烧,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。请回答
最外层电子数之和为10。D为无色气体且不能燃烧,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。请回答 下列问题:
下列问题:
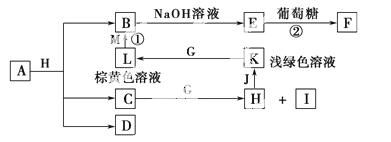
(1)写出A的化学式:____________。
(2)比较Y与Z的原子半径大小:________>________(填元素符号)。
(3)检验L溶液中金属阳离子的方法是________________________________________。
(4)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体。请写出该反应的化学 方程式:_______________________________________________________________________。
方程式:_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
A.X元素的氢化物的水溶液显碱性
B.Z元素的离子半径大于W元素的离子半径
C.Z元素的单质在一定条件下能与X元素的单质反应
D.Y元素最高价氧化物的晶体具有很高的熔点和沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.铝在空气中耐腐蚀,所以铝是不活泼金属
B.点燃的镁条插入盛有二氧化碳的集气瓶里,则迅速熄灭
C.铝在高温下能还原锰、铁、铬等金属的氧化物
D.因为镁和铝在空气中都能形成氧化膜,所以镁和铝都不溶于浓硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com