
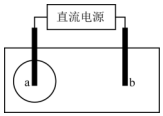
 用两根铅笔芯接触饱和氯化钠溶液浸湿的试纸两端,接通直流电源.很短时间内,a电极与试纸接触处便宜出现一蓝色圆.下列说法正确的是( )
用两根铅笔芯接触饱和氯化钠溶液浸湿的试纸两端,接通直流电源.很短时间内,a电极与试纸接触处便宜出现一蓝色圆.下列说法正确的是( )| A. | 该试纸可能是pH试纸,b电极为正极 | |
| B. | 该试纸可能是pH试纸,b电极处亦出现一蓝色圆 | |
| C. | 该试纸可能是淀粉碘化钾试纸,b电极附近溶液pH变小 | |
| D. | 该试纸可能是淀粉碘化钾试纸,b电极处发生还原反应 |
分析 接通直流电源,很短时间内,a电极与试纸接触处便宜出现一蓝色圆,若该试纸是pH试纸,说明a极为阴极产生了H2和OH-,电极方程式为2H2O-4e-═H2↑+2OH-,b为阳极,电极反应式为:2Cl--2e-═Cl2↑;若该试纸是淀粉碘化钾试纸,则说明a极为阳极先产生了Cl2,电极反应式为:2Cl--2e-═Cl2↑,氯气将碘离子氧化成碘单质,与淀粉出现一蓝色圆,b为阴极,电极方程式为2H2O-4e-═H2↑+2OH-,所以b极附近的pH增大,据此分析解答.
解答 解:A、该试纸可能是pH试纸,则说明a极为阴极产生了H2和OH-,电极方程式为2H2O-4e-═H2↑+2OH-,b为阳极,故A错误;
B、该试纸可能是pH试纸,则说明a极为阴极产生了H2和OH-,电极方程式为2H2O-4e-═H2↑+2OH-,b为阳极,电极反应式为:2Cl--2e-═Cl2↑,不会出现一蓝色圆,故B错误;
C、该试纸可能是淀粉碘化钾试纸,则说明a极为阳极先产生了Cl2,电极反应式为:2Cl--2e-═Cl2↑,氯气将碘离子氧化成碘单质,与淀粉出现一蓝色圆,b为阴极,电极方程式为2H2O-4e-═H2↑+2OH-,所以b极附近的pH增大,故C错误;
D、该试纸可能是淀粉碘化钾试纸,b为阴极,电极方程式为2H2O-4e-═H2↑+2OH-,发生还原反应,故D正确.
故选:D.
点评 该题以电解饱和食盐水为载体,重点考查学生对电解原理的熟悉了解程度.试题紧扣教材,趣味性强,有利于调动学生的学习兴趣和学习积极性,激发学生学习化学的求知欲,也有助于培养学生的逻辑思维能力和应试能力,提高学生的学习效率.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:选择题
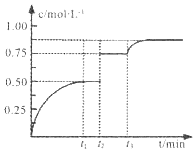 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )| A. | 反应方程式中的x=1 | |
| B. | t2时刻改变的条件是使用催化剂 | |
| C. | t3时刻改变的条件是移去少量物质C | |
| D. | t1~t3间该反应的平衡常数均为4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| C. | 氯水中放入有色布条,有色布条褪色,说明溶液中有Cl2存在 | |
| D. | 1.12LCl2含有1.7NA个质子(NA表示阿伏伽德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠跟水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向A12(SO4)3溶液中加入过量的氨水:A13++3NH3•H2O═A1(OH)3↓+3NH4+ | |
| C. | 向硫酸溶液中加入Ba(OH)2溶液:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| D. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F2、Cl2、Br2、I2和H2反应激烈程度递减 | |
| B. | HF、HCl、HBr、HI热稳定性减小 | |
| C. | F2、Cl2、Br2、I2的氧化性递增 | |
| D. | F-、Cl-、Br-、I-失电子能力递增 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{3}^{4}$He | B. | ${\;}_{2}^{3}$He | C. | ${\;}_{2}^{4}$He | D. | He${\;}_{3}^{3}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| 《本草经集注》记载“以火烧之,紫青烟起,云是真硝石(硝酸钾)也” | 碳酸氢钠药片 |  |  |
| 钾的焰色反应颜色为紫色 | 该药是抗酸药,服用时喝些醋能提高药效 | 看到有该标志的丢弃物,应远离并报警 | 该物品可做消毒剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
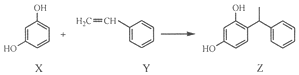
| A. | X和Z均能与FeCl3溶液反应显紫色 | |
| B. | X和Z均能与NaHCO3溶液反应放出CO2 | |
| C. | Y既能发生取代反应,也能发生加成反应 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com