
 ij����С������ͼװ�ý���ʵ�飬�Իش��������⣺
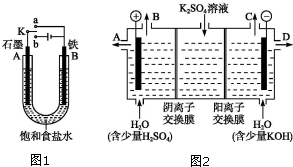
ij����С������ͼװ�ý���ʵ�飬�Իش��������⣺���� ��1����ʼʱ����K��a�����γ�ԭ��ط�Ӧ��B�缫��������ʧ���������������ӣ�����������Ӧ��A�缫ʯī��������Һ�������õ������������������ӣ�
��2����ʼʱ����K��b�����γɵ��أ����Դ����������A�缫Ϊ��������Һ��������ʧ�����������������Դ����������B�缫Ϊ���ص���������Һ�������ӵõ�������������������Ȼ�����Һ�����������ơ�������������
��3��A�����������������������ƶ���
B��A�缫Ϊ��������A�����ݳ���������������
C���ָ������ǰ����ʵ�Ũ�ȣ�����ʲô��ʲô����ԭ�������
D��B���ǵ��ص���������״���²���2.24L����Ϊ�������ʵ���Ϊ0.1mol�����ݵ缫��Ӧ���㣬��2H++2e-=H2���õ���Һ��ת��0.2mol����
��4���ٵ��ʱ����Һ�е����������ӵķŵ�����������������ӵķŵ�������������ʧ���ӷ���������Ӧ�������������ӵ��ƶ�����ͨ����ͬ����ʱ���������ӽ����ĸ����жϣ�
�ڵ���������������������������
�۵���������������ˮ������������ӷŵ磬ˮ�ĵ���ƽ���ܵ�Ӱ�죮
��� �⣺��1����ʼʱ����K��a�����γ�ԭ��ط�Ӧ��B�缫��������ʧ���������������ӣ��缫��ӦΪ��Fe-2e-=Fe2+���ʴ�Ϊ��Fe-2e-=Fe2+��
��2������K��b���ӣ�װ��Ϊ���أ���Ϊ������������ԭ��Ӧ�������ӵõ�����������������B�缫��ӦΪ2H++2e-=H2������ⱥ��ʳ��ˮ�����������ơ�����������������ܷ�Ӧ�����ӷ���ʽΪ2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2�����ʴ�Ϊ��2H++2e-=H2����2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
��3��A�����������������������ƶ���BΪ��������Һ��Na+��B���ƶ����ʢٴ���
B��A������������ʹʪ��KI������ֽ�������ʢ���ȷ��
C����Ӧһ��ʱ��������HCl���壬�ɻָ������ǰ����ʵ�Ũ�ȣ����Ǽ������ᣬ�ʢ۴���
D������״����B������2.24L������Ϊ�������ʵ���Ϊ0.1mol�����ݵ缫��Ӧ���㣬��2H++2e-=H2���õ���Һ��ת��0.2mol���ӣ��ʢ���ȷ��
�ʴ�Ϊ���ڢܣ�
��4���ٵ��ʱ��������ʧ���ӷ���������Ӧ����Һ�е����������ӵķŵ�����������������ӵķŵ���������������������������ʧ��������ˮ������4OH--4e-=2H2O+O2�����������������ӷŵ磬�������������������ƶ������������ӷŵ磬����������������ƶ�������ͨ����ͬ����ʱ��ͨ�������ӽ���Ĥ��������С��ͨ�������ӽ���Ĥ����������
�ʴ�Ϊ��4OH--4e-=2H2O+O2����С�ڣ�
�ڵ������������������������ɣ���������������Һ�ӳ���D�������ʴ�Ϊ��D��
�۵���������������ˮ������������ӷŵ磬2H++2e-=H2��������ˮ�ĵ���ƽ�������ƶ�����������������Ũ�ȴ��������ӣ���Һ��ʾ���ԣ��ʴ�Ϊ������������������ˮ������������ӷŵ磬2H++2e-=H2��������ˮ�ĵ���ƽ�������ƶ�����������������Ũ�ȴ��������ӣ���Һ��ʾ���ԣ�
���� ���⿼����ԭ��غ͵���ԭ�����ѶȲ���ע��ȼ��ԭ��ص缫��Ӧʽ����дʱ��Ҫ���ݵ������Һ�������ȷ�����ɵ����ӻ����ʣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 A��B��C����ѧ��ѧ�������������ʣ�����֮����ת����ϵ���£����ַ�Ӧ������������ȥ����A$\stackrel{O_{2}}{��}$B$\stackrel{O_{2}}{��}$C
A��B��C����ѧ��ѧ�������������ʣ�����֮����ת����ϵ���£����ַ�Ӧ������������ȥ����A$\stackrel{O_{2}}{��}$B$\stackrel{O_{2}}{��}$C�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K�Ĵ�С����ʼŨ���й� | B�� | �¶�Խ�ߣ�KֵԽ�� | ||
| C�� | KֵԽ��Ӧ������еij̶�Խ�� | D�� | KֵԽ��Ӧ������еij̶�ԽС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ�� | B�� | ���� | C�� | �մ� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
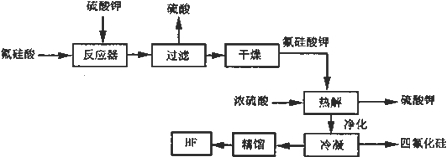
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ĵ缫��ӦʽΪAl-3e-��Al3+ | |
| B�� | �õ�ص��ܷ�ӦʽΪ2Li+FeS�TLi2S+Fe | |
| C�� | LiAl�ڵ������Ϊ�������ϣ��ò�����Li�Ļ��ϼ�Ϊ+1 | |
| D�� | ���ʱ�����������ĵ缫��ӦʽΪLi2S+Fe-2e-�T2Li++FeS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ϩ����� | ������� |
| ��CH3��2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
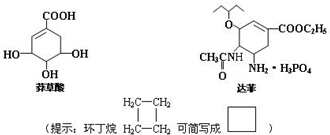
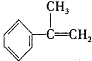 ��HBr��Ӧ����Ҫ����Ľṹ��ʽ
��HBr��Ӧ����Ҫ����Ľṹ��ʽ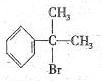 ��
��
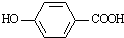 �����䷴Ӧ����Ϊ����ȥ��Ӧ��
�����䷴Ӧ����Ϊ����ȥ��Ӧ��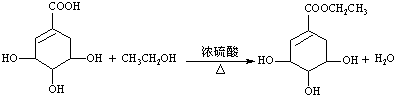 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com