
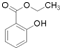
 )广泛用于黑醋栗酒、依兰、百合等的花香型的调和香料,还用作草莓等果香香精及化工行业.水杨酸乙酯为无色油状液体,呈淡的冬青油香气,沸点233℃,溶于乙醇、乙醚,微溶于水和甘油.利用水杨酸(沸点:211℃)、乙醇(沸点:78.4℃)和浓硫酸在硫酸铝存在下于100℃下酯化而成,反应方程式如下:
)广泛用于黑醋栗酒、依兰、百合等的花香型的调和香料,还用作草莓等果香香精及化工行业.水杨酸乙酯为无色油状液体,呈淡的冬青油香气,沸点233℃,溶于乙醇、乙醚,微溶于水和甘油.利用水杨酸(沸点:211℃)、乙醇(沸点:78.4℃)和浓硫酸在硫酸铝存在下于100℃下酯化而成,反应方程式如下: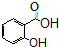 +C2H5OH?
+C2H5OH?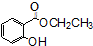 +H2O
+H2O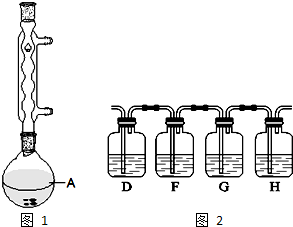
分析 (1)用水杨酸与乙醇制备水杨酸乙酯,加入过量乙醇可以提高水杨酸的转化率,反应后水杨酸乙酯与水杨酸、乙醇等混合在一起,但它们的沸点不同,据此判断获得水杨酸乙酯的实验方法;
(2)实验过程中观察到了溶液变黑,是因为浓硫酸的脱水性,使得有机物发生碳化,碳与浓硫酸在加热的条件下发生反应生成二氧化碳和二氧化硫,所以有刺激性气味的混合气体应为二氧化碳和二氧化硫的混合气体,为探究该混合气体的成分,根据题中装置图可知,应先用品红检验二氧化硫的存在,再用高锰酸钾除去二氧化硫,再用品红溶液检验二氧化硫是否除尽,再将气体通过澄清石灰水检验二氧化碳的存在,所以装置D中应为品红溶液,F中应为高锰酸钾溶液,G中为品红溶液,H中为澄清石灰水,据此答题;
(3)根据强碱弱酸盐溶液呈碱性,可判断NaH2PO4是一种弱酸的酸式盐.
解答 解:(1)用水杨酸与乙醇制备水杨酸乙酯,加入过量乙醇可以提高水杨酸的转化率,反应后水杨酸乙酯与水杨酸、乙醇等混合在一起,但它们的沸点不同,所以要获得水杨酸乙酯可以用蒸馏的方法,
故答案为:提高水杨酸的转化率;蒸馏;
(2)实验过程中观察到了溶液变黑,是因为浓硫酸的脱水性,使得有机物发生碳化,碳与浓硫酸在加热的条件下发生反应生成二氧化碳和二氧化硫,所以有刺激性气味的混合气体应为二氧化碳和二氧化硫的混合气体,为探究该混合气体的成分,根据题中装置图可知,应先用品红检验二氧化硫的存在,再用高锰酸钾除去二氧化硫,再用品红溶液检验二氧化硫是否除尽,再将气体通过澄清石灰水检验二氧化碳的存在,所以装置D中应为品红溶液,F中应为高锰酸钾溶液,G中为品红溶液,H中为澄清石灰水,
①根据上面的分析可知,装置D中的试剂是 品红溶液,
故答案为:品红溶液;
②根据上面的分析可知,装置F的作用是 除去二氧化硫,
故答案为:除去二氧化硫;
③在吸收用高锰酸钾溶液吸收二氧化硫时,可以根据高锰酸钾溶液的颜色的变化判断二氧化硫是否被完全吸收,若反应过程中高锰酸钾溶液颜色不褪去,则可以确定二氧化硫完全除去,所以能将实验装置G删除,产生有刺激性气味的混合气体的化学反应方程式为C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:能;如果高锰酸钾过量,而反应过程中颜色不褪去,则可以确定二氧化硫完全除去;C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(3)根据强碱弱酸盐溶液呈碱性,可判断NaH2PO4是一种弱酸的酸式盐,实验方法为将NaH2PO4配制成0.1mol/L的溶液,测量溶液的pH值,pH值大于1小于7,说明NaH2PO4是一种弱酸的酸式盐,
故答案为:将NaH2PO4配制成0.1mol/L的溶液,测量溶液的pH值,pH值大于1小于7,说明NaH2PO4是一种弱酸的酸式盐.
点评 本题考查有机物的合成实验、基本操作、实验条件的控制与分析评价等,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 将15.6 g Na2O2和5.4 g Al同时放入一定量的水中可以产生标况下气体6.72 L | |
| B. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该气体能使品红溶液褪色,则该溶液可能既含有SO32-又含有CO32- | |
| C. | 大多数碳的化合物都是共价化合物,其原因是碳元素有三种同位素 | |
| D. | 石油分馏可获得乙烯、丙烯和丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
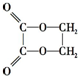 )时最合理的合成路线需经下列反应:
)时最合理的合成路线需经下列反应:| A. | ①②③⑤⑥ | B. | ⑤②①③⑥ | C. | ⑥③①②⑤ | D. | ①②⑤③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40K和40Ca 具有相同的中子数 | |
| B. | 40K+和40Ca2+ 具有相同的电子层结构 | |
| C. | 39K和40Ca互为同位素 | |
| D. | 40K的原子半径小于40Ca 的原子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| B. | C6H6十Br2$\stackrel{Fe}{→}$C6H5Br+HBr | |
| C. | CH2═CH2+Br2CH2Br-CH2Br | |
| D. | CH3COOH+CH3CH2OH$→_{加热}^{浓硫酸}$CH3COOCH2CH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙炔和苯 | B. | 甲烷和乙烷 | C. | 乙烯和丁炔 | D. | 苯和苯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2使品红溶液褪色 | |
| B. | 浓硫酸暴露在空气中会增重 | |
| C. | 常温下,可用铁、铝制容器来盛装浓硫酸或浓硝酸 | |
| D. | 氨气遇到氯化氢气体冒“白烟” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑦ | B. | ①④ | C. | ③④⑥ | D. | ①③⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com