
| A. | 加入少量W,逆反应速率增大 | |
| B. | 升高温度时,正反应速率增大,逆反应速率减小 | |
| C. | 压强不变,充入与反应体系不反应的N2,Z的物质的量减少 | |
| D. | 平衡后加入X,上述反应的△H增大 |
分析 A.固体量的增减不会影响反应速率;
B.升温,正逆反应速率都加快;
C.压强不变,充入与反应体系不反应的N2,反应容器体积增大,平衡逆向移动;
D.反应热△H与物质的化学计量数有关,与参加反应的某物质的物质的量无关.
解答 解:A.W在反应中是固体,固体量的增减不会引起化学反应速率的改变和化学平衡的移动,故A错误;
B.升温,正逆反应速率都加快,故B错误;
C.压强不变,充入与反应体系不反应的N2,反应容器体积增大,平衡逆向移动,则Z的物质的量减少,故C正确;
D.反应热△H与物质的化学计量数有关,物质的化学计量数不变,热化学方程式中反应热不变,与参加反应的物质的物质的量无关,故D错误;
故选C.
点评 本题考查化学反应平衡影响因素,为高频考点,侧重考查学生分析判断能力,明确恒温恒压、恒温恒容的区别是解本题关键,注意分析压强增大时是否导致参加反应的各物质浓度改变,如果发生改变的,则发生平衡移动,否则不发生平衡移动,为易错题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 玻璃仪器洗涤干净倒掉水后,水在仪器上应既不能成滴也不能成股流下 | |
| B. | 环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏大 | |
| C. | 将玻璃导管蘸水后,边旋转边向橡皮导管中插入使其连接起来 | |
| D. | 做银镜反应实验后的试管内壁附有银,可用稀硝酸清洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
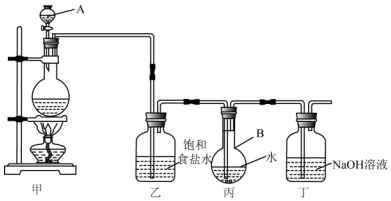
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
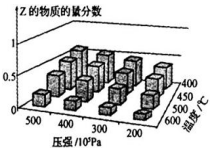 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是| A. | 在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平 衡时,Z的物质的量分数不变 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H>0,m+n>c | |
| D. | 温度不变,增大压强,平衡正向移动,达新平衡时,A的浓度比原平衡减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上用电解法冶炼钠、镁、铝等活泼金属 | |
| B. | 粗铜精炼时,与电源负极相连的是纯铜,该电极反应式为Cu2++2e-=Cu | |
| C. | 由C(s,石墨)=C(s,金刚石)△H=+1.9kJ/mol可知,金刚石比石墨稳定 | |
| D. | 反应SO2(g)+2H2S(g)=3S (s)+2H2O(l)在常温下能自发进行,则该反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2s后物质A的转化率为70% | |
| B. | 当各物质浓度满足c(A)=2c(B)=c(C)时,该反应达到了平衡状态 | |
| C. | 达到平衡状态时,增加A物质的量,A和B转化率都提高 | |
| D. | 达到平衡状态时,升高温度,则该化学平衡向左移动,同时化学平衡常数K减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
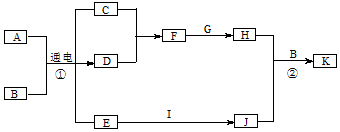
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com