
对于4℃时,水中溶解了22.4L HCl气体(标准状况下测得)后形成的溶液200mL,下列说法中正确的是
A.该溶液物质的量浓度为10mol/L
B.所用水的体积为177.6L
C.根据题干数据,该溶液物质的量浓度无法求得
D.该溶液中溶质的质量分数因溶液的密度未知而无法求得
科目:高中化学 来源:2016届浙江省高三上学期10月阶段测化学试卷(解析版) 题型:选择题
进行下列实验,由实验现象得出的结论错误的是
选项 | 操作及现象 | 溶液可能是 |
A | 通入CO2,溶液变浑浊。再升高至70℃,溶液变澄清。 | C6H5ONa溶液 |
B | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。 | Na2SiO3溶液 |
C | 通入CO2,溶液变浑浊。再加入品红溶液,红色褪去。 | Ca(ClO)2溶液 |
D | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊。 | Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷(解析版) 题型:选择题
在相同温度相同体积的甲、乙两容器中发生反应2SO2(g)+O2(g) 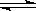 2SO3 (g),甲容器中充入1molSO2和1molO2,乙容器充入2molSO2和2molO2。下列叙述错误的是
2SO3 (g),甲容器中充入1molSO2和1molO2,乙容器充入2molSO2和2molO2。下列叙述错误的是
A.化学反应速率:乙>甲 B.平衡后O2的浓度:乙>甲
C.平衡后SO2的转化率:乙>甲 D.平衡后混合气体的密度:乙>2甲
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:选择题
将4molA和2molB在2L密闭容器中混合发生反应,2A(g)+B(g) 2C(g);ΔH<0,4秒后反应达到平衡状态,此时得C的浓度为0.6mol/L,下列说法正确的是
2C(g);ΔH<0,4秒后反应达到平衡状态,此时得C的浓度为0.6mol/L,下列说法正确的是
A.当A、B、C物质的量浓度化为2︰1︰2时,反应即达到平衡状态
B.4S内用物质B表示的反应速率为0.075mol/(L·S)
C.达平衡后通入一定量的氦气,A的转化率降低
D.达平衡后升高温度,C的浓度将增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上期中测试化学试卷(解析版) 题型:选择题
下列电离方程正确的是
A.NaHCO3=Na++H++CO32- B.Ba(OH)2=Ba2++OH-
C.Al2(SO4)3=2Al3++3SO42- D.H2SO4=H2++SO42-
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(每空1分,共11分)从下列各组反应对比,判断那种微粒的氧化性最强。
(1)铁钉浸入硫酸铜溶液中后,表面会附有红色物质,铜丝浸入硝酸银溶液后,表面会附有银白色物质。则铜、铁、银中,_____ ___原子的还原性最强;Cu2+、Ag+、Fe2+中, 离子的氧化性最强。
(2)在氯气中Fe锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液FeCl2。则氯气分子、氢离子、氯离子中, 具有氧化性, 氧化性最强。请书写出以上各反应的化学方程式________ 、 。
(3)已知在ⅣA族元素中,Pb2+和Sn4+的化合物较为稳定。
①据此可判断PbO2具有较强的________性,SnCl2具有较强的 性;写出PbO2溶于盐酸的离子方程式__________;写出SnCl2和FeCl3溶液混合的离子方程式__________ ;
②PbO2、Fe3+、Cl2、Sn4+氧化性由强到弱的顺序是__________ 。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰市宁城县高三上学期第一次统考化学试卷(解析版) 题型:选择题
已知硫酸亚铁溶液中加入过氧化钠时发生反应:
4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+则下列说法正确的是
A.该反应中还原剂为Fe2+,O2、Fe(OH)3均为氧化产物
B.充分反应后可以看到白色沉淀和气体生成
C.标准状况下,每生成22.4 L O2,则有4 mol Na2O2被还原
D.若有4 mol Na2O2参加反应,则反应中共转移6NA个电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版) 题型:选择题
某溶液中可能含有的阴离子有SO42-、CO32-、Cl-等.为了检验其中是否含有Cl-,需要下列化学试剂为
①HCl②HNO3③H2SO4④AgNO3⑤Ba(NO3)2⑥CaCl2
A.②④ B. ②④⑥ C. ①④⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省三门峡市高二上学期期中测试化学试卷(解析版) 题型:选择题
pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是
A.反应开始时的速率:甲>乙
B.反应结束时,pH值:甲=乙
C.反应开始时,酸的物质的量浓度:甲=乙
D.反应所需时间:甲>乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com