
【题目】把下列溶液加水稀释,溶液中每种离子的浓度都不会增加的是( )
A.CH3COOH溶液
B.NaCl溶液
C.NaOH溶液
D.FeCl3溶液
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】锌是一种重要的金属,锌及其化合物有着广泛的应用.
(1)指出锌在周期表中的位置:第周期第族,属于区.
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式;葡萄糖分子[CH2OHCHOH(CHOH)3CHO]中碳原子杂化方式有 .
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+ . 配位体NH3分子中心原子的 杂化方式是 , 属于(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在图中用箭头表示出[Zn(NH3)4]2+中Zn2+与N之间的化学键 . 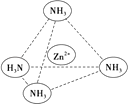
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在使用分液漏斗进行分液时,正确的操作是( )
A.上层液体经漏斗下口放出
B.分离液体时,将漏斗拿在手上进行分离
C.分离液体时,使分液漏斗玻璃塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液漏斗下面的活塞拧开
D.分液漏斗中盛装的是液体,振荡后不必打开活塞把气体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,体积均为20mL、浓度均为0.1mol·L-1的两种酸HX、HY分别与0.1mol·L-1的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是( )
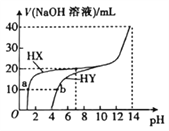
A. Ka(HY)的数量级约为10-3
B. a点c(X-)>b点c(Y-)
C. HX发生反应的离子方程式为HX+OH-=X-+H2O
D. pH=7时,两种反应后的溶液中c(Y-)>c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在高温高压下碳氧化物具有极高的化学活性,能与多种单质或化合物反应。
(1)一定条件下,CO与H2 可合成甲烷,反应方程式为:CO(g)+3H2(g) ![]() CH4(g)+ H2O(g)
CH4(g)+ H2O(g)
①一定条件下,该反应能够自发进行的原因是_________
②已知H2(g)、CO(g)和CH4(g)的燃烧热分别为285.8kJ/mol 283.0kJ/mol和890.0kJ/mol。
写出CO 与H2 反应生成CH4 和CO2 的热化学方程式:_____________。
(2)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO (g) +2H2 (g) ![]() CH3OH (g)
CH3OH (g)
反应Ⅱ: CO2 (g) +3H2 (g) ![]() CH3OH (g) +H2O (g)
CH3OH (g) +H2O (g)
①在以上制备甲醇的两个反应中:反应Ⅰ优于反应Ⅱ,原因为______________。
②一定温度下,在体积可变的密闭容器中加入4molH2和一定量的CO发生反应Ⅰ,开始时容器体积为2L,CO 和CH3OH (g) 的浓度随时可变化如图。10min 达到平衡,则反应1的化学平衡常数为____________。
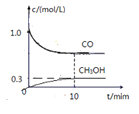
③恒温恒容条件下,在密闭容器中等物质的量的通入CO2 和H2, 下列描述能说明反应Ⅱ已经达到平衡状态的是___。(填标号)
A.容器内CO2的体积分数不再变化
B.当CO2和H2转化率的比值不再变化
C.单位时间CH3OH分子断裂5NA个共价键,同时断裂3NA个H-H键
D.容器内混合气体的平均相对分子质量为34.5,且保持不变
(3)甲烷碱性燃料电池装置如图所示(开始时两边溶液质量相等),用电器为惰性电极电解装置,其原理是:通电后,将Co2+氧化成Co3+,进而彻底氧化CN-为无害气体使废水得以净化。
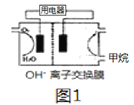
①当除去1molCN-时,图1两边质量差为__________g.
②负极电极反应式为__________.
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为:CH3OH(g)+CO(g) ![]() HCOOCH3(g) ΔH=-29.1KJ/mol,科研人员对该反应进行了研究.部分研究结果如下:
HCOOCH3(g) ΔH=-29.1KJ/mol,科研人员对该反应进行了研究.部分研究结果如下:
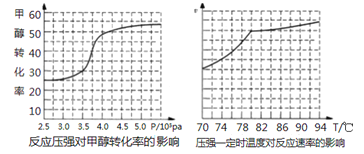
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是_____。
②实际工业生产中采用的温度是80℃,其理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.用激光笔照射硫酸铜溶液,侧面可观察到明显的光路
B.氢氧化铁胶体带正电荷是氢氧化铁胶体稳定存在的主要原因
C.根据是否有丁达尔效应,将分散系分为溶液、胶体、浊液
D.江河入海口三角洲的形成通常与胶体的性质有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液与100 mL 0.5 mol·L-1 NaCl溶液中所含Cl-的物质的量浓度相同的是( )
A. 100 mL0.5molL-1 MgCl2溶液 B. 200 mL0.25molL-1 AlCl3溶液
C. 50mL1molL-1 NaCl溶液 D. 25mL 0.5molL-1 HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al、Fe、Cu都是重要的金属元素,下列说法正确的是:( )
A. 三者的单质长期放置在空气中均只生成氧化物
B. 硬铝是一种铝合金,其硬度相当于钢材,可用于制做门窗框架,它比纯铝熔点高
C. 三者的单质在一定条件下都能与水反应生成H2
D. 将用砂纸打磨过的铝箔在酒精灯外焰上加热,发现铝箔发红卷缩,变暗失去光泽,铝箔熔化但不落下,说明氧化铝致密且熔点高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com