
”¾ĢāÄæ”æÅš¼°Ęä»ÆŗĻĪļŌŚ¹¤ŅµÉĻÓŠŠķ¶ąÓĆĶ¾”£ŅŌĢśÅšæó£ØÖ÷ŅŖ³É·ÖĪŖMg2B2O5”¤H2OŗĶFe3O4£¬»¹ÓŠÉŁĮæFe2O3”¢FeO”¢CaO”¢Al2O3ŗĶSiO2µČ)ĪŖŌĮĻÖʱøÅšĖį(H3BO3)µÄ¹¤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öMg2B2O5”¤H2OÓėĮņĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½_____________”£ĪŖĢįøß½ž³öĖŁĀŹ£¬³żŹŹµ±Ōö¼ÓĮņĖįÅضČÅضČĶā£¬»¹æɲÉČ”µÄ“ėŹ©ÓŠ_________£ØŠ“³öĮ½Ģõ£©”£
£Ø2£©ĄūÓĆ µÄ“ÅŠŌ£¬æɽ«Ęä“Ó”°½žŌü”±ÖŠ·ÖĄė”£”°½žŌü”±ÖŠ»¹Ź£ÓąµÄĪļÖŹŹĒ______£ØŠ“»ÆѧŹ½£©”£
£Ø3£©”°¾»»Æ³żŌÓ”±ŠčĻČ¼ÓH2O2ČÜŅŗ£¬×÷ÓĆŹĒ_______”£ Č»ŗóŌŁµ÷½ŚČÜŅŗµÄpHŌ¼ĪŖ5£¬ÄæµÄŹĒ________”£
£Ø4£©”°“ÖÅšĖį”±ÖŠµÄÖ÷ŅŖŌÓÖŹŹĒ £ØĢīĆū³Ę£©”£
£Ø5£©ŅŌÅšĖįĪŖŌĮĻæÉÖʵĆÅšĒā»ÆÄĘ£ØNaBH4£©£¬ĖüŹĒÓŠ»śŗĻ³ÉÖŠµÄÖŲŅŖ»¹Ō¼Į£¬Ęäµē×ÓŹ½ĪŖ_______”£
£Ø6£©µ„ÖŹÅšæÉÓĆÓŚÉś³É¾ßÓŠÓÅĮ¼æ¹³å»÷ŠŌÄÜÅšøÖ”£ŅŌÅšĖįŗĶ½šŹōĆ¾ĪŖŌĮĻæÉÖʱøµ„ÖŹÅš£¬ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾Öʱø¹ż³Ģ___________”£
”¾“š°ø”æ£Ø1£© Mg2B2O5”¤H2O+2H2SO4![]() 2MgSO4+2H3BO3£»¼õŠ”ĢśÅšæó·ŪĮ£¾¶”¢Ģįøß·“Ó¦ĪĀ¶Č”£
2MgSO4+2H3BO3£»¼õŠ”ĢśÅšæó·ŪĮ£¾¶”¢Ģįøß·“Ó¦ĪĀ¶Č”£
£Ø2£© Fe3O4£» SiO2ŗĶCaSO4£»
£Ø3£©½«Fe2+Ńõ»ÆĪŖFe3+£»Ź¹Al3+ÓėFe3+ŠĪ³ÉĒāŃõ»ÆĪļ¶ų³żČ„”£
£Ø4£©£ØĘßĖ®£©ĮņĖįĆ¾
£Ø5£©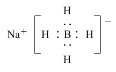
£Ø6£© 2H3BO3 ![]() B2O3+3HO B2O3+3Mg
B2O3+3HO B2O3+3Mg ![]() 3MgO+2B
3MgO+2B
”¾½āĪö”æ£Ø1£©ĪŹŠ“»Æѧ·½³ĢŹ½£¬ŹĒ·ĀÕÕ¼īŹ½Ģ¼ĖįŃĪŗĶĖįµÄ·“Ó¦£¬µ«ŹĒŅŖĻČ·ÖĪöMg2B2O5”¤H2O ÖŠÅšŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+3¼Ū£¬ĮŖĻµµ½Į÷³ĢĶ¼×īÖÕ²śĪļæÉĶĘÖŖ£ŗÅšŌŖĖŲ±äĪŖH3BO3£ØH3BO3ĪŖČõĖį£¬Ņ×ČÜÓŚĖ®£©£»Õā²»ŹĒŃõ»Æ»¹Ō·“Ó¦£¬¹ŹĆ¾ŌŖĖŲ×Ŗ»ÆĪŖĮņĖįĆ¾”£¼Óæģ·“Ó¦ĖŁĀŹæÉŅŌ²ÉÓĆÉżĪĀµČ“ėŹ©£¬Ōö“ó¹ĢĢåæÅĮ£µÄ½Ó“„Ć껿Ņ²ŹĒ֊ѧ³£¹ę”£
£Ø2£©ĢåĻµÖŠÓŠ“ÅŠŌÖ»ÓŠFe3O4£¬¹ŹĢīŠ“Fe3O4£Ø֊ѧĖłŃ§·“Ó¦æÉÄÜĄ§ČÅæ¼Éś£©”£Ź£ĻĀµÄ²»ČÜĪļ³żĮĖSiO2»¹ÓŠCaSO4”£
£Ø3£©ĻČ½«ČÜŅŗÖŠµÄFe2+Ńõ»ÆĪŖFe3+£¬ŌŁµ÷½ŚČÜŅŗµÄpHæÉŅŌ³żČ„ČÜŅŗÖŠµÄAl3+ŗĶFe3+£¬ÕāŹĒøßČż¾³£ŃµĮ·µÄ³żŌÓ·½·Ø”£
£Ø4£©ĢāÖŠ½²µ½ŗ¬ĮņĖįĆ¾µÄÄøŅŗ£¬Ó¦øĆČŻŅ×Ļėµ½ĮņĖįĆ¾Ņ²»į½į¾§Īö³ö£¬Ö»ŹĒ¾§Ģåŗ¬ÓŠĘßøö½į¾§Ė®²»ČŻŅ×Ļėµ½£Ø“ÓĘßĖ®ĮņĖįŠæ£¬ĘßĖ®ĮņĖįŃĒĢśĮŖĻė£©£¬½²ĮņĖįĆ¾¾§ĢåÓ¦øĆŅ²æÉŅŌ”£
£Ø5£©ÅšĒā»ÆÄʵĵē×ÓŹ½ŗܲ»³£¹ę£¬µē×ÓŹ½ŹĒÓÉĄė×Ó¼üŗĶŅõĄė×ÓÄŚ²æµÄ¹²¼Ū¼üĮ½²æ·ÖŗĻ³É”£
£Ø6£©×öĢāŹ±ÕāŃłĻė£¬Õāøö·“Ó¦µÄĪĀ¶ČÓ¦øĆ±Č½Ļøߣ¬ĖłŅŌH3BO3»į·Ö½ā£¬Č»ŗó¾ĶŹĒÖĆ»»·“Ó¦”£ŌŁ½«»Æѧ·½³ĢŹ½ÅäĘ½¾ĶŗĆ”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·ÖĄąŹĒČĖĆĒČĻŹ¶ŹĀĪļŹ±³£ÓƵÄæĘѧ·½·Ø£¬ĻĀĮŠ¹ŲÓŚĢ¼Ėį¼Ų·ÖĄąµÄĖµ·Ø“ķĪóµÄŹĒ£Ø£©
A£®ŹōÓŚµē½āÖŹ
B£®ŹōÓŚ»ÆŗĻĪļ
C£®ŹōÓŚĢ¼ĖįŃĪ
D£®ŹōÓŚ·ÖÉ¢Ļµ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖę×ÅæĘ¼¼µÄ½ų²½£¬ŗĻĄķĄūÓĆ׏Ō“”¢±£»¤»·¾³³ÉĪŖµ±½ńÉē»į¹Ų×¢µÄ½¹µć
£Ø1£©°±µŖŹĒŌģ³ÉĖ®Ģåø»ÓŖŃų»ÆµÄÖŲŅŖŅņĖŲÖ®Ņ»£¬ÓĆ“ĪĀČĖįÄĘĖ®½āÉś³ÉµÄ“ĪĀČĖį½«Ė®ÖŠµÄ°±µŖ£ØÓĆNH3±ķŹ¾£©×Ŗ»ÆĪŖµŖĘų³żČ„£¬ĘäĻą¹Ų·“Ó¦µÄÖ÷ŅŖČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
·“Ó¦¢Ł£ŗNH3£Øaq£©+HClO£Øaq£©= NH2Cl£Øaq£©+H2O£Øl£©”÷H1= akJmol©1
·“Ó¦¢Ś£ŗNH2Cl£Øaq£©+HClO£Øaq£©= NHCl2£Øaq£©+H2O£ØI£©”÷H2= bkJmol©1
·“Ó¦¢Ū£ŗ2NHCl2£Øaq£©+H2O£Øl£©= N2£Øg£©+HClO£Øaq£©+3HCl£Øaq£©”÷H3= ckJmol©1
¢Ł 2NH3£Øaq£©+3HClO£Øaq£©= N2£Øg£©+3H2O£ØI£©+3HCl£Øaq£©µÄ”÷H=______”£
¢Ś ČÜŅŗpH¶Ō“ĪĀČĖįÄĘČ„³ż°±µŖÓŠ½Ļ“óµÄÓ°Ļģ£ØČēĶ¼1ĖłŹ¾£©”£ŌŚpH½ĻµĶŹ±ČÜŅŗÖŠÓŠĪŽÉ«ĪŽĪ¶µÄĘųĢåÉś³É£¬°±µŖČ„³żŠ§ĀŹ½ĻµĶ£¬ĘäŌŅņŹĒ_________________”£
¢Ū ÓƵē»Æѧ·ØŅ²æÉŅŌČ„³ż·ĻĖ®ÖŠ°±µŖ£®ŌŚÕōĮóĖ®ÖŠ¼ÓČėĮņĖįļ§ÓƶčŠŌµē¼«Ö±½Óµē½ā·¢ĻÖ°±µŖČ„³żŠ§ĀŹ¼«µĶ£¬µ«ŌŚČÜŅŗÖŠŌŁ¼ÓČėŅ»¶ØĮæµÄĀČ»ÆÄĘŗó£¬Č„³żŠ§ĀŹæÉŅŌ“ó“óĢįøß”£·“ӦװÖĆČēĶ¼2ĖłŹ¾£¬bĪŖµē¼«__¼«£¬µē½āŹ±Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ_____________”£

£Ø2£©”°µĶĢ¼¾¼Ć”±Õż³ÉĪŖæĘѧ¼ŅŃŠ¾æµÄÖ÷ŅŖæĪĢā”£
¢Ł ŅŌ¶žŃõ»ÆīѱķĆęø²øĒCu2Al2O4 ĪŖ“߻ƼĮ£¬æÉŅŌ½«CO2 ŗĶCH4 Ö±½Ó×Ŗ»Æ³ÉŅŅĖį”£ŌŚ²»Ķ¬ĪĀ¶ČĻĀ“߻ƼĮµÄ“߻Ɗ§ĀŹÓėŅŅĖįµÄÉś³ÉĖŁĀŹČēÓŅĶ¼ĖłŹ¾”£250”«300 ”ꏱ£¬ĪĀ¶ČÉżø߶ųŅŅĖįµÄÉś³ÉĖŁĀŹ½µµĶµÄŌŅņŹĒ__________________”£
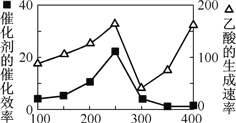
¢Ś ĪŖĮĖĢįøßøĆ·“Ó¦ÖŠCO2µÄ×Ŗ»ÆĀŹ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ_____________”££ØŠ“Ņ»Ģõ¼“æÉ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃéÉč¼Ę¼°Ęä¶ŌÓ¦µÄĄė×Ó·½³ĢŹ½¾łÕżČ·µÄŹĒ£Ø £©
A. ½«ĀČĘųČÜÓŚĖ®Öʱø“ĪĀČĖį£ŗCl2+H2O£½2H++Cl£+ClO£
B. Ė®²£Į§ŌŚæÕĘųÖŠ±äÖŹ£ŗNa2SiO3+CO2+H2O£½2Na++CO32-+H2SiO3”ż
C. ÓĆFeCl3ČÜŅŗøÆŹ“ĶĻßĀ·°å£ŗCu+2Fe3+£½Cu2++2Fe2+
D. ÓĆÅØŃĪĖįĖį»ÆµÄKMnO4ČÜŅŗÓėH2O2·“Ó¦£¬Ö¤Ć÷H2O2¾ßÓŠ»¹ŌŠŌ£ŗ2MnO![]() +6H++5H2O2£½2Mn2++5O2”ü+8H2O
+6H++5H2O2£½2Mn2++5O2”ü+8H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放2016½ģ»įÄžĻŲŅ»ÖŠµŚĖÄ“ĪŌĀæ¼”æĢś¼°Ęä»ÆŗĻĪļŌŚČÕ³£Éś»ī”¢Éś²śÖŠÓ¦ÓĆ¹ć·ŗ”£
£Ø1£©øßĢśĖįÄĘ£ØNa2FeO4£©ŹĒĖ®“¦Ąķ¹ż³ĢÖŠµÄŅ»ÖÖŠĀŠĶ¾»Ė®¼Į£¬¹¤ŅµÉĻĄūÓĆNaClO ŗĶNaOHµÄ»ģŗĻČÜŅŗ½«2Fe£ØOH£©3Ńõ»ÆŠŌÖʱøøßĢśĖįÄĘ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £»øßĢśĖįÄĘÄÜÓĆ×÷ŠĀŠĶ¾»Ė®¼ĮµÄŌĄķŹĒ £»
£Ø2£©Ńõ»ÆĢśŗģŃÕĮĻøśÄ³Š©ÓĶĮĻ»ģŗĻ£¬æÉŅŌÖĘ³É·ĄŠāÓĶĘį”£ŅŌ»ĘĢśæóĪŖŌĮĻÖĘĮņĖį²śÉśµÄĮņĖįŌüÖŠŗ¬Fe2O3”¢SiO2”¢Al2O3”¢MgOµČ£¬ÓĆĮņĖįŌüÖʱøĢśŗģ£ØFe2O3£©µÄ¹ż³ĢČēĻĀ£ŗ
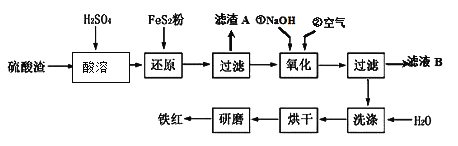
¢ŁĖįČܹż³ĢÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £¬ £¬ £»”°ĀĖŌüA”±Ö÷ŅŖ³É·ŻµÄ»ÆѧŹ½ĪŖ ”£
¢Ś»¹Ō¹ż³ĢÖŠ¼ÓČėFeS2µÄÄæµÄŹĒ½«ČÜŅŗÖŠµÄFe3 +»¹ŌĪŖFe2 +£¬¶ų±¾Éķ±»Ńõ»ÆĪŖH2SO4£¬ĒėŠ“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ £»
¢ŪŃõ»Æ¹ż³ĢÖŠ£¬O2”¢NaOHÓėFe2+·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
¢ÜĪŖĮĖČ·±£ĢśŗģµÄÖŹĮæŗĶ“æ¶Č£¬Ńõ»Æ¹ż³ĢŠčŅŖµ÷½ŚČÜŅŗµÄpHµÄ·¶Ī§ŹĒ £¬
³ĮµķĪļ | Fe£ØOH£©3 | Al£ØOH£©3 | Fe£ØOH£©2 | Mg£ØOH£©2 |
æŖŹ¼³ĮµķpH | 2.7 | 3.8 | 7.6 | 9.4 |
ĶźČ«³ĮµķpH | 3.2 | 5.2 | 9.7 | 12.4 |
Čē¹ūpH¹ż“ó£¬æÉÄÜŅżĘšµÄŗó¹ūŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“×ĖįÄĘÖŠ²»“ęŌŚ£Ø £©
A. Ąė×Ó¼ü B. ¼«ŠŌ¼ü C. ·Ē¼«ŠŌ¼ü D. ·Ö×Ó¼ä×÷ÓĆĮ¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放2015±±¾©Ąķ×Ū»Æѧ”æŌŚĶØ·ē³÷ÖŠ½ųŠŠĻĀĮŠŹµŃé£ŗ
²½Öč |
|
| |
ĻÖĻó | Fe±ķĆę²śÉś“óĮæĪŽÉ«ĘųÅŻ£¬ŅŗĆęÉĻ·½±äĪŖŗģ×ŲÉ« | Fe±ķĆę²śÉśÉŁĮæŗģ×ŲÉ«ĘųÅŻŗó£¬ŃøĖŁĶ£Ö¹ | Fe”¢Cu½Ó“„ŗó£¬Ęä±ķĆę²śÉśŗģ×ŲÉ«ĘųÅŻ |
ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ £Ø £©
A£®¢ńÖŠĘųĢåÓŠĪŽÉ«±äŗģ×ŲÉ«µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2NO+O2=2NO2
B£®¢ņÖŠµÄĻÖĻóĖµĆ÷Fe±ķĆęŠĪ³ÉÖĀĆܵÄŃõ»Æ²ć£¬×čÖ¹Fe½ųŅ»²½·“Ó¦
C£®¶Ō±Č¢ń”¢¢ņÖŠĻÖĻó£¬ĖµĆ÷Ļ”HNO3µÄŃõ»ÆŠŌĒæÓŚÅØHNO3
D£®Õė¶Ō¢óÖŠĻÖĻó£¬ŌŚFe”¢CuÖ®¼äĮ¬½ÓµēĮ÷¼Ę£¬æÉÅŠ¶ĻFeŹĒ·ń±»Ńõ»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放2017ÉÜŠĖÄ£Äā”æĻĀĮŠ¹ŲÓŚ·“Ó¦ĖŁĀŹµÄĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A£®·“Ó¦ĖŁĀŹÓĆÓŚŗāĮæ»Æѧ·“Ó¦½ųŠŠµÄæģĀż
B£®æÉÄę·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬Ź±£¬Õż”¢Äę·“Ó¦ĖŁĀŹ¶¼ĪŖ0
C£®¾ö¶Ø·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲŹĒ·“Ó¦ĪļµÄŠŌÖŹ
D£®Ōö“ó·“Ó¦ĪļÅØ¶Č£¬Ģįøß·“Ó¦ĪĀ¶Č¶¼ÄÜŌö“ó·“Ó¦ĖŁĀŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ŲÓŚĘųĢåĦ¶ūĢå»żµÄĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ (””””)
A. ĘųĢåĦ¶ūĢå»żŹĒµ„Ī»ĪļÖŹµÄĮæµÄĘųĢåĖłÕ¼µÄĢå»ż
B. ±ź×¼×“æöĻĀ£¬ĘųĢåĦ¶ūĢå»żŌ¼ĪŖ22.4 L
C. ±ź×¼×“æöĻĀ£¬1 molČĪŗĪĪļÖŹĖłÕ¼µÄĢå»żŌ¼ŹĒ22.4 L
D. ±ź×¼×“æöĻĀ£¬1 molĒāĘųĖłÕ¼µÄĢå»żŌ¼ŹĒ22.4 L”¤mol£1
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com