
分析 (1)解答题目的关键是找到突破口.D和A、B都能生成气体,而题给离子中只有H+与CO32-、OH-与NH4+能反应生成气体,故D只能为(NH4)2CO3;在A或D中滴入C,均有沉淀生成,说明A中含有SO42-,C中应含有Ba2+,而A和D反应生成的气体说明A一定是硫酸,产生的气体是二氧化碳,能被B吸收,说明B是一种碱,所以C是硝酸钡,B是氢氧化钠,以此解答该题;
(2)铵根离子和氢氧根离子共热反应生成氨气,氨气可以和酸反应生成铵盐;
(3)只要通入CO2,立刻就有沉淀CaCO3产生;将Ca(OH)2消耗完毕,接下来消耗KOH,因而此段不会产生沉淀(即沉淀的量保持不变);KOH被消耗完毕,接下来消耗KAlO2,有Al(OH)3沉淀生成;又因二氧化碳足量,还可以继续与上面反应的产物K2CO3、CaCO3、发生反应.
解答 解:(1)以上离子中可能生成的气体有NH3和CO2两种,由D和A、B反应生成,则D中含有CO32-和NH4+离子,应为(NH4)2CO3,
在A或D中滴入C,均有沉淀生成,说明A中含有SO42-,C中应含有Ba2+,而A和D反应生成的气体说明A一定是硫酸,产生的气体是二氧化碳,能被B吸收,说明B是一种碱,所以C是硝酸钡,B是氢氧化钠,
故答案为:H2SO4;NaOH;Ba(NO3)2;(NH4)2CO3;
(2)D和B反应生成的气体为NH3,反应的离子方程式为NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H20,能被H2SO4吸收,反应的离子方程式为NH3+H+=NH4+,
故答案为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H20、NH3+H+=NH4+.
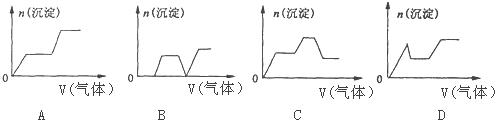
(3)将二氧化碳气体通入含有氢氧化钾,氢氧化钙,KAlO2的混合溶液中,生成沉淀的量和通入二氧化碳的量的关系以二氧化碳的体积为横坐标,以沉淀的物质的量为纵坐标的图象的画法,可以做如下分析:
CO2先与Ca(OH)2反应(有沉淀CaCO3生成);当Ca(OH)2消耗完毕后再与KOH反应(此时无沉淀);最后与KAlO2反应(有沉淀Al(OH)3生成).到现在的图标应是出现沉淀(CaCO3),平台,沉淀增加[因有Al(OH)3生成];
过量的CO2还可以继续与K2CO3反应得到KHCO3,继续过量的CO2还可以使CaCO3沉淀溶解.最后是Al(OH)3沉淀.
图形应该是:出现沉淀(CaCO3),平台,沉淀增加[Al(OH)3],平台,沉淀减少(CaCO3溶解).
故答案为:C.
点评 本题考查离子的检验和推断,题目难度中等,注意解答题目的关键是找到突破口,而本题的突破口为D和A、B都能生成气体.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

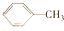 $\stackrel{KMnO_{4}(H)}{→}$
$\stackrel{KMnO_{4}(H)}{→}$
 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$  (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)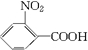 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CHO | B. | OHCCH(OH)CH2OH | ||
| C. | 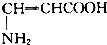 | D. | 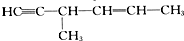 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
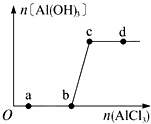 向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成Al (OH)3沉淀的量随ALCL3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成Al (OH)3沉淀的量随ALCL3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应的溶液中:Na+、Fe3+、SO4-、HCO3- | |
| B. | b点对应的溶液中:Na+、S2-、SO42-、Cl- | |
| C. | c点对应的溶液中:Ag+、Ca2+、NO3-、F- | |
| D. | d点对应的溶液中:K+、NH4+、CO32-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 等量的硫蒸气和硫固体分别完全燃烧,前者反应速率快,后者放出热量多 | |
| B. | 由C(石墨)→C(金刚石)△H=+1.9 kJ•mol-1可知,石墨比金刚石稳定 | |
| C. | 在稀溶液中:H++OH-═H2O△H1=-57.3 kJ•mol-1,若含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液的反应热为△H2,则△H1>△H2 | |
| D. | 在101 kPa时,10g H2完全燃烧生成液态水,放出1429 kJ热量,氢气燃烧热的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=-517.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液(BaCl2):加Na2SO4溶液,过滤 | |
| B. | NaCl溶液(I2):加酒精,萃取 | |
| C. | KNO3溶液(AgNO3):加NaCl溶液,过滤 | |
| D. | KNO3溶液(I2):加CCl4,萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
试管编号 实验步骤 | 1 | 2 | 3 | 4 |
| 1%NaCl溶液(mL) | 1 | |||
| 1% CuSO4溶液(mL) | 1 | |||
| 1% Na2SO4溶液(mL) | 1 | |||
| 蒸馏水(mL) | 1 | |||
| pH6.8缓冲液(mL) | 1 | 1 | 1 | 1 |
| 1%淀粉溶液(mL) | 1 | 1 | 1 | 1 |
| 唾液淀粉酶液(mL) | 1 | 1 | 1 | 1 |
| 各试管放入37℃恒温水浴保温适宜时间 | ||||
| 取出试管,加入1%碘溶液0.1mL | ||||
| 观察结果 | 无色 | 深蓝色 | 浅蓝色 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaHSO4溶液中滴加Ba(OH)2至SO42-沉淀完全:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| B. | 碳酸钠溶液与醋酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 氢氧化亚铁与硝酸混合:Fe(OH)2+2H+=Fe2++2H2O | |
| D. | 将1~2mL氯化铁饱和溶液加到20mL沸水中:Fe3++3H2O?Fe(OH)3(胶体)+3H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com