
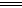 CO2ӟ+H2O
CO2ӟ+H2O
|
| A£®¢Ł¢Ś | B£®¢Ü | C£®¢Ū¢Ü | D£®¢Ś¢Ū¢Ü |

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| ŃōĄė×Ó | K+ Ag + Ba 2+ A13+ Fe3+ |
| ŅõĄė×Ó | OH - C1 - SO4 2- NO3- CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĢśŠ¼ČÜÓŚ¹żĮæĻ”ĻõĖį£ŗ3Fe£«8H+£«2NO3-£½3Fe2+£«2NO”ü£«4H2O |
| B£®Fe£ØOH£©3ČÜÓŚ¹żĮæµÄHIČÜŅŗ£ŗ2Fe£ØOH£©3+6H++2I©„£½2Fe2++I2+6H2O |
| C£®ŌŚAlCl3ČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗAl3++3NH3”¤H2O£½Al£ØOH£©3”ż+3NH4+ |
| D£®¹żĮæµÄNH4HSO4ČÜŅŗÓėBa£ØOH£©2ČÜŅŗ·“Ó¦£ŗ2H++SO42©„+Ba2++2OH©„£½BaSO4”ż+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĶÓėĻ”ĻõĖį·“Ó¦£ŗ Cu£«2H£«£«NO3£===Cu2£«£«NO”ü£«H2O |
| B£®ĮņĖįŃĒĢśČÜŅŗÖŠ¼ÓČėÓĆĮņĖįĖį»ÆµÄ¹żŃõ»ÆĒāČÜŅŗ£ŗ Fe2£«£«2H£«£«H2O2===Fe3£«£«2H2O |
| C£®¹żĮæµÄ¶žŃõ»ÆĢ¼ĶØČėĘÆ°×·ŪČÜŅŗÖŠ£ŗ ClO££«CO2£«H2O===HClO£«HCO3£ |
| D£®AlCl3ČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĮņĖįŃĒĢśŌŚæÕĘųÖŠŃõ»Æ£ŗ4Fe2++ 302+6H2O=4Fe(OH)3 |
| B£®ĻņĻõĖįŅųČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗAg++ NH3©qH2O==AgOH”ż+NH4+ |
| C£®ĻņĮņĖįĀĮļ§·ÆČÜŅŗÖŠµĪ¼Ó¹żĮæµÄĒāŃõ»Æ±µČÜŅŗ£ŗ NH4++ Al3++2SO42-+2Ba2+ +50H-==AlO2-+2BaS04”ż+ NH3©qH2O +2H2O |
| D£®Ļņ“ĪĀČĖįÄĘČÜŅŗÖŠĶØČė×ćĮæSO2ĘųĢå£ŗ ClO-+SO2+H2O==HClO+HSO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 g2+ŗĶ1 mol Al3+µÄ»ģŗĻČÜŅŗ£¬ĻÖ°“ĻĀĶ¼ŗį×ų±źŅĄ“Ī¼ÓČė7 mol NaOHČÜŅŗ”¢1 molŃĪĖį£¬ĶØČė1 mol CO2ĘųĢå£¬×Ż×ų±źĪŖ»ģŗĻ³ĮµķµÄĪļÖŹµÄĮ攣Ēė»³ö³ĮµķµÄĮæĖę·“Ó¦µÄ±ä»ÆĒśĻߣ¬²¢Š“³öø÷²½·“Ó¦µÄĄė×Ó·½³ĢŹ½”£
g2+ŗĶ1 mol Al3+µÄ»ģŗĻČÜŅŗ£¬ĻÖ°“ĻĀĶ¼ŗį×ų±źŅĄ“Ī¼ÓČė7 mol NaOHČÜŅŗ”¢1 molŃĪĖį£¬ĶØČė1 mol CO2ĘųĢå£¬×Ż×ų±źĪŖ»ģŗĻ³ĮµķµÄĪļÖŹµÄĮ攣Ēė»³ö³ĮµķµÄĮæĖę·“Ó¦µÄ±ä»ÆĒśĻߣ¬²¢Š“³öø÷²½·“Ó¦µÄĄė×Ó·½³ĢŹ½”£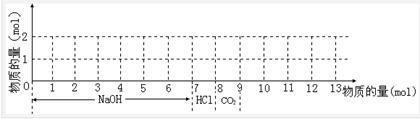
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®NaHCO3ČÜŅŗÖŠ¼ÓČėÉŁĮæNaHSO4ČÜŅŗ£ŗHCO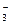 +HSO +HSO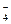 =SO =SO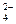 +H2O +H2O |
B£®Ca£ØHCO3£©2ČÜŅŗÖŠ¹õČėÉŁĮæCa£ØOH£©2ČÜŅŗ£ŗCa2++OH-+HCO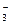 =CaCO3”ż+H2O =CaCO3”ż+H2O |
C£®½šŹōĀĮČÜÓŚŃõ»ÆÄĘČÜŅŗ£ŗ2Al+6OH-=2AlO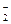 +3H2”ü +3H2”ü |
| D£®Fel2ČÜŅŗÖŠĶØČėÉŁĮæCl2£ŗ2Fe2++Cl2=2Fe3+=2Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĮņĖįÓėĀČ»Æ±µČÜŅŗ·“Ó¦£ŗ SO42£+ Ba2+ =BaSO4”ż |
| B£®Ģ¼ĖįøĘÓėŃĪĖį·“Ó¦£ŗ CaCO3 + 2H+ =Ca2+ + CO2”ü + H2O |
C£®ÄĘĶ¶ČėĮņĖįĶČÜŅŗÖŠ£ŗ 2Na + Cu2+ = 2N a+ + Cu a+ + Cu |
| D£®ĀČĘųĶØČėĖ®ÖŠ£ŗCl2 + H2O = H+ + Cl£+ HClO |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com