
下面关于电解质的叙述中错误的是()
A. 在水溶液中或熔融状态下均不导电的化合物叫非电解质
B. 电解质、非电解质都指化合物而言,单质不属于此范畴
C. 电解质在水中一定能导电,在水中导电的化合物一定是电解质
D. BaSO4不溶于水,但BaSO4是电解质
考点: 电解质与非电解质.
分析: A.根据非电解质的概念进行判断;
B.根据电解质和非电解质的概念进行判断;
C.电解质在水中不一定能导电;在水中导电的化合物也不一定是电解质;
D.BaSO4不溶于水,但在熔融状态下能导电,是电解质.
解答: 解:A.非电解质:在熔融状态和水溶液中都不能导电的化合物,故A正确;
B.电解质、非电解质都指化合物而言,单质既不是电解质也不是非电解质,故B正确;
C.电解质在水中不一定能导电,如硫酸钡,难溶于水,在熔融状态下能导电,是电解质;在水中导电的化合物不一定是电解质,如二氧化碳溶于水能导电,但二氧化碳是非电解质,故C错误;
D.BaSO4不溶于水,但在熔融状态下能导电,是电解质,故D正确;
故选C.
点评: 本题考查电解质、非电解质概念的辨析,难度不大.解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A—I为原子序数递增的前4周期的元素,已知A原子的最外层电子是次外层电子数的2倍,D为周期表中电负性最大的元素,F与C位于同一主族,E与G在周期表的位置是上下相连,两元素所在主族中所有元素都是金属,H为应用最广泛的金属;I处于周期表中的第二副族。请回答下列问题:(以下问题中的所有原子都必须在上述元素中寻找)
(1)B单质分子中σ与π键数目比为 B、C、D第一电离能由小到大的顺序为 (填写元素符号)
 (2)H元素原子的价层电子排布式为 ,H3+离子可以与上述元素中的三种形成的某阴离子生成血红色络合物;该阴离子又与A—I元素中的某些原子形成的分子互为等电子体,这种分子的化学式为 (写一种即可),该阴离子空间构型为 。
(2)H元素原子的价层电子排布式为 ,H3+离子可以与上述元素中的三种形成的某阴离子生成血红色络合物;该阴离子又与A—I元素中的某些原子形成的分子互为等电子体,这种分子的化学式为 (写一种即可),该阴离子空间构型为 。
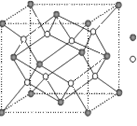
(3)D与G可以形成右图的晶胞,则黑点表示的是 元素(填写元素符号),该元素原子在该晶胞中的配位数为
(4)若将上述晶胞圆圈对应的原子所在上下两层平面原子,按两条相互垂直的对角线上各去掉该原子2个(共去掉4个),并将小点和圆圈对应的元素更改为另外两种元素,则这个晶胞化学式为 ,若再将留下的所有原子换成另外一种新元素的原子,则成为另外一种晶胞,该晶胞中成键原子键角为 。
(5)已知,F单质晶体的原子堆积为ABAB型,那么,该晶体的空间利用率为 如果F单质的摩尔质量为M,晶胞棱长为a,晶胞高度为c则,该晶体密度表达式为 。(阿伏加德罗常数用NA表示,不化简)如果F的原子半径为R,用R表示的晶胞高度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
为配制0.1mol/L的NaOH溶液,下列说法中正确的是()
A. 取4g NaOH固体溶于1L水中
B. 取0.4g NaOH固体溶于水配成1L溶液
C. 取4g NaOH固体溶于水配成1L溶液
D. 取0.4g NaOH固体溶于1L水中
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列化学方程式中,能够用离子方程式Ba2++SO42﹣=BaSO4↓表示的是()
A. BaCl2+K2SO4=BaSO4↓+2KCl
B. BaCO3+H2SO4=BaSO4↓+CO2↑+H2O
C. Ba(OH)2+H2SO4=BaSO4↓+2H2O
D. Ba(OH)2+2KHSO4=BaSO4↓+K2SO4+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式,错误的是()
A. 铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2
B. 碳酸钙与盐酸反应:CaCO3+2H+═Ca2++CO2↑+H2O
C. 铁投入硫酸铜溶液中:Fe+Cu2+═Cu+Fe2+
D. KHCO3溶液中滴加H2SO4溶液:HCO3﹣+H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中氧原子数目与93g Na2O中氧原子数一定相等的是()
A. 67.2L CO2 B. 33g CO2 C. 80g SO3 D. 98g H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 稀H2SO4能导电,所以稀H2SO4是电解质
B. 氧化还原反应中有一种元素化合价升高必定有另一种元素化合价降低
C. 根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
D. 根据交叉分类法MgSO4既是镁盐又是硫酸盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com