
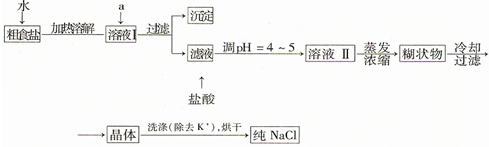
分析 (1)①把杂质转化为沉淀或气体除去,除钙离子用碳酸根离子,除镁离子、铁离子用氢氧根离子,除硫酸根离子用钡离子,要注意除杂质的顺序,后加的试剂最好能把前面先加的过量试剂除掉;
②用氯化钡溶液检验硫酸根离子的存在;
③根据题中提供的试剂,可以用75%乙醇洗涤氯化钠固体,可以除去表面的氯化钾,同时可以减少氯化钠的损失;
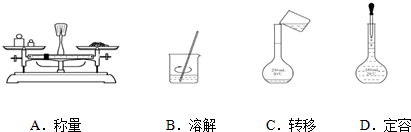
(2)Ⅰ.用氯化钠固体配制一定物质的量浓度的溶液,通常的步骤为:计算、称量、溶解、移液、洗涤、定容、摇匀等操作;
Ⅱ.根据这些操作可知所用的仪器;
Ⅲ.在计算溶质的质量时要按容量瓶的规格计算;
Ⅳ.用天平称物品时,物品在左边,砝码在右边;溶解时要用玻璃棒搅拌;向容量瓶中加液体时要用玻璃棒引流;定容时,滴管不能伸到容量瓶中;
Ⅴ.实验过程中,若定容时俯视液面,则所配制溶液的体积偏小,据此分析.
解答 解:(1)①除去粗盐中的可溶性杂质:Ca2+、Mg2+、Fe3+、SO42-时,可以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,
故答案为:BaCl2、NaOH、Na2CO3(或NaOH、BaCl2、Na2CO3或BaCl2、Na2CO3、NaOH);
②检验滤液中是否存在SO42-的方法是:取少量滤液于试管中,滴入BaCl2溶液,若未出现浑浊现象,则滤液中不存在SO42-,
故答案为:取少量滤液于试管中,滴入BaCl2溶液,若未出现浑浊现象,则滤液中不存在SO42-;
③可用75%乙醇冲洗固体表面的氯化钾,这样可以减少晶体的损失,
故答案为:75%乙醇;
(2)Ⅰ.用氯化钠固体配制一定物质的量浓度的溶液,通常的步骤为:计算、称量、溶解、移液、洗涤、定容、摇匀等操作,所以实验操作步骤的正确顺序是①③⑤②④⑥,
故答案为:①③⑤②④⑥;
Ⅱ.根据这些操作可知所用的仪器除药匙、托盘天平、烧杯、胶头滴管、玻璃棒外还有500 mL容量瓶,
故答案为:500 mL容量瓶;
Ⅲ.在计算溶质的质量时要按容量瓶的规格计算,所以配制480mL 1.00mol•L-1 NaCl溶液,需要氯化钠的质量为0.5L×1.00mol•L-1×58.5g/mol=29.3g,
故答案为:29.3;
Ⅳ.A、用天平称物品时,物品在左边,砝码在右边,故A错误;
B、溶解时要用玻璃棒搅拌,故B正确;
C、向容量瓶中加液体时要用玻璃棒引流,故C错误;
D、定容时,滴管不能伸到容量瓶中,故D错误,
故选B;
Ⅴ.实验过程中,若定容时俯视液面,则所配制溶液的体积偏小,会使溶液浓度偏高,
故答案为:偏高.
点评 本题主要考查了粗盐提纯过程中的除杂方面的知识,综合性强,难度一般,要注意除杂质选取和添加的先后顺序.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:解答题
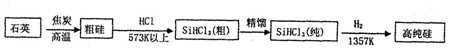
| N2H4 | N2O4 | |
| 密度/g/cm3 | 1.004 | 1.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子直径在1~100nm之间 | B. | 胶体粒子带电荷 | ||
| C. | 胶体粒子能穿过滤纸 | D. | 胶体粒子能够发生布朗运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
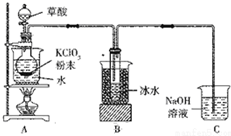 二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如图所示:
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在.| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
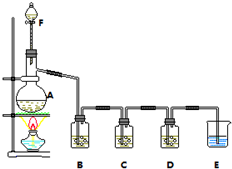 某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com