
为了除去氯化钾中含有的少量硫酸镁和氯化钙杂质,需进行下列六项操作,先后次序正确的是:①加水溶解 ②加热蒸发得到晶体 ③加入过量的氯化钡溶液 ④加入适量的盐酸 ⑤加入过量碳酸钾和氢氧化钾 ⑥过滤
A.①④③⑤⑥② B.①⑤③④⑥② C.①③④⑥⑤② D.①③⑤⑥④②
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届陕西省高三上学期12月月考化学试卷(解析版) 题型:填空题
碱式氧化镍(NiOOH)可用作镍氢电池的正极材料。以含镍(Ni2+)废液为原料生产NiOOH的一种工艺流程如下:

(1)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是______________________________,过滤时需用到的玻璃仪器有烧杯、_______________________。
(2)写出碳酸镍与稀硫酸反应的离子方程式:_____________________。
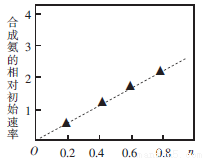
(3)硫酸镍溶液可用于制备合成氨的催化剂ConNi(1-n) Fe2 O4。如图表示在其他条件相同时合成氨的相对初始速率随催化 剂中n值变化的曲线,由图分析可知Co2+、 Ni2+两种离子中催化效果更好的是_________。
(4)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源:2016届北京西城(南区)重点中学高三第一学期课堂综合练习化学试卷(解析版) 题型:选择题
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2- )在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是
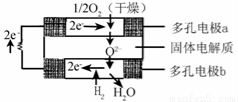
A.有O2参加反应的a极为电池的负极
B.有H2参加反应的b极为电池的正极
C.a极对应的电极反应式为O2 + 2H2O -4e = 4OH-
D.该电池的总反应方程式为:2H2+O2 = 2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省盐城市高一上学期期中考试化学试卷(解析版) 题型:选择题
将白醋、食用油、食盐、酒精分别放入水中,不能形成溶液的是
A.白醋 B.食用油
C.食盐 D.酒精
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃西北师大附属中学高一上期中化学试卷(解析版) 题型:选择题
取一小块金属钠放在燃烧匙里加热,下列实验现象:
①金属先熔化 ②在空气中燃烧,放出黄色火花 ③燃烧后得白色固体 ④燃烧时火焰为黄色
⑤燃烧后生成浅黄色固体物质。描述正确的是
A. ①② B.①②③ C.①④⑤ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第二次月考化学试卷(解析版) 题型:填空题
以下是25℃时几种难溶电解质的溶解度:
难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些杂质离子。例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。
请回答下列问题:
(1)上述三种除杂方案都能够达到很好的效果,Fe2+、Fe3+都被转化为_______(填化学式)而除去。
(2)①中加入的试剂应该选择_________为宜,其原因是_____________。
(3)②中除去Fe3+所发生的离子方程式为__________________________。
(4)下列与方案③相关的叙述中,正确的是__________________(填字母,多选不得分,少选得1分)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上第二次月考化学试卷(解析版) 题型:填空题
现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡________移动(填“向左”、“向右”或“不”);另取10 mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 的比值将________(填“增大”、“减小”或“无法确定”)。
的比值将________(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)________pH(乙)(填“大于”、“小于”或“等于”,下同)。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为:V(甲)________V(乙)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第二次月考化学试卷(解析版) 题型:选择题
两气体A和B的摩尔质量之比为3:1,则它们在同温、同压、同体积时的分子个数比应为
A、1:1 B、1:3 C、3:1 D、9:1
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期第二次诊断测试化学试卷(解析版) 题型:选择题
向稀硫酸中加入铜粉不发生反应,若再加入某种盐,则铜粉可以逐渐溶解,该盐是
A.KNO3 B. ZnSO4 C. KCl D.FeSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com