
2SO2£Øg£©+O2£Øg£©=2SO3£Øg£©·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾”£ŅŃÖŖ1mol SO2£Øg£©Ńõ»ÆĪŖ1mol SO3£Øg£©µÄ¦¤H= ”Ŗ99kJ”¤mol-1”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
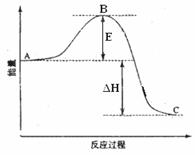
£Ø1£©Ķ¼ÖŠA±ķŹ¾ £¬EµÄ“󊔶ŌøĆ·“Ó¦µÄ·“Ó¦ČČ £ØĢī”°ÓŠ”±»ņ”°ĪŽ”±£©Ó°Ļģ”£øĆ·“Ó¦Ķس£ÓĆV2O5×÷“߻ƼĮ£¬¼ÓV2O5»įŹ¹Ķ¼ÖŠBµć £ØĢī”°Éżøß”±»¹ŹĒ”°½µµĶ”±£©£¬”÷H £ØĢī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±£©£¬ĄķÓÉŹĒ ”£
£Ø2£©ŅŃÖŖµ„ÖŹĮņµÄČ¼ÉÕČČĪŖ296 KJ”¤mol-1£¬¼ĘĖćÓÉ S£Øs£©Éś³É3 molSO3£Øg£©µÄ”÷H£ØŅŖĒó¼ĘĖć¹ż³Ģ£©”£
S£Øs£©Éś³É3 molSO3£Øg£©µÄ”÷H£ØŅŖĒó¼ĘĖć¹ż³Ģ£©”£
£Ø1£©·“Ó¦Īļ×ÜÄÜĮ棻 Éś³ÉĪļ×ÜÄÜĮæ ĪŽ£» ½µµĶ£» ²»±ä£»ŅņĪŖ“߻ƼĮæÉŅŌ½µµĶ·“Ó¦µÄ»ī»ÆÄÜ£¬µ«²»ÄÜøı䷓ӦĪļµÄ×ÜÄÜĮæŗĶÉś³ÉĪļµÄ×ÜÄÜĮæÖ®²ī£¬¼“²»øı䷓ӦČČ”£
£Ø2£©£Ø3 ·Ö£©½ā£ŗøł¾ŻĢāŅāæÉŠ“³öĻĀĮŠĮ½øöČČ»Æѧ·½³ĢŹ½£ŗ
·Ö£©½ā£ŗøł¾ŻĢāŅāæÉŠ“³öĻĀĮŠĮ½øöČČ»Æѧ·½³ĢŹ½£ŗ
S£Øs£©+O2£Øg£© = SO2£Øg£© ”÷H1= ”Ŗ296 KJ”¤mol-1 ,
SO2£Øg£©+1/2O2£Øg£© =SO3£Øg£© ”÷H2= ”Ŗ99 KJ”¤mol-1
øł¾ŻøĒĖ¹¶ØĀÉµĆ£ŗ S£Øs£©+3/2O2£Øg£©=SO3£Øg£© ”÷H3= ”Ŗ395 KJ”¤mol-1
”÷H= 3”÷H3 = ”Ŗ1185 KJ”¤mol-1



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ±ź×¼×“æöĻĀ£¬ ÖŹĮæĪŖmµÄĘųĢåAÓėÖŹĮæĪŖnµÄĘųĢåB
ÖŹĮæĪŖmµÄĘųĢåAÓėÖŹĮæĪŖnµÄĘųĢåB µÄ·Ö×ÓŹżĻąĶ¬£¬ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ (””””)
µÄ·Ö×ÓŹżĻąĶ¬£¬ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ (””””)
A£®ĘųĢåAÓėĘųĢåBµÄĻą¶Ō·Ö×ÓÖŹĮæ±ČĪŖm”Ćn
B£®Ķ¬ÖŹĮæĘųĢåAÓėĘųĢåBµÄ·Ö×ÓøöŹż±ČĪŖn”Ćm
C£®Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬AĘųĢåÓėBĘųĢåµÄĆܶȱČĪŖn”Ćm
D£®ĻąĶ¬×“æöĻĀ£¬Ķ¬Ģå»żAĘųĢåÓėBĘųĢåµÄÖŹĮæ±ČĪŖm”Ćn
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠ»śĪļPAS-NaŹĒŅ»ÖÖÖĪĮĘ·Ī½įŗĖŅ©ĪļµÄÓŠŠ§³É·Ö£¬ÓŠ»śĪļGŹĒŅ»ÖÖŹ³ÓĆĻćĮĻ£¬ŅŌ¼×±½ĪŖŌĮĻŗĻ³ÉÕāĮ½ÖÖĪļÖŹµÄĀ·ĻßČēĻĀ£ŗ
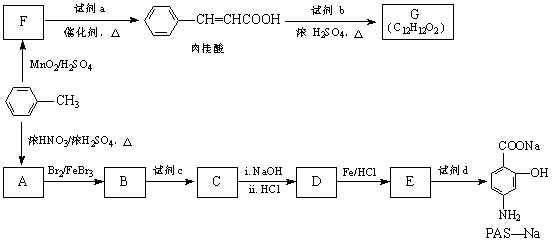

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©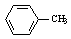 Éś³ÉAµÄ·“Ó¦ĄąŠĶŹĒ ”£
Éś³ÉAµÄ·“Ó¦ĄąŠĶŹĒ ”£
£Ø2£©FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒ £»ŹŌ¼ĮaµÄ½į¹¹¼ņŹ½ĪŖ ”£
£Ø3£©Š“³öÓÉAÉś³ÉBµÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø4£©ÖŹĘ×Ķ¼ĻŌŹ¾ŹŌ¼ĮbµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ58£¬·Ö×ÓÖŠ²»ŗ¬¼×»ł£¬ĒŅĪŖĮ“ד½į¹¹£¬Š“³öČā¹šĖįÓėŹŌ¼ĮbÉś³ÉGµÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø5£©µ±ŹŌ¼Įd¹żĮæŹ±£¬æÉŅŌŃ”ÓƵďŌ¼ĮdŹĒ £ØĢī×ÖÄøŠņŗÅ£©”£
a£®NaHCO3 b£®NaOH c£®Na2CO3
£Ø6£©Š“³öCÓėNaOH·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
£Ø7£©Čā¹šĖįÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬·ūŗĻĻĀĮŠĢõ¼žµÄÓŠ ÖÖ”£
a£®±½»·ÉĻÓŠČżøöČ”“ś»ł£»
b£®ÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ĒŅ1 moløĆÓŠ»śĪļ×ī¶ąÉś³É4 mol Ag”£
ÓÉÉĻŹö·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÖŠ£¬Š“³ö±½»·ÉĻÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³ĒāŌ×ÓµÄÓŠ»śĪļµÄ½į¹¹¼ņŹ½£ØČĪŠ“Ņ»ÖÖ¼“æÉ£© ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ģå»żĻąĶ¬”¢pHĻąĶ¬µÄHClČÜŅŗŗĶCH3COOHČÜŅŗ£¬ÓėNaOHČÜŅŗÖŠŗĶŹ±Į½ÕßĻūŗĵÄNaOHµÄĪļÖŹµÄĮæ
A£®ÖŠŗĶCH3COOHµÄ¶ą B£®ÖŠŗĶHClµÄ¶ą
C£®ĻąĶ¬ D£®ĪŽ·Ø±Č½Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«4 mol AĘųĢåŗĶ2 mol BĘųĢåŌŚ2 LµÄČŻĘ÷ÖŠ»ģŗĻ²¢ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗ2A£Øg£©+B£Øg£© 2C£Øg£©”£Čō¾2 sŗó²āµĆCµÄÅضČĪŖ0.6 mol”¤L-1£¬ĻÖÓŠĻĀĮŠ¼øÖÖĖµ·Ø£ŗ
2C£Øg£©”£Čō¾2 sŗó²āµĆCµÄÅضČĪŖ0.6 mol”¤L-1£¬ĻÖÓŠĻĀĮŠ¼øÖÖĖµ·Ø£ŗ
A£®ÓĆĪļÖŹA±ķŹ¾µÄ·“Ó¦Ę½¾łĖŁĀŹĪŖ0.3 mol”¤L-1”¤s-1
B£®ÓĆĪļÖŹB±ķŹ¾µÄ·“Ó¦µÄĘ½¾łĖŁĀŹĪŖ0.6 mol”¤L-1”¤s-1
C£®2 sŹ±ĪļÖŹAµÄ×Ŗ»ÆĀŹĪŖ70%
D£®2 sŹ±ĪļÖŹBµÄÅضČĪŖ0.7 mol”¤L-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪļÖŹµÄĮæÅضČĻąĶ¬µÄĻĀĮŠČÜŅŗÖŠ£¬ŗ¬Į£×ÓÖÖĄą×ī¶ąµÄŹĒ( ””)
A. K2CO3 B.CH3COONa
C.NH4Cl D. CaCl2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻąĶ¬ĪĀ¶ČĻĀ£¬100 mL 0.01 mol”¤L£1µÄ“×ĖįČÜŅŗÓė10 mL 0.1 mol”¤L£1µÄ“×ĖįČÜŅŗĻą±Č½Ļ£¬ĻĀĮŠŹżÖµĒ°Õß“óÓŚŗóÕߵďĒ( )
A£®c(OH£) B£®c(H£«) C£®ÖŠŗĶŹ±ĖłŠčNaOHµÄĮæ D£®c(CH3COOH)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬Č”0.2 mol”¤L£1 HClČÜŅŗÓė0.2 mol”¤L£1 MOHČÜŅŗµČĢå»ż»ģŗĻ(ŗöĀŌ»ģŗĻŗóČÜŅŗĢå»żµÄ±ä»Æ)£¬²āµĆ»ģŗĻČÜŅŗµÄpH£½6£¬ŹŌ»Ų“šŅŌĻĀĪŹĢā£ŗ
(1)»ģŗĻČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc (H£«) 0.2 mol”¤L£1 HClČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc (H£«) (Ģī”°£¾”¢£¼»ņ=”±)”£
(2)Ēó³ö»ģŗĻĪļÖŠĻĀĮŠĖćŹ½µÄ¾«Č·¼ĘĖć½į¹ū(Ģī¾ßĢåŹż×Ö)£ŗ
c (Cl£) − c (M£«)£½ ”” ””mol”¤L£1£¬c (H£«) − c (MOH) £½ ”” ””mol”¤L£1 ”£
(3)Čō³£ĪĀĻĀČ”0.2 mol”¤L£1 MOHČÜŅŗÓė0.1 mol”¤L£1 HClČÜŅŗµČĢå»ż»ģŗĻ£¬²āµĆ»ģŗĻČÜŅŗµÄpH£¼7£¬ĖµĆ÷MOHµÄµēĄė³Ģ¶Č”” ””(Ģī”°£¾”¢£¼»ņ=”±)MClµÄĖ®½ā³Ģ¶Č”£ČÜŅŗÖŠø÷Ąė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ ”””” ”£
(4)Čō³£ĪĀĻĀpH£½3µÄŃĪĖįÓėpH£½11µÄ°±Ė®ČÜŅŗµČĢå»ż»ģŗĻ£¬Ōņ»ģŗĻČÜŅŗµÄpH”” ””7(Ģī”°£¾”¢£¼»ņ=”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¶ŌĻąĶ¬×“æöĻĀµÄ12C18OŗĶ14N2Į½ÖÖĘųĢå,ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
(””””)
A.ČōÖŹĮæĻąµČ,ŌņÖŹ×ÓŹżĻąµČ
B.ČōŌ×ÓŹżĻąµČ,ŌņÖŠ×ÓŹżĻąµČ
C.Čō·Ö×ÓŹżĻąµČ,ŌņĢå»żĻąµČ
D.ČōĢå»żĻąµČ,ŌņĆܶČĻąµČ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com