
| A.通入Cl2 | B.加入Zn | C.加入Fe | D.加入Cu |
科目:高中化学 来源:不详 题型:填空题
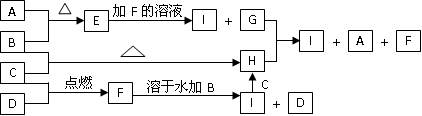
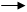 (4)写出G+H I+A+F的离子方程式_______________________________。
(4)写出G+H I+A+F的离子方程式_______________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
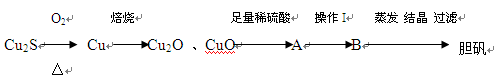
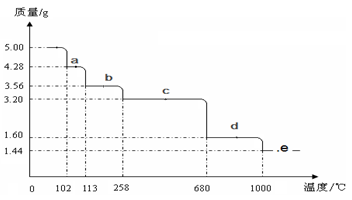
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeO | B.Fe2O3 | C.CuO | D.Cu2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
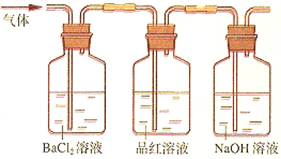
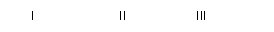
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
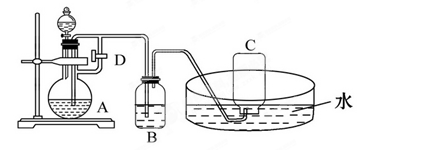
 应预先加入的试剂是________,A中反应的离子方程式为____________________________________________________。
应预先加入的试剂是________,A中反应的离子方程式为____________________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
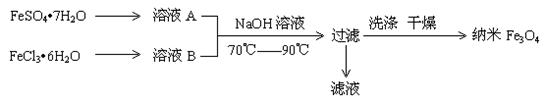
 O 和 FeCl3·6H2O的物质的量之比最好应为 ,在此条件下,检验铁元素是否沉淀完全的实验操作是 。
O 和 FeCl3·6H2O的物质的量之比最好应为 ,在此条件下,检验铁元素是否沉淀完全的实验操作是 。| A.纳米Fe3O4磁硫体分散系属于溶液。 |
B.纳米Fe3O4磁硫体可 以通过渗析法得到提纯。 以通过渗析法得到提纯。 |
| C.当一束可见光通过该磁硫体时会出现光亮的通路。 |
| D.纳米Fe3O4磁硫体比较稳定。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com