
����Ŀ��ij�¶�ʱ����һ���ݻ�Ϊ3L���ܱ������У�A��B��C������̬���ʵ����ʵ�����ʱ��仯������ͼ��ʾ����ش��������⣺
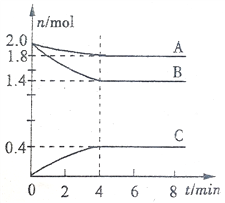
��1���÷�Ӧ�Ļ�ѧ����ʽ��_________________________________��
��2����Ӧ�ӿ�ʼ��ƽ��ʱ������B��ƽ����Ӧ������___________________��
��3���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��______________________________��
��4�������������䣬�����¶ȣ��淴Ӧ���ʽ�____________�������ӿ���������������������������
��5����Ӧ��ƽ��������������䣬�������������ƽ�⽫__________�����������ƶ������������ƶ����������ƶ�������
���𰸡� ��1��A��g��+3B��g��![]() 2C��g�� 0.05mol/(L��min) K=c2��C��/c��A����c3��B�� �ӿ� �����ƶ�
2C��g�� 0.05mol/(L��min) K=c2��C��/c��A����c3��B�� �ӿ� �����ƶ�
��������������������⿼��ͼ��ķ�������ѧ��Ӧ���ʵļ��㣬��ѧƽ�ⳣ������ʽ����д����������Ի�ѧ��Ӧ���ʺͻ�ѧƽ���Ӱ�졣
��1������ʱ������ƣ�A��B���ʵ�����С��C���ʵ��������࣬��A��BΪ��Ӧ�CΪ�������0~4min����A��B��C���ʵ����ĸı�ֵ����Ϊ��2.0mol-1.8mol������2.0mol-1.4mol������0.4mol-0������A��B��C�Ļ�ѧ����������Ϊ1��3��2��4min����������ʵ������ٸı䣬�����ﵽ��ƽ��״̬���÷�ӦΪ���淴Ӧ����Ӧ�Ļ�ѧ����ʽΪA��g��+3B��g��![]() 2C��g����
2C��g����
��2������B��=![]() =
=![]() =0.05mol/(L��min)��
=0.05mol/(L��min)��
��3�����ݷ�Ӧ����ʽд����ѧƽ�ⳣ���ı���ʽK=![]() ��
��
��4�������������䣬�����¶ȣ��淴Ӧ���ʽ��ӿ���
��5���÷�Ӧ������ӦΪ�����������С�ķ�Ӧ����Ӧ��ƽ��������������䣬�����������������Сѹǿ��ƽ�⽫�����ƶ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeS��һ��Ũ�ȵ�HNO3��Ӧ������Fe(NO3)3��Fe2(SO4)3��NO2��N2O4��NO��H2O����NO2��N2O4��NO�����ʵ���֮��Ϊ4��1��4ʱ��ʵ�ʲμӷ�Ӧ��������ʵ���֮��Ϊ( )
A. 1��6 B. 2��15 C. 2��3 D. 16��25
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaOH���������������
A.�������ֻ�ѧ��B.�����ۼ������ӻ�����
C.������������D.�����ۼ��Ĺ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ��ó���ʯ��ˮ����CO2 �� ��֪��20��ʱ��ÿ100gˮ�ܽ�Ca��OH��20.165g���ﵽ���ͣ�
��1����20��500gˮ�м���37.0g Ca��OH��2��ĩ������ֽ��裬��Һ�������Ϊ500mL����OH�����ӵ����ʵ���Ũ�ȣ�
��2����ʹԭ500mL��Һ�е�c��Ca2+��������0.01mol/L������Ҫͨ���״���¶�����̼�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѡ���ڱ�״���£�m g����A��n g����B�ķ�������ͬ������˵���в���ȷ���ǣ� ��
A.��������A��B����Է�������֮��Ϊm��n
B.ͬ��������A��B�ķ�����֮��Ϊm��n
C.ͬ��ͬѹ�£�A��B��������ܶ�֮��Ϊn��m
D.��ͬ״���£�ͬ���A��B�����������֮��Ϊm��n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����еķ��뷽������ȷ����( )��
A���þƾ���ȡ��ˮ�еĵ�
B��������ķ���������ˮ�Ƴ�����ˮ
C���ù��˵ķ�����ȥʳ��ˮ�е���ɳ
D������ϴ�ķ�����ɳ���Խ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�l mol X��n mol Y�����Ϊ2L���ܱ������з������·�Ӧ��X(g) + Y(g)![]() 2Z(g) + M(s)��5min��ﵽƽ�⣬��ʱ����2a mol Z������˵����ȷ����
2Z(g) + M(s)��5min��ﵽƽ�⣬��ʱ����2a mol Z������˵����ȷ����
A. ��X��ʾ5min�ڴ˷�Ӧ�ķ�Ӧ�����ǣ�0.1��0.2a��mol��(L��min)��1
B. �����������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬
C. ��ƽ������ϵ�м���l mol M��ƽ�����淴Ӧ�����ƶ�
D. ������ƽ����ϵ���ٳ���l mol X��v(��)����v(��)��С��ƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ����Ҫ100mL��0.1mol/L��Na2CO3��Һ��
��1����ͨ�����²������ƣ�
�ٰѳ����õĹ���Na2CO3����С�ձ��У�����������ˮ�ܽ⣮Ϊ�ӿ��ܽ����ʹ�������������ƣ����裻�ڰѢ�������Һ��ȴ�����º�С��ת�������������ƣ����ۼ���������ˮ��Һ���̶���1��2cm�������������������ƣ�С�ĵμ�����ˮ����Һ��Һ����͵���̶������У�������������ˮϴ�Ӳ��������ձ�2��3�Σ�ÿ��ϴ�ӵ���Һ��С��ת������ƿ��������ҡ�ȣ��ݽ�����ƿ���������ҡ�ȣ�
��2������������ȷ��˳����������ţ���
��3����û�в����ܣ���������Һ��Ũ�Ȼ����ƫ�ߡ���ƫ�͡�����
��4����ȡ��20mL��õ�Na2CO3��Һ��������ˮϡ�ͳ�c��Na+��=0.01mol/L����Һ����ϡ�ͺ���Һ�����ΪmL��
��5��������100mL 0.1mol/L��Na2CO3��Һʱ�����в����е��ᵼ�½��ƫ�ͣ����������д����
����������ƽ����ʱ����������� �ڽ��ձ��е���Һת�Ƶ�����ƿʱ������������ƿ�� �۶���ʱ���ӿ̶��� �ܶ���ʱ���ӿ̶��� �ݸɾ�������ƿδ�����������������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���к͵ζ�������֪Ũ�ȵ�ϡ����ζ�δ֪Ũ�ȵ�ϡ��ˮ������ʽ��ζ�����������Һ���ƣ�c1V1=c2V2���� ��
A.�յ���Һƫ����
B.�յ���Һ��c(NH4+)=c(Cl-)
C.�յ���Һ�а�����
D.���ʵ�ָʾ���Ǽ��ȶ��Ƿ�̪
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com