
| A. | ①②③ | B. | ②③④⑥ | C. | ③④⑤⑥ | D. | ⑤⑥ |
分析 ①能量高的电子也可以在s轨道上运动;
②电子质量很小且带负电荷;
③电子在原子核周围很小的空间里运动;
④电子在原子核周围高速运动;
⑤电子没有固定的运动轨道;
⑥电子的质量约为质子质量的$\frac{1}{1836}$.
解答 解:①能量高的电子也可以在s轨道上运动,如7s轨道上的电子能量也很高,比4f能量还高,故①错误;
②电子质量为9.3×10-31Kg,所以电子的质量很小,电子带一个单位的负电荷,故②正确;
③电子在原子核周围很小的空间里运动,所以电子运动的空间范围很小,故③正确;
④电子在原子核周围高速运动,故④正确;
⑤电子没有固定的运动轨道,故⑤错误;
⑥电子的质量约为质子质量的$\frac{1}{1836}$,氢离子质量等于质子的质量,故⑥正确;
所以正确的有②③④⑥,
故选:B.
点评 本题考查了核外电子的有关知识,注意电子的特点及原子结构,题目难度不大.


科目:高中化学 来源: 题型:解答题
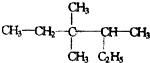 3,3,4-三甲基己烷
3,3,4-三甲基己烷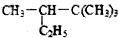 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷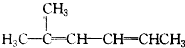 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯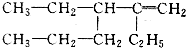 2,3-二乙基-1-己烯.
2,3-二乙基-1-己烯.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
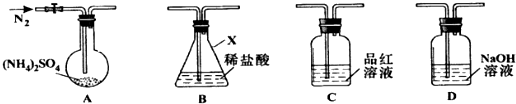
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥ | B. | ①②③⑤ | C. | ①②⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
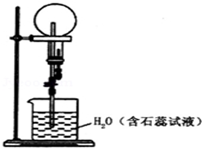 已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法正确的是( )
已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法正确的是( )| A. | NH3和HCl分别形成红色、蓝色喷泉 | |
| B. | 制备干燥的NH3和HCl,可分别用无水CaCl2、碱石灰干燥 | |
| C. | 改为NO2气体,所得溶液溶质的物质的量浓度与前两者不同 | |
| D. | 去掉装置中的胶头滴管,改为单孔塞,也可引发喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ③④⑤ | C. | ③⑤ | D. | ②⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com