
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应:
A(g)  B(g)+C(g) ΔH=+85.1 kJ·mol-1。
B(g)+C(g) ΔH=+85.1 kJ·mol-1。
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/ 100 kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为_______________________________________
________________________________________________________________________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为____________,平衡时A的转化率为________ ,列式并计算反应的平衡常数K______________ ______。
______。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=________mol,n(A)=________mol。
②下表为反应物A的浓度与反应时间的数据,计算:a=________。
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.006 5 |
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是
________________________________________________________________________,
由此规律推出反应在12 h时反应物的浓度c(A)为________mol·L-1。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
向含有10.26g金属M氢氧化物的澄清溶液中,加入NaHCO3和Na2CO3•xH2O固体混合物6.70g,充分反应后过滤,所得滤液为NaOH溶液,将其稀释至200mL,测得Na+的物质的量浓度为0.35mol/L;再将所得沉淀MCO3溶于足量的稀盐酸中,收集到气体2.64g。
请回答下列问题:
(1)通过计算确定M的元素符号。
(2)通过计算确定x的值。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 目的 | 分离方法 | 原理 |
| A. | CO2中混有的少量CO | 通入适量O2点燃 | CO会燃烧成CO2 |
| B. | 除去鸡蛋清胶体中混有的NaCl | 过滤 | 鸡蛋清胶体不能通过滤纸 |
| C. | 除去NaHCO3固体中混有的Na2CO3 | 加热 | NaHCO3受热分解 |
| D. | 除去BaSO4粉末中混有的BaCO3 | 盐酸溶解后过滤、洗涤 | 盐酸可溶解BaCO3,不溶解BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。下列判断正确的是( )
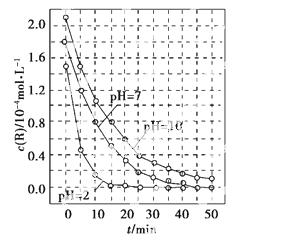
A.在0~50 min之间,pH=2和pH=7时R的降解百分率相等
B.溶液酸性越强,R的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在20~25 min之间,pH=10时R的平均降解速率为0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如图所示。据图分析,下列判断不正确的是( )
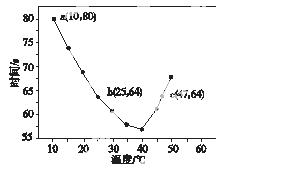
A.40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中b、c两点对应的NaHSO3反应速率相等
C.图中a点对应的NaHSO3反应速率为5.0×10-5 mol·L-1·s-1
D.温度高于40 ℃时,淀粉不宜用作该实 验的指示剂
验的指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)  2C
2C (g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
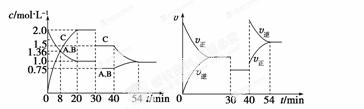
下列说法中正确的是  ( )
( )
A.30~40 min间该反应使用了催化剂
B.反应方程式中的x=1,正反应为吸热反应
C.30 min时降低温度,40 min时升高温度
D.8 min前A的平均反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
根据酸碱的质子理论,“凡是能给出质子的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒:
①HS-,②CO32-,③HPO42-,④NH3,⑤OH-,⑥H2O,⑦HCO3-,⑧HAc,⑨KHSO4
(1)只属于碱的微粒是: ;
(2)只属于酸的微粒是: ;
(3)属于两性的微粒是: 。(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
图中a、b是惰性电极,通电2 min后b电极附近溶液呈红色,b电极生成标准状况时的气体体积为0.224 L,NaCl溶液体积为500 mL,下列说法不正确的是( )

A.电解过程中 CuSO4溶液物质的量浓度不变
CuSO4溶液物质的量浓度不变
B.电子流动的方向是由a流向Cu电极
C.电路中通过的电子为0.02 mol
D.电解速率v(OH-)=0.02 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应:N2(g)+3H2 (g) 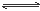 2NH3(g)的正、逆反应速度可用各反应物或生成物浓度变化来表示。下列各关系中能说明反应已经达到化学平衡的是 ( )
2NH3(g)的正、逆反应速度可用各反应物或生成物浓度变化来表示。下列各关系中能说明反应已经达到化学平衡的是 ( )
A.3v正(N2)=v逆(H2)
B.v正(N2)=v逆(NH3)
C.2v正(H2)=3v正(NH3)
D.v正(N2)=3v逆(H2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com