
ΓΨΧβΡΩΓΩΗΏ¥ΩΝρΥαΟΧΉςΈΣΚœ≥…ΡχνήΟΧ»ΐ‘Σ’ΐΦΪ≤ΡΝœΒΡ‘≠ΝœΘ§ΙΛ“Β…œΩ…”…Χλ»ΜΕΰ―θΜ·ΟΧΖέ”κΝρΜ·ΟΧΩσΘ®ΜΙΚ§FeΓΔAlΓΔMgΓΔZnΓΔNiΓΔSiΒ»‘ΣΥΊΘ©÷Τ±ΗΘ§ΙΛ“’»γΆΦΥυ ΨΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
œύΙΊΫπ τάκΉ”[c0(Mn+)=0.1molΓΛL-1]–Έ≥…«β―θΜ·Έο≥ΝΒμ![]() pHΖΕΈß»γœ¬ΘΚ
pHΖΕΈß»γœ¬ΘΚ
Ϋπ τάκΉ” | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
ΩΣ Φ≥ΝΒμΒΡpH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
≥ΝΒμΆξ»ΪΒΡpH | 10.1 | 8 3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
Θ®1Θ©–¥≥ωΜυΧ§ΟΧ‘≠Ή”ΚΥΆβΒγΉ”≈≈≤Φ Ϋ___ΓΘ
Θ®2Θ©ΓΑ―θΜ·Γ±÷–ΧμΦ” ΝΩΒΡMnO2ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ «___ΓΘ
Θ®3Θ©ΓΑΒςpHΓ±≥ΐΧζΚΆ¬ΝΘ§»ή“ΚΒΡpHΖΕΈß”ΠΒςΫΎΈΣ___~6÷°ΦδΓΘ
Θ®4Θ©ΓΑ≥ΐ‘”2Γ±ΒΡΡΩΒΡ «…ζ≥…MgF2≥ΝΒμ≥ΐ»ΞMg2+ΓΘ»τ»ή“ΚΥαΕ»ΙΐΗΏΘ§Mg2+≥ΝΒμ≤ΜΆξ»ΪΘ§‘≠“ρ «___ΓΘ
Θ®5Θ©–¥≥ωΓΑ≥ΝΟΧΓ±ΒΡάκΉ”ΖΫ≥Χ Ϋ___ΓΘ
Θ®6Θ©≤ψΉ¥ΡχνήΟΧ»ΐ‘Σ≤ΡΝœΩ…ΉςΈΣο°άκΉ”Βγ≥Ί’ΐΦΪ≤ΡΝœΘ§ΤδΜ·―ß ΫΈΣLiNixCoyMnzO2Θ§Τδ÷–NiΓΔCoΓΔMnΒΡΜ·ΚœΦέΖ÷±πΈΣ+2ΓΔ+3ΓΔ+4ΓΘΒ±x=y=![]() ±Θ§z=___ΓΘ
±Θ§z=___ΓΘ
ΓΨ¥πΑΗΓΩ[Ar]3d54s2 2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O 4.7 F”κH+ΫαΚœ–Έ≥…»θΒγΫβ÷ HFΘ§MgF2(s)Mg2+(aq)+2F(aq)»ήΫβΤΫΚβœρ”““ΤΕ· Mn2++2HCO3-=MnCO3Γΐ+CO2Γϋ+H2O ![]()
ΓΨΫβΈωΓΩ
ΝρΜ·ΟΧΩσ(ΜΙΚ§FeΓΔAlΓΔMgΓΔZnΓΔNiΓΔSiΒ»‘ΣΥΊ)ΚΆMnO2ΖέΦ”»κœΓΝρΥαΘ§Εΰ―θΜ·ΟΧΖέΚΆΝρΜ·ΟΧΩσ…ζ≥…MnSO4ΓΔSΘ§Ά§ ±»ή“Κ÷–ΜΙ”–Ρ―»ή–‘ΒΡSiO2ΦΑΡ―»ή–‘ΒΡΙηΥα―ΈΘ§Υυ“‘ΒΟΒΫΒΡ¬Υ‘ϋ1ΈΣSiO2ΚΆSΚΆΡ―»ή–‘ΒΡΙηΥα―ΈΘΜ»ΜΚσœρ¬Υ“Κ÷–Φ”»κMnO2Θ§MnO2―θΜ·ΜΙ‘≠–‘άκΉ”Fe2+…ζ≥…Fe3+Θ§‘Όœρ»ή“Κ÷–Ά®»κΑ±ΤχΒςΫΎ»ή“ΚΒΡpH≥ΐΧζΚΆ¬ΝΘ§Υυ“‘¬Υ‘ϋ2ΈΣFe(OH)3ΓΔAl(OH)3Θ§ΓΑ≥ΐ‘”1Γ±ΒΡΡΩΒΡ «≥ΐ»ΞZn2+ΚΆNi2+Θ§Φ”»κΒΡNa2SΚΆZn2+ΓΔNi2+Ζ¥”Π…ζ≥…ΝρΜ·Έο≥ΝΒμΘ§Υυ“‘¬Υ‘ϋ3ΈΣNiSΚΆZnSΘ§ΓΑ≥ΐ‘”2Γ±ΒΡΡΩΒΡ «…ζ≥…MgF2≥ΝΒμ≥ΐ»ΞMg2+Θ§Υυ“‘¬Υ‘ϋ4ΈΣMgF2Θ§ΉνΚσœρ¬Υ“Κ÷–Φ”»κΧΦΥα«βοßΒΟΒΫMnCO3≥ΝΒμΘ§”ΟœΓΝρΥα»ήΫβ≥ΝΒμΒΟΒΫΝρΥαΟΧΘ§”…¥ΥΖ÷ΈωΓΘ
(1)ΟΧΒΡ‘≠Ή”–ρ ΐΈΣ27Θ§ΗυΨίΚΥΆβΒγΉ”≈≈≤Φ ΫΘ§ΜυΧ§ΟΧ‘≠Ή”ΚΥΆβΒγΉ”≈≈≤Φ Ϋ[Ar]3d54s2ΘΜ
(2)MnO2―θΜ·ΜΙ‘≠–‘άκΉ”Fe2+…ζ≥…Fe3+ Θ§ΓΑ―θΜ·Γ±÷–ΧμΦ” ΝΩΒΡMnO2ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ2Fe2++MnO2+4H+=2Fe3++Mn2++2H2OΘΜ
(3)ΓΑΒςpHΓ±≥ΐΧζΚΆ¬ΝΘ§»ή“ΚΒΡpH”ΠΗΟ¥σ”Ύ’βΝΫ÷÷άκΉ”Άξ»Ϊ≥ΝΒμΥυ–ηpH«“–Γ”ΎΤδΥϋάκΉ”…ζ≥…≥ΝΒμΒΡpH÷ΒΘ§‘ΎpH=4.7 ±Fe3+ΚΆAl3+≥ΝΒμΆξ»ΪΘ§‘ΎpH=6.2 ±Zn2+ΩΣ Φ≤ζ…ζ≥ΝΒμΘ§»ή“ΚΒΡpHΖΕΈßΈΣ4.7ΓΪ6÷°ΦδΘΜ
(4)ΓΑ≥ΐ‘”2Γ±ΒΡΡΩΒΡ «…ζ≥…MgF2≥ΝΒμ≥ΐ»ΞMg2+Θ§»ή“Κ÷–¥φ‘ΎMgF2ΒΡ»ήΫβΤΫΚβΘ§»γΙϊ»ή“ΚΥα–‘Ϋœ«ΩΘ§…ζ≥…»θΒγΫβ÷ HFΕχ¥ΌΫχΖζΜ·ΟΨ»ήΫβΘ§Φ¥F-”κH+ΫαΚœ–Έ≥…»θΒγΫβ÷ HFΘ§MgF2(s)Mg2+(aq)+2F(aq)»ήΫβΤΫΚβœρ”““ΤΕ·Θ§Υυ“‘ΟΨάκΉ”≥ΝΒμ≤ΜΆξ»ΪΘΜ
(5)ΓΑ≥ΝΟΧΓ± ±ΟΧάκΉ”ΚΆΧΦΥα«βΗυάκΉ”Ζ¥”Π…ζ≥…ΧΦΥαΟΧ≥ΝΒμΘ§Ά§ ±ΜΙ…ζ≥…Υ°ΓΔΕΰ―θΜ·ΧΦΘ§άκΉ”ΖΫ≥Χ ΫΈΣΘΚMn2++2HCO3-=MnCO3Γΐ+CO2Γϋ+H2OΘΜ
(7)≤ψΉ¥ΡχνήΟΧ»ΐ‘Σ≤ΡΝœΩ…ΉςΈΣο°άκΉ”Βγ≥Ί’ΐΦΪ≤ΡΝœΘ§ΤδΜ·―ß ΫΈΣLiNixCoyMnzO2Θ§Τδ÷–NiΓΔCoΓΔMnΒΡΜ·ΚœΦέΖ÷±πΈΣ+2ΓΔ+3ΓΔ+4Θ°Β±x=y=![]() Θ§ΗυΨίΜ·ΚœΦέΒΡ¥ζ ΐΚΆΈΣ0Θ§z=
Θ§ΗυΨίΜ·ΚœΦέΒΡ¥ζ ΐΚΆΈΣ0Θ§z=![]() ΓΘ
ΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΆ§―ßΟ«“―Ψ≠―ßœΑΝΥΆ§ΈΜΥΊΓΔΆ§œΒΈοΓΔΆ§ΥΊ“λ–ΈΧεΓΔΆ§Ζ÷“λΙΙΧεΘ§ΡψΡή«χ±π’β–©Η≈Ρν¬πΘΩœ¬ΟφΝ–≥ωΝΥΦΗΉιΈο÷ Θ§«κΫΪΈο÷ ΒΡΚœ ΉιΚ≈Χν–¥‘Ύœ¬±μ÷–ΓΘ
ΔΌ![]() ΚΆ
ΚΆ![]()
ΔΎ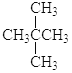 ΚΆ
ΚΆ![]()
ΔέCH4ΚΆCH3CH2CH3ΘΜΔήΫπΗ’ ·”κ ·ΡΪΘΜΔίκ≠ΓΔκ°”κκΑΘΜΔό16OΓΔ17OΚΆ18OΘΜΔΏ““¥Φ(CH3CH2OH)ΚΆΦΉΟ―(CH3OCH3)ΘΜΔύ―θΤχ(O2)”κ≥τ―θ(O3)ΓΘ
άύ±π | Ά§ΈΜΥΊ | Ά§œΒΈο | Ά§ΥΊ“λ–ΈΧε | Ά§Ζ÷“λΙΙΧε |
ΉιΚ≈ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣΘΚH2O(g)=H2O(l) ΠΛHΘΫQ1 kJΓΛmolΘ≠1
C2H5OH(g)=C2H5OH(l)ΠΛHΘΫQ2 kJΓΛmolΘ≠1
C2H5OH(g)ΘΪ3O2(g)=2CO2(g)ΘΪ3H2O(g)ΠΛHΘΫQ3 kJΓΛmolΘ≠1
»τ Ι46 g“ΚΧεΨΤΨΪΆξ»Ϊ»Φ…’Θ§ΉνΚσΜ÷Η¥ΒΫ “Έ¬Θ§‘ρΖ≈≥ωΒΡ»»ΝΩΈΣ
A. Θ≠(3Q1Θ≠Q2ΘΪQ3) kJB. Θ≠0.5(Q1ΘΪQ2ΘΪQ3) kJ
C. Θ≠(0.5Q1Θ≠1.5Q2ΘΪ0.5Q3) kJD. Θ≠(Q1ΘΪQ2ΘΪQ3) kJ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥ΈΔΝΘAΒΡΫαΙΙ Ψ“βΆΦΈΣ![]()
Θ®1Θ©»τA «‘≠Ή”Θ§‘ρAΒΡ‘ΣΥΊΖϊΚ≈ΈΣ__ΘΜ»τA «¥χ“ΜΗω’ΐΒγΚ…ΒΡ―τάκΉ”Θ§‘ρX=__ΓΘ
Θ®2Θ©»τX=8Θ§‘ρ¥Υ“θάκΉ””κΘ®1Θ©÷–¥χ“ΜΗω’ΐΒγΚ…ΒΡ―τάκΉ”–Έ≥…“Μ÷÷≥ΘΦϊΜ·ΚœΈοΒΡΜ·―ß Ϋ «__Θ§–¥≥ω¥ΥΜ·ΚœΈο”κ―ΈΥαΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ__ΓΘ
Θ®3Θ©1molΈΔΝΘAΚ§”–10molΒγΉ”Θ§œ¬Ν–ΈΔΝΘΗς1molΘ§“≤Κ§”–10molΒγΉ”ΒΡ”–ΘΚ__(Χν–ρΚ≈)ΓΘ
ΔΌCH4 ΔΎH2O2 ΔέHF ΔήAl3+ ΔίCl- ΔόNH4+
Θ®4Θ©»τAΒΡ―τάκΉ”ΈΣAn+«“÷ ΝΩ ΐΈΣaΘ§‘ρ÷–Ή” ΐΈΣ__(”ΟΚ§”–aΘ§nΒΡ¥ζ ΐ Ϋ±μ¥ο)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩIΘ°Ψί±®ΒάΘ§Έ“Ιζ‘ΎΡœΚΘ±±≤Ω…ώΚϋΚΘ”ρΫχ––ΒΡΩ…»Φ±υ(ΦΉΆιΒΡΥ°ΚœΈο) ‘≤…ΜώΒΟ≥…ΙΠΓΘΦΉΆι «“Μ÷÷÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΓΘ
Θ®1Θ©ΦΉΆι÷Ί’ϊ «ΧαΗΏΦΉΆιάϊ”Ο¬ ΒΡ÷Ί“ΣΖΫ ΫΘ§≥ΐ≤ΩΖ÷―θΜ·ΆβΜΙ”–“‘œ¬ΝΫ÷÷ΘΚ
Υ°’τΤχ÷Ί’ϊΘΚCH4(g)ΘΪH2O(g) ![]() CO(g)ΘΪ3H2(g)ΓΓΠΛH1ΘΫΘΪ205.9 kJΓΛmolΘ≠1ΓΓ ΔΌ
CO(g)ΘΪ3H2(g)ΓΓΠΛH1ΘΫΘΪ205.9 kJΓΛmolΘ≠1ΓΓ ΔΌ
CO(g)ΘΪH2O(g) ![]() CO2(g)ΘΪH2(g)ΓΓΠΛH2ΘΫΘ≠41.2 kJΓΛmolΘ≠1ΓΓΔΎ
CO2(g)ΘΪH2(g)ΓΓΠΛH2ΘΫΘ≠41.2 kJΓΛmolΘ≠1ΓΓΔΎ
Εΰ―θΜ·ΧΦ÷Ί’ϊΘΚCH4(g)ΘΪCO2(g) ![]() 2CO(g)ΘΪ2H2(g)ΓΓΠΛH3ΓΓΔέ
2CO(g)ΘΪ2H2(g)ΓΓΠΛH3ΓΓΔέ
‘ρΖ¥”ΠΔΌΉ‘ΖΔΫχ––ΒΡΧθΦΰ «______________Θ§ΠΛH3ΘΫ________kJΓΛmolΘ≠1ΓΘ
Δρ.ΒΣΒΡΙΧΕ®“Μ÷± «ΩΤ―ßΦ“―–ΨΩΒΡ÷Ί“ΣΩΈΧβΘ§Κœ≥…Α±‘ρ «»ΥΙΛΙΧΒΣ±»Ϋœ≥… λΒΡΦΦ θΘ§Τδ‘≠άμΈΣN2 (g)ΘΪ3H2 (g) ![]() 2NH3(g)ΓΘ
2NH3(g)ΓΘ
Θ®2Θ©‘Ύ≤ΜΆ§Έ¬Ε»ΓΔ―Ι«ΩΚΆœύΆ§¥ΏΜ·ΦΝΧθΦΰœ¬Θ§≥θ ΦN2ΓΔH2 Ζ÷±πΈΣ0.1 molΓΔ0.3 mol ±Θ§ΤΫΚβΚσΜλΚœΈο÷–Α±ΒΡΧεΜΐΖ÷ ΐ(Π’)»γœ¬ΆΦΥυ ΨΓΘ
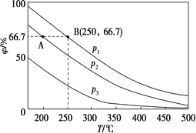
ΔΌΤδ÷–Θ§p1ΓΔp2 ΚΆp3 ”…¥σΒΫ–ΓΒΡΥ≥–ρ «____________Θ§ΗΟΖ¥”ΠΠΛH _______0(ΧνΓΑ>Γ±ΓΑ<Γ±ΜρΓΑΘΫΓ±)ΓΘ
ΔΎ»τΖ÷±π”ΟvA(N2)ΚΆvB(N2)±μ Ψ¥”Ζ¥”ΠΩΣ Φ÷Ν¥οΤΫΚβΉ¥Χ§AΓΔB ±ΒΡΜ·―ßΖ¥”ΠΥΌ¬ Θ§‘ρvA(N2)________vB(N2)(ΧνΓΑ>Γ±ΓΑ<Γ±ΜρΓΑΘΫΓ±)ΓΘ
Δέ»τ‘Ύ250 ΓφΓΔp1 ΈΣ105 PaΧθΦΰœ¬Θ§Ζ¥”Π¥οΒΫΤΫΚβ ±»ίΤςΒΡΧεΜΐΈΣ1 LΘ§‘ρΗΟΧθΦΰœ¬BΒψN2 ΒΡΖ÷―Ιp(N2)ΈΣ_______Pa (Ζ÷―ΙΘΫΉή―ΙΓΝΈο÷ ΒΡΝΩΖ÷ ΐΘ§±ΘΝτ“ΜΈΜ–Γ ΐ)ΓΘ
Δσ.“‘Ν§ΕΰΝρΥαΗυ(S2O42-)ΈΣΟΫΫιΘ§ Ι”ΟΦδΫ”ΒγΜ·―ßΖ®“≤Ω…¥Πάμ»ΦΟΚ―ΧΤχ÷–ΒΡNOΘ§ΉΑ÷Ο»γΆΦΥυ ΨΘΚ
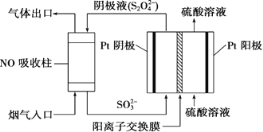
Θ®3Θ©ΔΌ“θΦΪ«χΒΡΒγΦΪΖ¥”Π ΫΈΣ___________ΓΘ
ΔΎNOΈϋ ’ΉΣΜ·ΚσΒΡ÷ς“Σ≤ζΈοΈΣNH4+Θ§»τΆ®Βγ ±Βγ¬Ζ÷–ΉΣ“ΤΝΥ0.3 mol eΘ≠Θ§‘ρ¥ΥΆ®ΒγΙΐ≥Χ÷–άμ¬έ…œΈϋ ’ΒΡNO‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐΈΣ________mLΓΘ
Δτ.Θ®4Θ©≥ΘΈ¬œ¬Θ§ΫΪa molΓΛL-1ΒΡ¥ΉΥα”κb molΓΛL-1Ba(OH)2 »ή“ΚΒ»ΧεΜΐΜλΚœΘ§≥δΖ÷Ζ¥”ΠΚσΘ§»ή“Κ÷–¥φ‘Ύ2c(Ba2+)=c(CH3COO-)Θ§‘ρΗΟΜλΚœ»ή“Κ÷–¥ΉΥαΒΡΒγάκ≥Θ ΐKa=___________(”ΟΚ§aΚΆbΒΡ¥ζ ΐ Ϋ±μ Ψ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣΖ¥”Π ΫΘΚmX(g)+nY(?)Q(s)+2mZ(g)Θ§“―÷ΣΖ¥”Π“―¥οΤΫΚβΘ§¥Υ ±c(X)=0.3mol/LΘ§ΤδΥϋΧθΦΰ≤Μ±δΘ§ΫΪ»ίΤςΥθ–ΓΒΫ‘≠ά¥ΒΡ![]() Θ§c(X)=0.5mol/LΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
Θ§c(X)=0.5mol/LΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.Ζ¥”ΠœρΡφΖ¥”ΠΖΫœρ“ΤΕ·
B.YΩ…Ρή «ΙΧΧεΜρ“ΚΧε
C.Μ·―ßΦΤΝΩ ΐnΘΨm
D.ZΒΡΧεΜΐΖ÷ ΐΦθ–Γ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥œϊΕΨ“ΚΒΡ÷ς“Σ≥…Ζ÷ΈΣNaClOΘ§ΜΙΚ§”–“ΜΕ®ΝΩΒΡNaOHΘ§œ¬Ν–”Οά¥Ϋβ Ά ¬ ΒΒΡΖΫ≥Χ Ϋ÷–≤ΜΚœάμΒΡ «Θ®“―÷ΣΘΚ±ΞΚΆNaClO»ή“ΚΒΡpH‘ΦΈΣ11Θ©
A. ΗΟœϊΕΨ“ΚΩ…”ΟNaOH»ή“ΚΈϋ ’Cl2÷Τ±ΗΘΚCl2+2OHΘ≠="==" ClΘ≠+ ClOΘ≠+ H2O
B. ΗΟœϊΕΨ“ΚΒΡpH‘ΦΈΣ12ΘΚClOΘ≠+ H2O![]() HClO+ OHΘ≠
HClO+ OHΘ≠
C. ΗΟœϊΕΨ“Κ”κΫύ≤όΝιΘ®÷ς“Σ≥…Ζ÷ΈΣHClΘ©Μλ”ΟΘ§≤ζ…ζCl2ΘΚ2HΘΪ+ ClΘ≠+ ClOΘ≠= Cl2Γϋ+H2O
D. ΗΟœϊΕΨ“ΚΦ”ΑΉ¥Ή…ζ≥…HClOΘ§Ω…‘ω«ΩΤ·ΑΉΉς”ΟΘΚCH3COOH+ ClOΘ≠= HClO+CH3COOΓΣ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΐΕ…Ϋπ τ‘ΣΥΊ―θΜ·ΈοΒΡ”Π”Ο―–ΨΩ «ΡΩ«ΑΩΤ―ß―–ΨΩΒΡ«Α―Ί÷°“ΜΘ§ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Δώ.Εΰ―θΜ·ν―ΉςΙβ¥ΏΜ·ΦΝΡήΫΪΨ” “Έέ»ΨΈοΦΉ»©ΓΔ±ΫΒ»”–ΚΠΤχΧεΩ…ΉΣΜ·ΈΣΕΰ―θΜ·ΧΦΚΆΥ°Θ§¥οΒΫΈόΚΠΜ·Θ°”–ΙΊΦΉ»©ΓΔ±ΫΓΔΕΰ―θΜ·ΧΦΦΑΥ°ΥΒΖ®’ΐ»ΖΒΡ «__ΓΘ
A.±Ϋ”κB3N3H6ΜΞΈΣΒ»ΒγΉ”Χε
B.ΦΉ»©ΓΔ±ΫΖ÷Ή”÷–ΧΦ‘≠Ή”Ψυ≤…”Οsp2‘”Μ·
C.±ΫΓΔΕΰ―θΜ·ΧΦ «Ζ«ΦΪ–‘Ζ÷Ή”Θ§Υ°ΚΆΦΉ»© «ΦΪ–‘Ζ÷Ή”
D.Υ°ΒΡΖ–Βψ±»ΦΉ»©ΗΏΒΟΕύΘ§ «“ρΈΣΥ°Ζ÷Ή”ΦδΡή–Έ≥…«βΦϋ
Δρ.2007Ρξ≈Β±¥ΕϊΈοάμ―ßΫ±ΈΣΖ®ΙζΩΤ―ßΦ“ΑΔΕϊ±¥Ζ―ΕϊΚΆΒ¬ΙζΩΤ―ßΦ“±ΥΒΟΗώΝ÷±¥ΗώΕϊΙ≤Ά§ΜώΒΟΘ§“‘±μ’ΟΥϊΟ«‘ΎΨό¥≈ΒγΉη–ß”Π(CMR–ß”Π)―–ΨΩΖΫΟφΒΡ≥…ΨΆΓΘΡ≥ΗΤν―–ΆΗ¥Κœ―θΜ·Έο(»γΆΦ1)Θ§“‘A‘≠Ή”ΈΣΨßΑϊΒΡΕΞΒψΘ§AΈΜΩ…“‘ «CaΓΔSrΓΔBaΜρPbΘ§Β±BΈΜ «VΓΔCrΓΔMnΓΔFe ±Θ§’β÷÷Μ·ΚœΈοΨΏ”–CMR–ß”ΠΓΘ
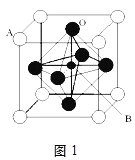
Θ®1Θ©”ΟAΓΔBΓΔO±μ Ψ’βάύΧΊ βΨßΧεΒΡΜ·―ß ΫΘΚ__ΓΘ
Θ®2Θ©“―÷ΣLaΈΣ+3ΦέΘ§Β±±ΜΗΤΒ»ΕΰΦέ‘ΣΥΊAΧφ¥ζ ±Θ§Ω…–Έ≥…Η¥ΚœΗΤν―ΩσΜ·ΚœΈοLa1-xAxMnO3Θ§(x<0.1)Θ§¥Υ ±“Μ≤ΩΖ÷ΟΧΉΣ±δΈΣ+4ΦέΓΘΒΦ÷¬≤ΡΝœ‘ΎΡ≥“ΜΈ¬Ε»ΗΫΫϋ”–Ζ¥Χζ¥≈-Χζ¥≈ΓΔΧζ¥≈-Υ≥¥≈ΉΣ±δΦΑΫπ τ-ΑκΒΦΧεΒΡΉΣ±δΘ§‘ρLa1-xAxMnO3÷–»ΐΦέΟΧ”κΥΡΦέΟΧΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣΘΚ__(”ΟΚ§xΒΡ¥ζ ΐ Ϋ±μ Ψ)ΓΘ
Θ®3Θ©MnΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣΘΚ___ΓΘ
Θ®4Θ©œ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «___ΓΘ
A.ογΓΔΟΧΓΔ―θΖ÷±πΈΜ”Ύ÷ήΤΎ±μfΓΔdΓΔp«χ
B.―θΒΡΒΎ“ΜΒγάκΡή±»ΒΣΒΡΒΎ“ΜΒγάκΡή¥σ
C.ΟΧΒΡΒγΗΚ–‘ΈΣ1.59Θ§CrΒΡΒγΗΚ–‘ΈΣ1.66Θ§ΥΒΟςΟΧΒΡΫπ τ–‘±»Ηθ«Ω
D.ΗθΒΡΕ―ΜΐΖΫ Ϋ”κΦΊœύΆ§Θ§‘ρΤδΕ―ΜΐΖΫ Ϋ»γΆΦ2ΘΚ
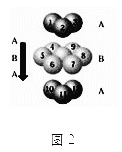
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“ΜΕ®ΧθΦΰœ¬Θ§‘ΎΧεΜΐΈΣ1LΒΡΟή±’»ίΤς÷–Θ§l molXΚΆ1 mol YΫχ––Ζ¥”ΠΘΚ2X(g)+Y(g) ![]() Z(g)Θ§œ¬Ν––π ωΡή÷ΛΟςΗΟΖ¥”Π“―¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§ΒΡ «( )ΓΘ
Z(g)Θ§œ¬Ν––π ωΡή÷ΛΟςΗΟΖ¥”Π“―¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§ΒΡ «( )ΓΘ
A.c(X)ΓΟc(Y)ΓΟc(Z) = 2ΓΟ1ΓΟlB.»ίΤςΡΎ‘≠Ή”Ήή ΐ≤Μ‘ΌΖΔ…ζ±δΜ·
C.XΒΡΑΌΖ÷Κ§ΝΩ≤Μ‘ΌΖΔ…ζ±δΜ·D.Ά§“Μ ±ΦδΡΎœϊΚΡ2n mol XΒΡΆ§ ±…ζ≥…n mol Z
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com