
下列说法或表示正确的是 ( )
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量少
B.A、B互为同素异形体,由A转化为B时ΔH=+119 kJ·mol-1可知B比A稳定
C.对ΔH < 0的化学反应,不需要加热,一定能够自发进行到底
D.在101 kPa时,H2燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(l) ΔH=-571.6
kJ·mol-1,则H2在101 kPa时的燃烧热为571.6 kJ·mol-1
科目:高中化学 来源: 题型:
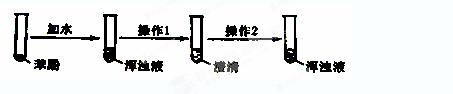
如下图所示的操作和实验现象,能证明苯酚的两个性质。则
性质I是 ,操作1是 、操作2是 。
性质II是 ,操作1是 、操作2是 。
写出所发生的化学方程式: ; 。
查看答案和解析>>
科目:高中化学 来源: 题型:
西亚一些国家连年动乱,油井发生火灾,产生大量的废气:①浓烟中的炭粒、②氮的氧化物、③碳的氧化物、④硫的氧化物、⑤碳氢化合物的蒸气,其中对大气造成污染并导致雨水酸化的有害、有毒气体是( )
A.①③⑤ B.②④ C.②③④ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组实验探究:探究碳、硅元素的非金属性的相对强弱。根据要求回答下列问题:
(1)实验装置如下:(装置E中盛足量酸性KMnO4溶液)

填写所示仪器名称A
(2)实验步骤: 连接仪器、_________ ____、加药品后,打开a、然后滴入浓硫酸,加热
(3)问题探究:①铜与浓硫酸反应的化学方程式是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性
___ __(填“能”或“否”),原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
关于常温下pH=2的醋酸溶液,下列叙述正确的是 ( )
A.c(CH3COOH)=0.01mol·L-1 B.c(H+)=c(CH3COO-)
C.加水稀释100倍后,溶液pH=4 D.加入醋酸钠固体,可抑制醋酸的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
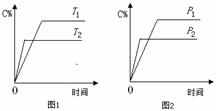
可逆反应A+a B 
 C+2 D(a为化学计量数),已知B、C、D为气态物质。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是 ( )
C+2 D(a为化学计量数),已知B、C、D为气态物质。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是 ( )
A.T2>T1,p2>p1
B.该反应为放热反应
C.若a=2,则A为液态或固态物质
D.增加B的物质的量,该反应的DH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列实验操作和现象,所得的实验结论正确的是 ( )
| 实验操作及现象 | 实验结论 | |
| A | 向2 mL 0.1 mol·L-1 CH3COOH溶液中滴加等浓度的NaHCO3溶液,有气泡产生 | 酸性: CH3COOH > H2CO3 |
| B | 向2 mL 0.1 mol·L-1 NaOH溶液中滴加3滴0.1 mol·L-1 MgCl2溶液,出现白色沉淀后,再滴加3滴0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀 | 碱性: Mg(OH)2>Fe(OH)3 |
| C | 在少量无水乙醇中加入金属Na,生成可以在空气中燃烧的气体 | CH3CH2OH是弱电解质 |
| D | 用3 mL稀H2SO4溶液与足量Zn反应,当气泡稀少时,加入1 mL浓H2SO4,又迅速产生较多气泡 | H2SO4浓度增大,反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关,下列情况会对人体健康造成较大危害的是
A.用Cl2对自来水进行消毒杀菌
B.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
C.用SO2漂白食品
D.用小苏打(NaHCO3)发酵面团制作馒头
查看答案和解析>>
科目:高中化学 来源: 题型:
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。NF3沸点-129 ℃,可在铜的催化作用下由F2和过量NH3反应得到。
(1) NF3分子构型: ,N原子杂化方式: 。
(2)写出制备 NF3的化学反应方程式: 。
(3)NF3的沸点比NH3的沸点(-33 ℃)低得多的主要原因是 。
(4)理论上HF、NaAlO2和NaCl按6∶1∶2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,则该物质的化学式为 。
(5)1~36元素中原子核外电子排布未成对电子数最多的元素其外围电子排布式为_____,有_________个能级;某元素原子的价电子为3d14s2,元素名称为_________,最高正化合价为_______;请写出有2个能层且p轨道中只有一个成对电子的基态原子的外围电子排布图__________________。
(6)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1 ),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①若以上五种元素为前四周期元素,则R为_____________。(填元素符号)
②若五种元素为主族元素,则T为__________区元素。
③若T为第三周期元素,E是第三周期元素中原子半径最小的元素,则T、E形成化合物的空间构型为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com