
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
科目:高中化学 来源:不详 题型:单选题
| A.还原性:HF>HCI>HBr>HI | B.稳定性:HF<HCl<HBr<HI |
| C.与水反应由易到难:Cl2>Br2>I2>F2 | D.密度:F2<Cl2<Br2<I2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素周期表有七个横行,分为七个周期 |
| B.元素周期表有九个横行,分为七个周期 |
| C.元素周期表有十八个纵行,分为十六个族 |
| D.元素周期表有十八个纵行,分为十八个族 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |



查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物中可能含有共价键 |
| B.共价化合物中可能含有离子键 |
| C.共价化合物中可能不含极性键 |
| D.金属离子一定是满足最外层2个电子或8个电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
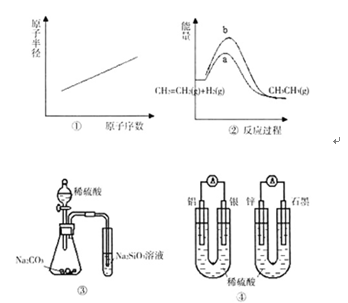
| A.图①表示第三周期元素原子半径的变化规律 |
| B.图②a、b曲线分别表示反应:CH2=CH2(g)+H2(g)→CH3CH3(g) △H>0,在使用和未使用催化剂时,反应过程中的能量变化 |
| C.图③所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
| D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第二周期元素氢化物稳定性顺序是HF>H2O>NH3;则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3 |
| B.Fe3O4可写成FeO·Fe2O3;Pb3O4也可写成PbO·Pb2O3 |
| C.可电解熔融MgCl2来制取金属镁;也能电解熔融AlCl3来制取金属铝 |
| D.晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com