
|
ŌŚ4”ꏱĻņ100 mLĖ®ÖŠČܽāĮĖ22.4 L””HClĘųĢå(±ź×¼×“æöĻĀ²āµĆ)ŗóŠĪ³ÉµÄČÜŅŗ£®ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ | |
A£® |
øĆČÜŅŗĪļÖŹµÄĮæÅضČĪŖ10 mol”¤L£1 |
B£® |
øĆČÜŅŗĪļÖŹµÄĮæÅضČŅņČÜŅŗµÄĆܶČĪ“ÖŖ¶ųĪŽ·ØĒóµĆ |
C£® |
øĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżŅņČÜŅŗµÄĆܶČĪ“ÖŖ¶ųĪŽ·ØĒóµĆ |
D£® |
ĖłµĆČÜŅŗµÄĢå»żĪŖ22.5 L |

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| 1 |
| 2 |
| 1 |
| 2 |
| ||||
|
| ||||
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
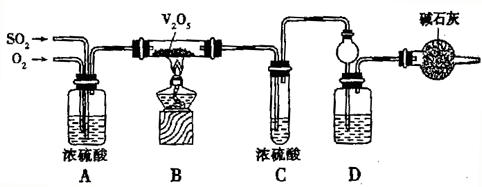
| ČŻĘ÷ | ĘšŹ¼Ź±ø÷ĪļÖŹµÄĮæ | µ½“ļĘ½ŗāŹ±·Å³öµÄČČĮæ£ØQkJ£© | Ę½ŗāŹ±SO2×Ŗ»ÆĀŹ £ØX£© | |||
| SO2£Ømol£© | O2£Ømol£© | SO3£Ømol£© | N2 | |||
| ¼× | 2 | 1 | 0 | 0 | Q1 | X1 |
| ŅŅ | 1 | 0.5 | 0 | 0 | Q2=39.4 | X2 |
| ±ū | 1 | 0.5 | 0 | 1 | Q3 | X3 |
| ¶” | 1.8 | 0.9 | 0.2 | 0 | Q4 | X4 |

| t1-t2 | t3-t4 | t4-t5 | t6-t7 |
| K1 | K2 | K3 | K4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 a Z£Øg£©+W£Øg£©”÷H=-Q kJ?mol-1£ØQ£¾0£©
a Z£Øg£©+W£Øg£©”÷H=-Q kJ?mol-1£ØQ£¾0£©| c(Z)?c(W1) |
| c2(X)?c(Y) |
| c(Z)?c(W1) |
| c2(X)?c(Y) |
| Q1 |
| Q |
| Q1 |
| Q |
| Q1 |
| Q |
| Q1 |
| Q |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā

| 500-850”ę |
| Īķ»Æŗó·ĻĮņĖįŅŗµĪÖ±¾¶ | ·ĻĮņĖįĶźČ«ĮŃ½āĖłŠčŹ±¼ä | |
| ĘÕĶØĪķ»ÆĘ÷ | 800-1200/¦Ģm | 10sŅŌÉĻ |
| Šż×ŖŹ½Īķ»ÆĘ÷ | 600-850 ¦Ģm | 8-10s |
| Ń¹Ėõ·ēĪķ»ÆĘ÷ | 400-650 ¦Ģm | 6-7s |
| ³¬Éł²ØĪķ»ÆĘ÷ | 100-300¦Ģm | 3.5-5s |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğÉĻŗ£ŹŠÕ¢±±ĒųøßČżÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŅŃÖŖŌŖĖŲMŹĒ×é³ÉĪļÖŹNH4Al£ØSO4£©2µÄŅ»ÖÖŌŖĖŲ”£ŌŖĖŲMµÄĘųĢ¬Ō×ÓÖšøöŹ§Č„µŚ1øöÖĮµŚ4øöµē×ÓĖłŠčÄÜĮæ£Ø¼“µēĄėÄÜ£¬ÓĆ·ūŗÅI1ÖĮI4±ķŹ¾£©ČēĻĀ±ķĖłŹ¾£ŗ
|
|
I1 |
I2 |
I3 |
I4 |
|
µēĄėÄÜ£ØkJ/mol£© |
578 |
1817 |
2745 |
11578 |
£Ø1£©ŌŖĖŲMµÄĆū³ĘŹĒ_______________£»
£Ø2£©ĮņŌ×ÓŗĖĶāÓŠ______ÖÖ²»Ķ¬ŌĖ¶ÆדĢ¬µÄµē×Ó£¬ÓŠ______ÖÖ²»Ķ¬ŠĪדµÄµē×ÓŌĘ£»
£Ø3£©ĒėÓĆŅ»øöŹĀŹµÖ¤Ć÷ŃõĘųµÄŃõ»ÆŠŌ±ČĮņµÄŃõ»ÆŠŌĒæ£ŗ______________________________”£
£Ø4£©ĻąĶ¬Ģõ¼žĻĀ£¬0.1 mol/L NH4Al£ØSO4£©2ÖŠc£ØNH4+£©________£ØĢī”°µČÓŚ”±”¢”°“óÓŚ”±»ņ”°Š”ÓŚ”±£©0.1 mol/LNH4HSO4ÖŠc£ØNH4+£©”£
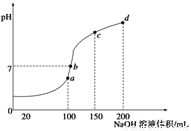
£Ø5£©ŹŅĪĀŹ±£¬Ļņ100 mL 0.1 mol/LNH4HSO4ČÜŅŗÖŠµĪ¼Ó0.1 mol/LNaOHČÜŅŗ£¬µĆµ½ČÜŅŗpHÓėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£ŗ
¢ŁŹŌ·ÖĪöĶ¼ÖŠa”¢b”¢c”¢dĖÄøöµć£¬Ė®µÄµēĄė³Ģ¶Č×ī“óµÄŹĒ____________£»
¢ŚŌŚbµć£¬ČÜŅŗÖŠø÷Ąė×ÓÅضČÓɓ󵽊”µÄÅÅĮŠĖ³ŠņŹĒ________£»
¢ŪŌŚc d¶Ī·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½_________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com