
·ÖĪö A”¢B”¢C”¢D”¢EĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ£¬CŌŖĖŲµÄ×īĶā²ćµē×ÓŹż±Č“ĪĶā²ćµē×ÓŹżÉŁ4£¬ŌņCŌŖĖŲŌ×ÓÓŠ3øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ4£¬ŌņCĪŖSiŌŖĖŲ£»DŌŖĖŲŌ×ÓŠņŹż“óÓŚ¹čŌŖĖŲ£¬“¦ÓŚµŚČżÖÜĘŚ£¬DŌŖĖŲŌ×Ó“ĪĶā²ćµē×ÓŹż±Č×īĶā²ćµē×ÓŹż¶ą3£¬Ōņ×īĶā²ćµē×ÓŹżĪŖ8-3=5£¬ŌņDĪŖĮ×ŌŖĖŲ£»A”¢B”¢EČżÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĮ½Į½½ŌÄÜ·¢Éś·“Ӧɜ³ÉŃĪŗĶĖ®£¬Ó¦ŹĒĒāŃõ»ÆĀĮÓėĒæĖį”¢Ēæ¼īµÄ·“Ó¦£¬ŌņAĪŖNa”¢BĪŖAl£¬ČżÖÖŌ×Ó×īĶā²ć¹²ÓŠ11øöµē×Ó£¬ŌņEµÄ×īĶā²ćµē×ÓŹżĪŖ11-1-3=7£¬ŌņEĪŖClŌŖĖŲ£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA”¢B”¢C”¢D”¢EĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ£¬CŌŖĖŲµÄ×īĶā²ćµē×ÓŹż±Č“ĪĶā²ćµē×ÓŹżÉŁ4£¬ŌņCŌŖĖŲŌ×ÓÓŠ3øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ4£¬ŌņCĪŖSiŌŖĖŲ£»DŌŖĖŲŌ×ÓŠņŹż“óÓŚ¹čŌŖĖŲ£¬“¦ÓŚµŚČżÖÜĘŚ£¬DŌŖĖŲŌ×Ó“ĪĶā²ćµē×ÓŹż±Č×īĶā²ćµē×ÓŹż¶ą3£¬Ōņ×īĶā²ćµē×ÓŹżĪŖ8-3=5£¬ŌņDĪŖĮ×ŌŖĖŲ£»A”¢B”¢EČżÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĮ½Į½½ŌÄÜ·¢Éś·“Ӧɜ³ÉŃĪŗĶĖ®£¬Ó¦ŹĒĒāŃõ»ÆĀĮÓėĒæĖį”¢Ēæ¼īµÄ·“Ó¦£¬ŌņAĪŖNa”¢BĪŖAl£¬ČżÖÖŌ×Ó×īĶā²ć¹²ÓŠ11øöµē×Ó£¬ŌņEµÄ×īĶā²ćµē×ÓŹżĪŖ11-1-3=7£¬ŌņEĪŖClŌŖĖŲ£¬
£Ø1£©ÓÉŅŌÉĻ·ÖĪöæÉÖŖAĪŖNa£¬BĪŖAl£¬CĪŖSi£¬DĪŖP£¬¹Ź“š°øĪŖ£ŗNa”¢Al”¢Si”¢P£»
£Ø2£©A”¢BŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·Ö±šĪŖNaOH”¢Al£ØOH£©3£¬¶žÕß·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗNaOH+Al£ØOH£©3=NaAlO2+2H2O£¬
¹Ź“š°øĪŖ£ŗNaOH+Al£ØOH£©3=NaAlO2+2H2O£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹”¢Ī»ÖĆÓėŠŌÖŹ£¬×ŪŗĻæ¼²éŌŖĖŲÖÜĘŚ±ķ”¢ÖÜĘŚĀÉŅŌ¼°Ō×Ó½į¹¹µÄĢŲµć£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬×¢Ņā°ŃĪÕŌ×Ó½į¹¹ĢŲµć£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Čõµē½āÖŹµÄµ¼µēÄÜĮ¦Ņ»¶Ø±ČĒæµē½āÖŹµÄµ¼µēÄÜĮ¦Čõ | |
| B£® | pH=4µÄ“×ĖįÓėpH=10µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗĻŌ¼īŠŌ | |
| C£® | ¶¹½¬ÖŠ¼ÓČėĮņĖįøĘ»įŹ¹µ°°×ÖŹ¾Ū³Į£® | |
| D£® | Ķ¬ÅØ¶ČµÄ¢ŁNaHCO3¢ŚNa2CO3¢ŪCH3COONaĖÄÖÖČÜŅŗ£¬pHÖµ“óŠ”ÅÅĮŠĖ³ŠņŹĒ¢Ś£¾¢Ł£¾¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
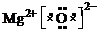 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
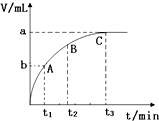 ĪŖĮĖŃŠ¾æĶā½ēĢõ¼ž¶Ō¹żŃõ»ÆĒā·Ö½āĖŁĀŹµÄÓ°Ļģ£¬Ä³Ķ¬Ń§×öĮĖŅŌĻĀŹµŃ飬Ēė»Ų“šĻĀĮŠĪŹĢā£®
ĪŖĮĖŃŠ¾æĶā½ēĢõ¼ž¶Ō¹żŃõ»ÆĒā·Ö½āĖŁĀŹµÄÓ°Ļģ£¬Ä³Ķ¬Ń§×öĮĖŅŌĻĀŹµŃ飬Ēė»Ų“šĻĀĮŠĪŹĢā£®| ±ąŗÅ | ²Ł ×÷ | ŹµŃéĻÖĻó |
| ¢Ł | ·Ö±šŌŚŹŌ¹ÜA”¢BÖŠ¼ÓČė 5mL 5% H2O2ČÜŅŗ£¬ø÷µĪČė1”«2 µĪ1mol/L FeCl3ČÜŅŗ£®“żŹŌ¹ÜÖŠ¾łÓŠŹŹĮæĘųÅŻ³öĻÖŹ±£¬½«ŹŌ¹ÜA·ÅČėŹ¢ÓŠ5”ę×óÓŅĄäĖ®µÄÉÕ±ÖŠ£»½«ŹŌ¹ÜB·ÅČėŹ¢ÓŠ40”ę×óÓŅČČĖ®µÄÉÕ±ÖŠ£® | ŹŌ¹ÜAÖŠ²»ŌŁ²śÉśĘųÅŻ£¬ŹŌ¹ÜBÖŠ²śÉśµÄĘųÅŻĮæŌö“ó |
| ¢Ś | ĮķČ”Į½Ö§ŹŌ¹Ü·Ö±š¼ÓČė 5mL 5%H2O2ČÜŅŗŗĶ 5mL10%H2O2ČÜŅŗ£® | ŹŌ¹ÜA”¢BÖŠ¾łĪ“¼ūĘųÅŻ²śÉś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹŅĪĀĻĀ£¬²āµĆĀČ»Æļ§ČÜŅŗpH£¼7£¬Ö¤Ć÷Ņ»Ė®ŗĻ°±ŹĒČõ¼ī£ŗNH4++2H2O=NH3•H2O+H3O+ | |
| B£® | ÓĆĒāŃõ»ÆÄĘČÜŅŗ³żČ„Ć¾·ŪÖŠµÄŌÓÖŹĀĮ£ŗ2Al+2OH-+2H2O=2AlO2-+3H2”ü | |
| C£® | ÓĆĢ¼ĖįĒāÄĘČÜŅŗ¼ģŃéĖ®ŃīĖįÖŠµÄōČ»ł£ŗ | |
| D£® | ÓĆøßĆĢĖį¼Ų±ź×¼ČÜŅŗµĪ¶Ø²ŻĖį£ŗ2MnO4-+16H++5C2O42-=2Mn2++10CO2”ü+8H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓŠæÉÄÜŹĒ½šŹō¾§Ģå | B£® | ÓŠæÉÄÜŹĒĄė×Ó¾§Ģå | ||
| C£® | Ņ»¶ØŹĒ·Ö×Ó¾§Ģå | D£® | Ņ»¶Ø²»ŹĒŌ×Ó¾§Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ¹²¼Ū¼ü | ¼üÄÜ | ¹²¼Ū¼ü | ¼üÄÜ |
| H-H | 436 | H-F | 565 |
| C-F | 427 | H-S | 339 |
| C-Cl | 330 | H-Se | 314 |
| A£® | H2£Øg£©”ś2H £Øg£©-436kJ | |
| B£® | ¼ü³¤Ō½¶Ģ£¬¹²¼Ū¼üŌ½ĄĪ¹Ģ | |
| C£® | ĻąĶ¬Ģõ¼žĻĀCH3F±ČCH3Cløü Ņ×·¢ÉśĖ®½ā·“Ó¦ | |
| D£® | ĻąĶ¬Ń¹ĒæĻĀ£¬H2SµÄ·Šµć±Č H2SeµÄ·Šµćøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬2.24 L Cl4ÖŠŗ¬CLŌ×ÓŹżÄæĪŖ0.4NA | |
| B£® | °×Į×·Ö×Ó£ØP4£©³ŹÕżĖÄĆęĢå½į¹¹£¬12.4g°×Į×ÖŠŗ¬ÓŠP-P¼üŹżÄæĪŖ0.6NA | |
| C£® | 5.6gĢś·ŪŌŚ2.24 L£Ø±ź×¼×“æö£©ĀČĘųÖŠ³ä·ÖČ¼ÉÕ£¬Ź§Č„µÄµē×ÓŹéĪŖ0.3NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ10g46%¾Ę¾«ČÜŅŗÖŠŗ¬ŃõŌ×Ó×ÜŹżĪŖ 0.3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com