
| A. | 酸性强弱:HClO4>H2SO4>H3PO4 | B. | 离子半径:Na+>Mg2+>Al3+>F- | ||
| C. | 热稳定性:H2S>PH3>SiH4>HCl | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |
分析 A.非金属性越强,最高价氧化物对应水合物的酸性越强;
B.离子的电子层越多,离子半径越大,电子层相同时,离子的核电荷数越大,离子半径越小;
C.非金属性越强,对应氢化物越稳定;
D.金属性越强,最高价氧化物对应水合物的碱性越强.
解答 解:A.非金属性:Cl>S>P,则最高价氧化物对应水合物的酸性:HClO4>H2SO4>H3PO4,故A正确;
B.四种离子的电子层数相同,核电荷数越大,离子半径越小,则离子半径大小为:F->Na+>Mg2+>Al3+,故B错误;
C.非金属性:Cl>S>Si>P,则氢化物的热稳定性:HCl>H2S>PH3>SiH4,故C错误;
D.金属性:Na>Ma>Al,则最高价氧化物对应水合物的碱性:NaOH>Mg(OH)2>Al(OH)3,故D正确;
故选BC.
点评 本题考查了原子结构与元素周期律的关系,题目难度不大,明确元素周期律内容为解答关键,注意熟练掌握 原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
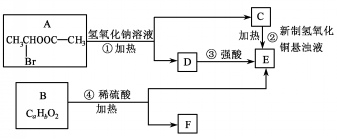
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,B的结构简式
,B的结构简式
 +HBr→
+HBr→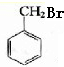 +H2O
+H2O
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
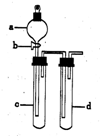 某兴趣小组设计出如图所示装置来进行“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来进行“铜与硝酸反应”实验,以探究化学实验的绿色化.| 方 案 | 反 应 物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸能与水以任意比例混溶 | B. | 醋酸能与碳酸钠反应 | ||
| C. | 醋酸能使紫色石蕊试液变红色 | D. | 0.1mol.L-1醋酸溶液pH=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的电子式: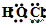 | |
| B. | 质子数为6、质量数为14的原子:${\;}_6^{14}N$ | |
| C. | CS2的结构式:S=C=S | |
| D. | 氯的原子结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 合金的熔点一般比其各成分金属的熔点低 | |
| C. | 铝钠合金投入到足量氯化铜溶液中,可能有铜析出 | |
| D. | mg不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则钠的质量分数越大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com