
将3.2克H2和CO的混合气体(其密度为相同条件下氧气密度的1/2),通入一盛有足量Na2O2密闭容器中,再通入过量O2,并用电火花点燃使其充分反应,最后容器中固体的质量增加了
A.3.2 g B.4.4 g C.5.6 g D.6.4 g
A
【解析】
试题分析:CO与氧气反应:2CO+O2 =2CO2,二氧化碳与过氧化钠反应:2CO2+2Na2O2=2Na2CO3+O2,总方程式为2CO+2Na2O2=2Na2CO3,固体增加的质量为CO的质量,氢气与氧气反应:2H2+O2 =2H2O,Na2O2与H2O反应:2H2O+2Na2O2=4NaOH+O2,总方程式为:2H2+2Na2O2=4NaOH,固体增加的质量为氢气质量,则CO和H2的混合气共3.2g与足量的Na2O2于密闭容器中,通入氧气用电火花点燃,充分反应后,固体增重质量是3.2g,故选A。
考点:本题考查混合物的计算,侧重于学生的分析能力和计算能力的考查,难度中等,注意从CO2、H2O与Na2O2生成固体质量的变化分析规律,是解答该题的关键。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、3.2g | B、4.4g |
| C、5.6g | D、6.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:
能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标。
(1)如图所示,组成一个原电池.
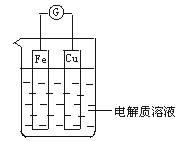
①当电解质溶液为稀硫酸时:
Cu电极是_____(填“正”或“负”)极,其电极反应为____,该反应是____(填“氧化”或“还原”)反应;
②当电解质溶液为浓硝酸时:
Cu电极是_____极,其电极反应为__________,该反应是_____反应.
(2)电解是将 能转化为 能。请写出电解硫酸铜溶液的总化学方程式____________
(3)燃烧氢气时耗氧量小,发热量大.已知4克H2燃烧生成液态水时放热为571.6kJ,试写出表示H2燃烧热的热化学方程式为: .
(4)下图是一碳酸盐燃料电池(MCFC),以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质。写出B极发生的电极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com