
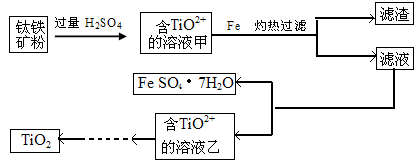
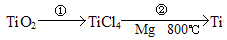
 TiO2·xH2O↓ + 4HCl
TiO2·xH2O↓ + 4HCl 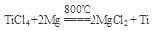 稀有气体保护,防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用
稀有气体保护,防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用 TiO2·xH2O↓ + 4HCl. ②检验TiO2·XH2O中Cl-是否被除净的方法是取最后一次洗涤液少量,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净。(5)根据题意和已知条件可得反应的方程式为
TiO2·xH2O↓ + 4HCl. ②检验TiO2·XH2O中Cl-是否被除净的方法是取最后一次洗涤液少量,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净。(5)根据题意和已知条件可得反应的方程式为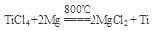 。因为Mg及反应产生的Ti容易与其它物质发生反应,为防止在高温下它们与空气中的氧气反应,所以该反应成功需要在稀有气体的环境中进行。2的制取方法及以TiO2为原料制取钛单质的反应原理、混合物的分离方法、反应条件的选择。
。因为Mg及反应产生的Ti容易与其它物质发生反应,为防止在高温下它们与空气中的氧气反应,所以该反应成功需要在稀有气体的环境中进行。2的制取方法及以TiO2为原料制取钛单质的反应原理、混合物的分离方法、反应条件的选择。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.先加稀盐酸将溶液酸化,再滴加氯化钡溶液,看是否生成白色沉淀 |
| B.先加稀硝酸将溶液酸化,再滴加氯化钡溶液,看是否生成白色沉淀 |
| C.直接向溶液中滴加稀硝酸酸化过的氯化钡溶液,看是否生成白色沉淀 |
| D.直接向溶液中滴加稀盐酸酸化过的氯化钡溶液,看是否生成白色沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.除去苯中混有的少量苯酚,可加入浓溴水后过滤 |
| B.除去乙酸乙酯中混有的少量乙酸,可加入饱和碳酸钠溶液分液 |
| C.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤 |
| D.除去石英中混有的少量铝粉,可加入氢氧化钠溶液溶解后过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
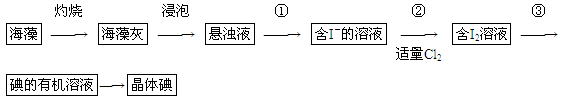 (1)实验操作③的名称是________,所用主要仪器名称为________。
(1)实验操作③的名称是________,所用主要仪器名称为________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某钠盐溶液中加入过量盐酸,产生能使澄清石灰水变浑浊的无色气体 | 该溶液为Na2CO3溶液 |
| B | 在有镀层的铁片上,用刀刻一槽,在槽上滴入少量0.1 mol/L盐酸,一段时间后滴入KSCN溶液,无红色出现 | 一定是镀锡的马口铁片 |
| C | 配制SnCl2溶液时,先将SnCl2溶于适量浓盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的锡粒 | 抵制Sn2+水解,并防止Sn2+被氧化为Sn4+ |
| D | 向等浓度的NaCl和KI的混合溶液中,逐滴加入AgNO3溶液,溶液中先产生黄色沉淀,后产生白色沉淀 | Ksp(AgCl)< Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
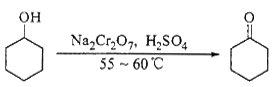
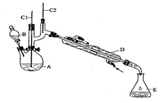
| 物质 | 沸点(℃) | 密度(g·cm-3, 20℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95) | 0.9478 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.3301 | |
| 水 | 100.0 | 0.9982 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
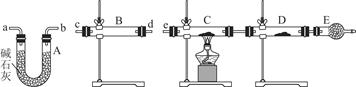
| 装置 | 所盛药品 | 实验现象 | 结论或解释 |
| B | | | |
| C | CuO固体 | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com