
| A. | NaNO3 | B. | MgCl2 | C. | SiO2 | D. | C2H4 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,据此分析解答.
解答 解:A.硝酸钠中钠离子和硝酸根离子之间存在离子键、N-O原子之间存在共价键,所以离子化合物,故A正确;
B.氯化镁中镁离子和氯离子之间只存在离子键,属于离子化合物,故B错误;
C.二氧化硅中Si-O原子之间只存在共价键,属于共价化合物,故C错误;
D.乙烯分子中C-C、C-H原子之间只存在共价键,属于共价化合物,故D错误;
故选A.
点评 本题考查离子键、共价键、离子化合物和共价键化合物的判断,侧重考查基本概念,明确物质构成微粒及物质之间作用力即可解答,注意B中两个氯原子之间不存在化学键,为易错点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ②③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸干碳酸钾溶液得到的固体物质为KOH | |
| B. | 铁表面镀铜时,铜与电源的负极相连,而铁与电源的正极相连 | |
| C. | 工业合成氨反应温度选择700 K左右,可使催化剂活性最强并提高原料利用率 | |
| D. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=2×283.0kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同主族元素随原子序数递增,元素原子的得电子能力逐渐增强 | |
| B. | 同主族元素随原子序数递增,单质氧化能力逐渐增强 | |
| C. | 同主族元素原子最外层电子数都相同 | |
| D. | 同主族元素的原子半径,随原子序数增大而逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
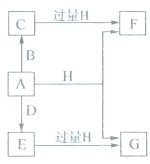
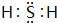 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com