
分析 由于NaCl混有Na2SO4和NaHCO3,故应先将样品加热,使NaHCO3分解为Na2CO3,待冷却后加水溶解,然后加入足量的BaCl2溶液除去SO42-和CO32-,生成BaSO4和BaCO3沉淀,然后过滤,在滤液中除了主要是NaCl,还有过量的BaCl2,故应加入过量的Na2CO3溶液,然后加盐酸除去过量的Na2CO3即可.据此分析.
解答 解:由于NaCl混有Na2SO4和NaHCO3,故应先将样品加热,使NaHCO3分解为Na2CO3,待冷却后加水溶解,然后加入足量的BaCl2溶液除去SO42-和CO32-,生成BaSO4和BaCO3沉淀,然后过滤,在滤液中除了主要是NaCl,还有过量的BaCl2,故应加入过量的Na2CO3溶液,然后加盐酸除去过量的Na2CO3即可.
(1)由上述分析可知,正确的操作顺序是:DACBE,故答案为:DACBE;
(2)D项中给样品加热时,NaHCO3分解为Na2CO3,化学方程式为:2NaHCO3$\frac{\underline{\;加热\;}}{\;}$Na2CO3+CO2↑+H2O,故答案为:2NaHCO3$\frac{\underline{\;加热\;}}{\;}$Na2CO3+CO2↑+H2O;
(3)向烧杯中加入足量的碳酸钠能除去过量的BaCl2,故答案为:除去过量的BaCl2;
(4)如果BaCl2已过量,则溶液中无SO42-和CO32-,则取上层清液于试管中,继续滴加BaCl2溶液,如果无沉淀产生,则BaCl2已过量.故答案为:取上层清液于试管中,继续滴加BaCl2溶液,如果无沉淀产生,则BaCl2已过量;
(5)测滤液的PH达5-6时,应用pH试纸,故答案为:pH试纸.
点评 本题考查了粗盐提纯过程中的操作顺序和加入试剂的目的以及所对应的反应,难度不大,根据题目所提供的信息分析出提出的步骤是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol CO(g)+1/2O2(g)═CO2(g),△H=-283.0 kJ/mol C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol | |
| C. | 在0.1mol/L的氨水中加水稀释,氨水的导电能力降低 | |
| D. | 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=$\frac{(ca)^{2}}{c(1-a)}$.若加入少量醋酸钠固体,则CH3COOH?CH3COO-+H+向左移动,α减小,Ka变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①=②>③>④>⑤ | B. | ④>③>①=⑤>② | C. | ③>①>②>④>⑤ | D. | ④>③>①>⑤>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0℃101kpa下22.4L氦气含质子的数目为4NA | |
| B. | 将CO2通入Na2O2使其增重a g时,反应中转移电子数目为NA | |
| C. | 标况下,将2.24L NH3溶于100ml水,所得溶液中粒子个数关系N(NH4+)+N(NH3•H2O)=0.1NA | |
| D. | 常温常压下14g氮气所含共用电子对数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 组别 | 温度/℃ | V(H2C2O4) /mL | V(KMnO4) /mL | V(H2O) /mL | KMnO4溶液 褪色时间/s |
| 1 | 30 | 10 | 10 | 20 | 40 |
| 2 | 30 | 20 | 20 | 0 | t |
| 3 | 30 | 15 | 10 | 15 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、SiO32-、Cl-、NO3- | B. | Cu2+、NH4+、Al3+、SO42- | ||
| C. | Na+、S2-、OH-、SO42- | D. | Na+、ClO-、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
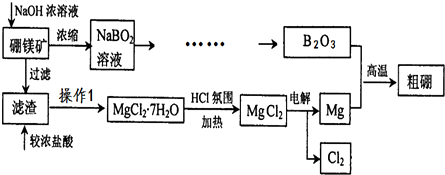

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com