
����Ŀ����������������Ʒ����Ѫ������������(33%)�����ѱ�����Ϊ����������θ������ֱ�����룬��θ�Ĥ�̼���С����һ������ȱ����ƶѪ�İ�ȫ��Ч�����Ƽ���ʵ����÷���ϩ����(�ֳƸ�����) Ϊԭ�ϣ����ʵ���pH��������Fe2+�γ�������ͼ25�Ǻϳɸ���������һ�ֹ���·��:

�ش���������:
��1��A�ĽṹΪ_______(�ýṹ��ʽ�����ʽ��ʾ)��B�Ļ�ѧ����Ϊ_______����A����B�ķ�Ӧ����Ϊ_______ ��
��2�� C��NaOH�Ҵ���Һ�з�Ӧ�ķ���ʽΪ_______ ��
��3�� ������Ľṹ��ʽΪ_______ ��
��4�����鸻Ѫ�����Ƿ���Fe3+��ʵ�����������_______ ��
��5��������Ϊ��Ԫ���ᣬ1mol����������������NaHCO3��Һ��Ӧ�ɷų�_______LCO2 (�����)���������ͬ���칹����������˳���칹����ͬΪ��Ԫ����Ļ���_______��д���ṹ��ʽ����
��6����ʯ���ѽ��еõ���1,3-����ϩ�ϳɶ�ϩ����ʱ��![]() �ǹؼ����м������÷�Ӧ����ͼ��ʾ��H2C=CH-CH=CH2��
�ǹؼ����м������÷�Ӧ����ͼ��ʾ��H2C=CH-CH=CH2��![]() �ı仯���̡�_____________
�ı仯���̡�_____________
���𰸡� ![]() һ�Ȼ����� ȡ����Ӧ
һ�Ȼ����� ȡ����Ӧ 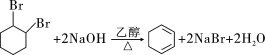
![]() ȡ������Ѫ��������ϡ�����ܽ⣬�ٵμ�KSCN��Һ������Һ��Ѫ��ɫ�����Ʒ�к���Fe3+����֮������Fe3+ 44.8
ȡ������Ѫ��������ϡ�����ܽ⣬�ٵμ�KSCN��Һ������Һ��Ѫ��ɫ�����Ʒ�к���Fe3+����֮������Fe3+ 44.8 ![]() ��
��![]()
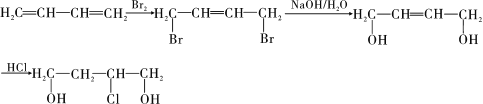
���������������������ڹ�������������BΪ±������B������ȥ��Ӧ���ɻ���ϩ����BΪ![]() ������ϩ���巢���ӳɷ�Ӧ����CΪ
������ϩ���巢���ӳɷ�Ӧ����CΪ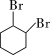 ��C�ٷ�����ȥ��Ӧ����
��C�ٷ�����ȥ��Ӧ����![]() ��
��![]() ����������ȡ����Ӧ����
����������ȡ����Ӧ����![]() ��
��![]() ����������Ӧ����
����������Ӧ����![]() ���ٷ�����ȥ��Ӧ���кͷ�Ӧ�õ�
���ٷ�����ȥ��Ӧ���кͷ�Ӧ�õ�![]() �������ữ�õ�������Ϊ
�������ữ�õ�������Ϊ![]() ����ʽ�ṹ����������Ϊ��Ԫ���ᣬ1mol����������������NaHCO3��Һ��Ӧ�ɷų�2mol CO2����������ɶ�����̼�����Ϊ2mol��22.4L/mol=44.8L���������ͬ���칹���У�ͬΪ��Ԫ����Ļ���
����ʽ�ṹ����������Ϊ��Ԫ���ᣬ1mol����������������NaHCO3��Һ��Ӧ�ɷų�2mol CO2����������ɶ�����̼�����Ϊ2mol��22.4L/mol=44.8L���������ͬ���칹���У�ͬΪ��Ԫ����Ļ���![]() ��
��![]() ��
��
��1��.��������������֪��AΪ![]() �� BΪ��
�� BΪ��![]() ����ѧ����Ϊһ�Ȼ����飬��A����B�ķ�Ӧ����Ϊȡ����Ӧ���ʴ�Ϊ��
����ѧ����Ϊһ�Ȼ����飬��A����B�ķ�Ӧ����Ϊȡ����Ӧ���ʴ�Ϊ��![]() ��һ�Ȼ����飻ȡ����Ӧ��
��һ�Ȼ����飻ȡ����Ӧ��
��2��.CΪ ����NaOH�Ҵ���Һ�з�����ȥ��Ӧ����Ӧ�ķ���ʽΪ��
����NaOH�Ҵ���Һ�з�����ȥ��Ӧ����Ӧ�ķ���ʽΪ��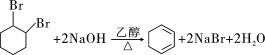 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3��.������������֪��������Ľṹ��ʽΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��4��.���鸻Ѫ�����Ƿ���Fe3+������ȡ������Ѫ��������ϡ�����ܽ⣬�ٵμ�KSCN��Һ������Һ��Ѫ��ɫ�����Ʒ�к���Fe3+����֮������Fe3+���ʴ�Ϊ��ȡ������Ѫ��������ϡ�����ܽ⣬�ٵμ�KSCN��Һ������Һ��Ѫ��ɫ�����Ʒ�к���Fe3+����֮������Fe3+��
��5��.������Ϊ��Ԫ���ᣬ��1mol����������������NaHCO3��Һ��Ӧ�ɷų�2molCO2 ���ڱ�״���µ������44.8L���������ͬ���칹���У�����˳���칹����ͬΪ��Ԫ����Ļ�����![]() ��
��![]() ���ʴ�Ϊ��44.8��
���ʴ�Ϊ��44.8��![]() ��
��![]() ��
��
��6����H2C=CH-CH=CH2����![]() ������H2C=CH-CH=CH2���巢��1��4-�ӳ�����
������H2C=CH-CH=CH2���巢��1��4-�ӳ�����![]() ��
��![]() ��NaOH��Һ��ˮ������
��NaOH��Һ��ˮ������![]() ��
��![]() ��HCl�����ӳɷ�Ӧ����
��HCl�����ӳɷ�Ӧ����![]() ���ϳ�·��Ϊ��
���ϳ�·��Ϊ��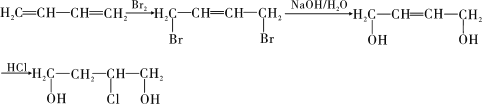 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1molX�����amolY����������ɱ���ܱ������з������·�Ӧ��X��g��+aY��g��![]() bZ��g��.��Ӧ�ﵽƽ����X��ת����Ϊ25��.���ң���ͬ��ͬѹ�»���÷�Ӧǰ���������ܶ��Ƿ�Ӧ���������ܶȵ�5/6����a��b��ֵ�����ǣ� ��
bZ��g��.��Ӧ�ﵽƽ����X��ת����Ϊ25��.���ң���ͬ��ͬѹ�»���÷�Ӧǰ���������ܶ��Ƿ�Ӧ���������ܶȵ�5/6����a��b��ֵ�����ǣ� ��
A. a=1,b=2 B. a=1,b=3
C. a=2,b=3 D. a=2,b=1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��Na2S2O3+H2SO4�TNa2SO4+SO2��+S��+H2O������ͨ�����ֻ��ǵĿ������жϷ�Ӧ�Ŀ����̶ȣ����и���ʵ�������ȳ��ֻ��ǵ��ǣ�������
ʵ�� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | ||
V/mL | c/��molL��1�� | V/mL | c/��molL��1�� | ||
A | 25 | 5 | 0.1 | 20 | 0.1 |
B | 25 | 5 | 0.2 | 10 | 0.2 |
C | 35 | 5 | 0.1 | 20 | 0.1 |
D | 35 | 5 | 0.2 | 10 | 0.2 |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ƺ������Ƶ���������ȷ���ǣ� ��
A.���ǰ�ɫ����B.���������Ӹ����Ȳ���ͬ
C.������ˮ��Ӧ����ǿ����ҺD.����ǿ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ࣨGe���ǵ��͵İ뵼��Ԫ�أ��ڵ��ӡ����ϵ�����Ӧ�ù㷺���ش��������⣺
��1����̬Geԭ�ӵĺ�������Ų�ʽΪ[Ar] �� ����δ�ɶԵ��ӣ�
��2��Ge��C��ͬ��Ԫ�أ�Cԭ��֮������γ�˫������������Geԭ��֮�������γ�˫������������ԭ�ӽṹ�Ƕȷ�����ԭ���� ��
��3���Ƚ�������±������۵�ͷе㣬������仯���ɼ�ԭ�� ��
GeCl4 | GeBr4 | GeI4 | |
�۵�/�� | ��49.5 | 26 | 146 |
�е�/�� | 83.1 | 186 | Լ400 |
��4�������ԭCO2�Ʊ�CH4��Ӧ�У���״����Zn2GeO4�Ǹ÷�Ӧ�����ô�����Zn��Ge��O�縺���ɴ���С��˳���� ��
��5��Ge�������н��ʯ�ͽṹ������Geԭ�ӵ��ӻ���ʽΪ��֮����ڵ��������� ��
��6����������������Ҫ�أ���ԭ�������������ʾ�����ڲ���ԭ�ӵ����λ�ã���ͼ��1��2��ΪGe�����ľ���������ԭ���������AΪ��0��0��0����BΪ�� ![]() ��0��
��0�� ![]() ����C��
����C�� ![]() ��
�� ![]() ��0������Dԭ�ӵ��������Ϊ ��
��0������Dԭ�ӵ��������Ϊ ��
�ھ������������������Ĵ�С����״����֪Ge�����ľ�������a=565.76pm�����ܶ�Ϊgcm��3���г�����ʽ���ɣ���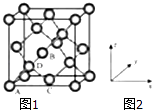
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������У�������һ��������ͬ��Ԫ��ԭ�ӵ��ǣ� ��
A.3p�ܼ���һ���չ���Ļ�̬ԭ�Ӻͺ�������Ų�Ϊ1s22s22p63s23p2��ԭ��
B.M��ȫ������N��Ϊ4s2��ԭ�Ӻͺ�������Ų�Ϊ1s22s22p63s23p63d64s2��ԭ��
C.�����������Ǻ������������1/5��ԭ�Ӻͼ۵����Ų�Ϊ4s24p5��ԭ��
D.2p�ܼ���һ��δ�ɶԵ��ӵĻ�̬ԭ�Ӻ�ԭ�ӵļ۵����Ų�Ϊ2s22p5��ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ٷ����ڷ�ҺΪ������ʹҩ����Ҫ��������ͷʹ�����գ�����Ҫ��ѧ�ɷֵĽṹ��ʽΪ�� ![]() �������йظ��л���������ȷ���ǣ� ��
�������йظ��л���������ȷ���ǣ� ��
A.����ʽΪC8H10NO2
B.�����ڦ����������ͬ���칹����3��
C.���л������ڦ���������
D.���л������FeCl3��Һ������ɫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���A��C��H��O����Ԫ����ɣ���һ�������£�A��B��C��D��E֮���ת����ϵ��ͼ����֪C�������ܶ�����ͬ������������22�������ɷ���������Ӧ�� 
д������ת���Ļ�ѧ����ʽ��
��1��B��Ϊ�߷�����
��2��A+O2��C��
��3��A+D��E ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ����Ϊ�ɻ�ѧ�����Ѻ��»�ѧ���γɵĹ��̡���ѧ���ļ�����ָ��(���γ�)1 molij��ѧ��������(��ų�)����������֪����(P4)��P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�P��PΪ198 kJ/mol��P��OΪ360 kJ/mol��������������ԭ�Ӽ�ļ���Ϊ498 kJ/mol����P4(s)��3O2(g)===P4O6(s)�ķ�Ӧ�Ȧ�HΪ(����)

A. ��1 638 kJ/mol B. ��1 638 kJ/mol
C. ��126 kJ/mol D. ��126 kJ/mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com