
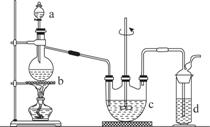
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂。它易溶于水,不溶于醇,受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2制得。实验室模拟该工业过程的装置如图所示。
回答下列问题:
(1)b中反应的离子方程式为________________,c中试剂为________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是________。
(3)d中的试剂为________。
(4)实验中要控制SO2生成速率,可以采取的措施有___________________________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是______________________。
(6) 所得产品常含有少量Na2SO3和Na2SO4。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀盐酸、蒸馏水中选择)
①取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,________________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
②为减少装置C中生成Na2SO4的量,在实验过程中应注意的操作顺序是_______________________________________________________________________。
【知识点】化学实验操作 B2 D3 G1
【答案解析】(16分)SO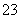 +2H+===SO2↑+H2O或HSO
+2H+===SO2↑+H2O或HSO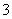 +H+===SO2↑+H2O (2分)硫化钠和碳酸钠混合溶液(2分)
+H+===SO2↑+H2O (2分)硫化钠和碳酸钠混合溶液(2分)
(2)硫(2分) (3)NaOH溶液(2分)
(4)控制反应温度、调节酸的滴加速率(或调节酸的浓度等) (2分)
(5)若SO2过量,溶液显酸性,产物分解(2分)
(6)①过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸 (2分)
②先向烧瓶滴加浓H2SO4,产生的气体将装置中的空气排尽后,再向C中烧瓶加入Na2S和Na2CO3混合溶液(2分)
解析::(1)第一个装置为二氧化硫的制取装置,制取二氧化硫的原料为亚硫酸钠和70%的浓硫酸,反应的离子方程式为:SO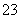 +2H+===SO2↑+H2O,c装置为Na2S2O3的生成装置,根据反应原理可知c中的试剂为:硫化钠和碳酸钠的混合溶液,故答案为:SO
+2H+===SO2↑+H2O,c装置为Na2S2O3的生成装置,根据反应原理可知c中的试剂为:硫化钠和碳酸钠的混合溶液,故答案为:SO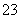 +2H+===SO2↑+H2O或HSO
+2H+===SO2↑+H2O或HSO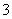 +H+===SO2↑+H2O 硫化钠和碳酸钠混合溶液
+H+===SO2↑+H2O 硫化钠和碳酸钠混合溶液
(2)反应开始时发生的反应为:Na2S+4SO2+H2O=2H2S+Na2SO3,SO2+2H2S=3S↓+2H2O,故该浑浊物是S,故答案为:S;
(3)d装置为尾气吸收装置,吸收二氧化硫和硫化氢等酸性气体,应选用氢氧化钠溶液,故答案为:氢氧化钠溶液;
(4)通过控制反应的温度或硫酸的滴加速度可以控制SO2生成速率,故答案为:控制反应的温度或硫酸的滴加速度;
(5)硫代硫酸钠遇酸易分解,若通入的SO2过量,则溶液显酸性,硫代硫酸钠会分解
(6)①根据:Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl;BaSO4难溶于水,难溶于稀HCl,以及硝酸具有强氧化性、加入硫酸会引入硫酸根离子可知,取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸,若沉淀未完全溶解,并有刺激性气味的气体产生,则可以确定产品中含有Na2SO3和Na2SO4,故答案为:过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸;
②因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na2SO4的量,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液,故答案为:先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液;
【思路点拨】本题考查了物质制备实验方案的设计和制备过程分析应用,掌握基础如离子反应方程式、定性检验、除杂,注意积累是解题关键,题目难度中等.


科目:高中化学 来源: 题型:
X、Y、Z是三种常见元素的单质,甲乙是两种常见的化合物,这些单质和化合物之间存在如图所示的关系,下列说法正确的是 ( ) 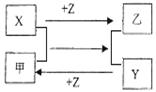
A.X、Y、Z都是非金属单质
B.X、Y、Z中至少有一种是金属单质
C.如果X、Y都为非金属单质,则Z必为金属单质
D.如果X、Y都为金属单质,则Z必为非金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
塑料是日常生活中常用的合成高分子材料,以甲烷为主要原料合成常用塑料H的线路如图:
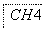
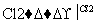
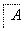
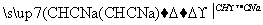
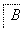
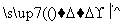
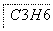
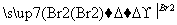
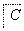
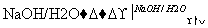
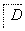
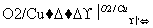

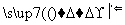
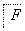
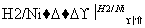
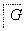
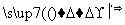
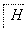
已知:CH3CH2X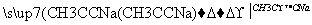 CH3CH2C≡CCH3。回答下列问题:
CH3CH2C≡CCH3。回答下列问题:
(1)反应①应控制的条件是__________________________,反应④的类型是
________________________________________________________________________;
(2)写出下列反应的化学方程式:反应
②________________________________________________________________________
________________________________________________________________________
________________________________________________________________________,
反应
⑥________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列微粒可以大量共存于同一溶液中的是( )
|
| A. | NH4+、CH3COO﹣、Ca2+、Cl﹣ | B. | Fe3+、Ag+、SO42﹣、NO3﹣ |
|
| C. | Cu2+、H+、S2﹣、NO3﹣ | D. | C6H5OH、Fe3+、K+、Cl﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某反应为:
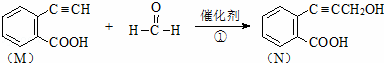
(1)1molM完全燃烧需要 9.5 molO2..
(2)有机物N不可发生的反应为 C :
A.氧化反应 B.取代反应 C.消去反应
D.还原反应 E.加成反应
(3)M有多种同分异构体,其中能使FeCl3溶液显紫色、苯环上只有两个取代基、无环物质的同分异构体有 6 种.
(4)物质N与H2反应生成的P(结构简式为)发生缩聚反应产物的结构简式为 ;P物质的钠盐在适当条件下氧化为芳香醛Q,则Q与银氨溶液发生反应的化学方程式为 .
(5)有机物Ⅰ、Ⅱ、Ⅲ的转化关系为:Ⅰ Ⅱ
Ⅱ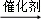 Ⅲ
Ⅲ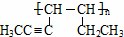
有机物Ⅱ的结构简式为 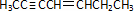 ;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为
;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为 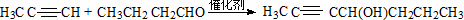 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组对离子方程式xR2+ + yH+ + O2 = mR3+ + nH2O的分析研究,下列说法中错误的是
A.根据电荷守恒,得出x与y的和一定等于m
B.根据原子守恒,得出x和m的数值一定相等
C.根据电子得失守恒,得出x=4的结论
D.根据氧化还原反应关系得出:R2+是还原剂, O2是氧化剂, R3+是氧化产物, H2O是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
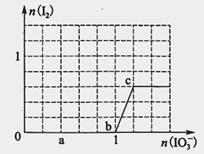
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,试回答下列问题:
(1)写出a点反应的离子方程式________________;反应中还原剂是______________;被还原的元素是__。
(2)写出b点到c点反应的离子方程式_____________________________。
(3)若往100 mL 1 mol·L-1的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中对应关系正确的是( )
| A | CH3CH3+Cl2 CH2===CH2+HCl—→CH3CH2Cl | 均为取代反应 |
| B | 由 由淀粉得到葡萄糖 | 均发生了水解反应 |
| C | Cl2+2Br-===2Cl-+Br2 Zn+Cu2+===Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O===4NaOH+O2↑ Cl2+H2O===HCl+HClO | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com