
【题目】有资料显示过量的氨气和氯气在常温下可合成岩脑砂![]() 主要成分为
主要成分为 ![]() ,某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
,某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
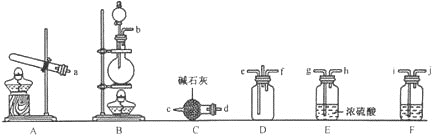
(1)岩脑砂的制备
![]() 利用装置A制取实验所需的氨气,写出反应的化学方程式:_____________。
利用装置A制取实验所需的氨气,写出反应的化学方程式:_____________。
![]() 该实验中用浓盐酸与
该实验中用浓盐酸与![]() 反应制取所需氯气,则装罝F中的试剂是
反应制取所需氯气,则装罝F中的试剂是![]() 填写试剂名称
填写试剂名称![]() ___________________。
___________________。
![]() 为了使氨气和氯气在D中充分混合,请确定上述装置的合理连接顺序:
为了使氨气和氯气在D中充分混合,请确定上述装置的合理连接顺序:![]() _____
_____![]() ________
________![]() 提示:氨气和氯气形成逆向流动,更有利于二者充分混合
提示:氨气和氯气形成逆向流动,更有利于二者充分混合![]()
![]() 证明氨气和氯气反应有岩脑砂生成,需要的检验试剂中,除了蒸馏水、稀
证明氨气和氯气反应有岩脑砂生成,需要的检验试剂中,除了蒸馏水、稀![]() 、NaOH溶液外,还需要____________________。
、NaOH溶液外,还需要____________________。
(2)岩脑砂中元素的测定
准确称取![]() 岩脑砂,与足量的氧化铜混合加热
岩脑砂,与足量的氧化铜混合加热![]() 发生的反应为
发生的反应为![]() ,利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
,利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
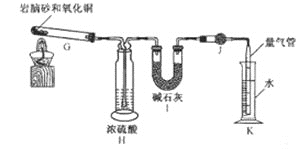
![]() 设置装置H的目的是____________________。
设置装置H的目的是____________________。
![]() 若装置Ⅰ增重
若装置Ⅰ增重 ![]() ,利用装置 K测得气体体积为
,利用装置 K测得气体体积为 ![]() 已知常温常压下气体摩尔体积为
已知常温常压下气体摩尔体积为 ![]() ,则岩脑砂中
,则岩脑砂中 ![]() _____________
_____________![]() 用含 b、V的代数式表示,不必化简
用含 b、V的代数式表示,不必化简![]() 。若测量体积时气体温度高于常温
。若测量体积时气体温度高于常温![]() 其他操作均正确
其他操作均正确![]() ,则
,则 ![]() 比正常值______________
比正常值______________![]() 填“偏高”“偏低”或“无影响”
填“偏高”“偏低”或“无影响”![]() 。
。
【答案】2NH4Cl+Ca(OH)2![]() CaCl2+2NH3+2H2O 饱和食盐水 e f
CaCl2+2NH3+2H2O 饱和食盐水 e f ![]() 溶液、红色石蕊试纸 吸收混合气体中的水蒸气,防止对测定氯化氢的质量产生影响
溶液、红色石蕊试纸 吸收混合气体中的水蒸气,防止对测定氯化氢的质量产生影响 ![]() 偏高
偏高
【解析】
(1)①装置A为制取氨气装置,氯化铵与熟石灰制取氨气;
②用饱和食盐水可除去氯气中混有的HCl,用饱和食盐水可除去氯气中混有的HCl,氯气在饱和食盐水中的溶解度较小;还可以除去氯化;
③制取干燥的气体,需要气体的发生装置,除杂装置,干燥装置,收集装置,尾气处理装置;
④检验氨与氯气反应有![]() 生成时,应检测铵根离子和氯离子,铵根离子用加入氢氧化钠后用红色石蕊试纸检验,氯离子用硝酸酸化的硝酸银溶液检验;
生成时,应检测铵根离子和氯离子,铵根离子用加入氢氧化钠后用红色石蕊试纸检验,氯离子用硝酸酸化的硝酸银溶液检验;
(2)产生的气体通过装置H中的浓硫酸,能够吸收混合气体中的水蒸气,防止对HCl测定造成干扰,减小实验误差;
②装置Ⅰ增重![]() ,即生成HCl的质量为bg,其物质的量为
,即生成HCl的质量为bg,其物质的量为![]() ;装置K测得气体体积为VL,则
;装置K测得气体体积为VL,则![]() 的物质的量为
的物质的量为![]() ,则岩脑砂中
,则岩脑砂中![]() ;测量体积时气体温度高于常温,此时气体的摩尔体积应大于
;测量体积时气体温度高于常温,此时气体的摩尔体积应大于![]() ,测定
,测定![]() 的物质的量偏大,结合原子守恒,则
的物质的量偏大,结合原子守恒,则![]() 比正常值偏高;
比正常值偏高;
(1)①装置A为制取氨气装置,故A中发生的反应方程式为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3+2H2O;
CaCl2+2NH3+2H2O;
②用饱和食盐水可除去氯气中混有的HCl,氯气在饱和食盐水中的溶解度较小;还可以除去氯化氢;
③为使氨和氯气在装置D中充分混合,根据氨和氯气的密度大小,e口通入氨气,f口通入氯气,B装置制取氯气,C装置干燥氨气,E装置干燥氯气,F装置除去氯气中的氯化氢,故连接顺序为:![]() ;
;
④检验氨与氯气反应有![]() 生成时,应检测铵根离子和氯离子,故需要的试剂为:蒸馏水、稀硝酸、红色石蕊试纸、氢氧化钠溶液、硝酸银溶液;
生成时,应检测铵根离子和氯离子,故需要的试剂为:蒸馏水、稀硝酸、红色石蕊试纸、氢氧化钠溶液、硝酸银溶液;
(2) ①产生的气体通过装置H中的浓硫酸,能够吸收混合气体中的水蒸气,防止对HCl测定造成干扰,减小实验误差;
②装置Ⅰ增重![]() ,即生成HCl的质量为bg,其物质的量为
,即生成HCl的质量为bg,其物质的量为![]() ;装置K测得气体体积为VL,则
;装置K测得气体体积为VL,则![]() 的物质的量为
的物质的量为![]() ,则岩脑砂中
,则岩脑砂中![]() ,测定
,测定![]() 的物质的量偏大,结合原子守恒,则
的物质的量偏大,结合原子守恒,则![]() 比正常值偏高。
比正常值偏高。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某同学用下列装置制备并检验Cl2的性质。下列说法正确的是
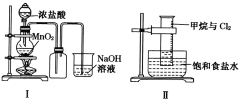
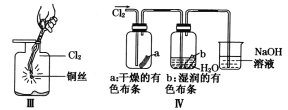
A. I图中:如果MnO2过量,浓盐酸就可全部被消耗
B. II图中:量筒中发生了加成反应
C. III图中:生成蓝色的烟
D. IV图中:湿润的有色布条能褪色将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时有关弱酸的电离平衡常数见下表:
弱酸化学式 | HA | H2B |
电离平衡常数(25 ℃) | Ka=1.7×10-6 | Ka1=1.3×10-3 Ka2=5.6×10-8 |
则下列有关说法正确的是( )
A.NaHB溶液中部分微粒浓度的大小为:c(Na+)>c(HB-)>c(B2-)>c(H2B)
B.等物质的量浓度的各溶液pH关系为:pH(Na2B)>pH(NaHB)>pH(NaA)
C.向Na2B溶液中加入足量的HA溶液发生反应的离子方程式为:B2-+2HA=2A-+H2B
D.将a mol/L的HA溶液与a mol/L的NaA溶液等体积混合,混合液中:c(Na+)>c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯![]() 是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用
是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用![]() 和NO制备ClNO并测定其纯度。请回答:
和NO制备ClNO并测定其纯度。请回答:
I.甲组的同学拟制备原料气NO和![]() ,制备装置如下图所示:
,制备装置如下图所示:
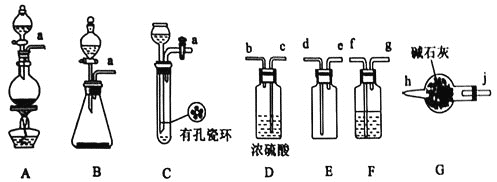
(1)若制备![]() 发生装置选B,则反应的离子方程式为_________________。若制备NO发生装置也选B,锥形瓶中放的是Cu片,则分液漏斗中的试剂为_______。
发生装置选B,则反应的离子方程式为_________________。若制备NO发生装置也选B,锥形瓶中放的是Cu片,则分液漏斗中的试剂为_______。
(2)欲收集一瓶干燥纯净的氯气,选择装置其连接顺序为:![]() ___
___![]() ___
___![]() ___
___![]() ___
___![]() ___
___![]() ___
___![]() 按气流方向,用小写字母表示
按气流方向,用小写字母表示![]() ,其中F装置的作用为________。
,其中F装置的作用为________。
II.乙组同学利用甲组制得的NO和![]() 制备NOCl,装置如图所示:
制备NOCl,装置如图所示:
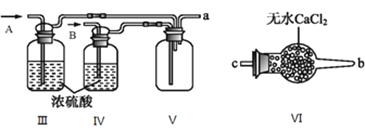
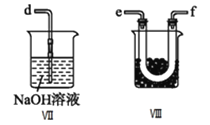
(3)为了使气体充分反应,从A处进入的气体是_______![]() 填
填![]() 或
或![]() 。
。
(4)装置Ⅲ、Ⅳ除可干燥NO、![]() 外,另一个作用是_________________。
外,另一个作用是_________________。
(5)装置Ⅷ的烧杯中盛放的试剂是______![]() 填编号:
填编号:![]() 水
水 ![]() 热水
热水 ![]() 冰水
冰水![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列叙述正确的是( )
为阿伏加德罗常数的值,下列叙述正确的是( )
A.![]() 中含有的
中含有的![]() 键数目为
键数目为![]()
B.标况下![]() 的
的![]() 分子,含共用电子对数
分子,含共用电子对数![]()
C.![]() 分别与足量的
分别与足量的![]() 和
和![]() 充分反应后转移的电子数均为
充分反应后转移的电子数均为![]()
D.![]() 的盐酸与氨水混合后溶液呈中性,则
的盐酸与氨水混合后溶液呈中性,则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,实验室里用![]() 的盐酸溶液滴定
的盐酸溶液滴定![]() 氨水溶液,若用AG表示溶液的酸度,其表达式为:
氨水溶液,若用AG表示溶液的酸度,其表达式为: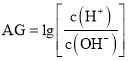 ,滴定曲线如图所示,下列说法正确的是
,滴定曲线如图所示,下列说法正确的是![]()
![]()
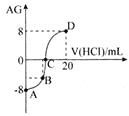
A.D点溶液中离子浓度关系为:![]()
B.C点加入盐酸的体积为10mL
C.若B点加入的盐酸溶液体积为5mL,所得溶液中:![]()
D.滴定过程中从A点到D点溶液中水的电离程度逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇能发生如下反应:
①![]() ;
;
②![]() ,
,![]() 。
。
由以上反应得出的结论错误的是( )
A.由反应①②可知,条件不同,乙醇与![]() 反应的产物不同
反应的产物不同
B.由反应②可知,![]() 是乙醇氧化生成乙醛的催化剂
是乙醇氧化生成乙醛的催化剂
C.由反应①可知,乙醇燃烧时,碳碳键、碳氢键、碳氧键 、氢氧键均断裂
D.由反应②可知,乙醇氧化为乙醛时,只断开氢氧键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_______。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是________。“滤液”中的溶质主要是_______。“调pH”中发生反应的化学方程式为__________。
(3)KIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式______。
②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有______________(写出一点)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲基丙烯酸甲酯的结构简式为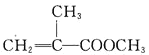 ,是有机玻璃的单体,其一种实验室制备方法如下:实验装置如图1所示(夹持装置及微波加热装置已略去):
,是有机玻璃的单体,其一种实验室制备方法如下:实验装置如图1所示(夹持装置及微波加热装置已略去):
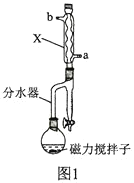
实验步骤如下:
Ⅰ![]() 量取86ml甲基丙烯酸
量取86ml甲基丙烯酸![]()
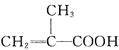
![]() 置于烧杯中,在搅拌的同时加入5ml浓硫酸,冷却至室温,再加入50ml甲醇,搅拌,混合均匀;
置于烧杯中,在搅拌的同时加入5ml浓硫酸,冷却至室温,再加入50ml甲醇,搅拌,混合均匀;
Ⅱ![]() 将混合溶液注入图1装置的反应器中,加入磁力搅拌子,微波加热温度为105℃,持续加热,充分反应;
将混合溶液注入图1装置的反应器中,加入磁力搅拌子,微波加热温度为105℃,持续加热,充分反应;
Ⅲ![]() 纯化产品,流程如图2所示:
纯化产品,流程如图2所示:
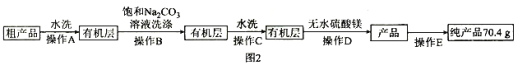
已知:
|
|
| |
溶解性 | 可溶于有机物、水 | 可溶于热水、酯 | 难溶于水、可溶于有机物 |
密度/gcm-3 | 0.79 | 1.01 | 0.94 |
沸点/℃ | 64.7 | 161 | 100~101 |
相对分子质量 | 32 | 86 | 100 |
回答下列问题:
(1)制备甲基丙烯酸甲酯的化学方程式为______________________________。
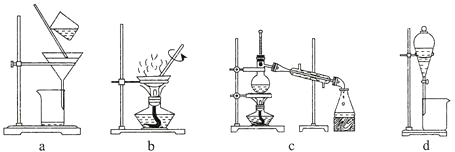
(2)图1中仪器X的名称为________________,其进水口应为________________(填“a”或“b”)口。
(3)采用微波加热可准确控制反应温度和时间,若反应温度控制不好,可能有副产物产生,写出一种有机副产物的结构简式:_________。
(4)从分水器中及时分离出水的目的是_____________________,如果分水器中的水层不再增厚,则表明__________________________。
(5)纯化过程中,用“饱和碳酸钠溶液洗涤”的目的是_______________________________;完成操作C应选____________(填选项字母,下同)装置,完成操作D应选____________装置。
(6)本实验中甲基丙烯酸甲酯的产率为_________________![]() 保留三位有效数字
保留三位有效数字![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com