
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
A.正极附近的SO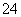 离子浓度逐渐增大
离子浓度逐渐增大
B.电子通过导线由铜片流向锌片
C.正极有O2逸出
D.铜片上有H2逸出
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
可逆反应A(g)+3B(g) 2C(g)+2D(g)在四种不同的情况下,反应速率分别为① vA=0.15mol·L-1·s-1,② vB=0.6mol·L-1·s-1,③ vC=0.4mol·L-1·s-1,④ vD=0.45mol·L-1·s-1,则以上四种情况下反应速率由小到大的排列是 ④>②=③>① 。
2C(g)+2D(g)在四种不同的情况下,反应速率分别为① vA=0.15mol·L-1·s-1,② vB=0.6mol·L-1·s-1,③ vC=0.4mol·L-1·s-1,④ vD=0.45mol·L-1·s-1,则以上四种情况下反应速率由小到大的排列是 ④>②=③>① 。
查看答案和解析>>
科目:高中化学 来源: 题型:
pH=5的氯化镁溶液中含有杂质氯化铁,为除去该杂质,可加入的试剂是( )
①MgO ②MgCO3 ③NaOH ④Na2CO3
A.①② B.②③ C.③④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入
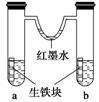
生铁块,放置一段时间。下列有关描述错误的是( )
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是Fe—→Fe2++2e-
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
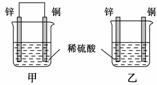
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速率甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
电子表所用纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液。其电极反应是:
Zn+2OH-—→ZnO+H2O+2e-
Ag2O+H2O+2e-—→2Ag+2OH-
总反应式为:Ag2O+Zn===2Ag+ZnO
下列判断正确的是( )
①锌为正极,Ag2O为负极
②锌为负极,Ag2O为正极
③原电池工作时,负极区溶液pH减小
④原电池工作时,负极区溶液pH增大
A.①② B.①③ C.②③ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时加水稀释10 mL pH=11的氨水,下列叙述正确的是( )
A.原氨水的浓度为10-3 mol·L-1
B.溶液中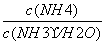 增大
增大
C.氨水的电离程度增大,溶液中所有离子的浓度均减小
D.再加入10 mL pH=3的盐酸充分反应后混合液的pH值肯定等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验不能达到预期目的的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 取少量溶液滴加Ca(OH)2溶液,观察是否出现白色浑浊 | 确定NaHCO3溶液中是否混有Na2CO3 |
| B | 向盛有1 mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 测定等浓度的HClO4、HNO3两溶液的pH | 比较氯、氮的非金属性强弱 |
| D | 将充满NO2的密闭玻璃球浸泡在热水中 | 研究温度对化学平衡移动的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分离苯和苯酚的混合物,通常采用的方法是( )
A.振荡混合物,用分液漏斗分离
B.加入NaOH溶液后振荡,用分液漏斗分离;取下层液体通入CO2,待分层后分液
C.加水振荡后用分液漏斗分离
D.加稀盐酸振荡后,用分液漏斗分离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com