
【题目】T℃时,在20.00mL0.10mol·L-1的一元酸HR溶液中滴入0.10mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。

下列说法不正确的是( )
A..T℃时,HR电离常数Ka≈1.0×10-5
B.M点对应的NaOH溶液体积为20.00mL
C.N点与Q点所示溶液中水的电离程度:N>Q
D.M点所示溶液中c(Na+)=c(R-)
【答案】B
【解析】
A.P点溶液的pH=3,则c(H+)=1×10-3mol/L,c(R-)≈c(H+),c(HR)≈0.1mol/L,则T℃时HR电离平衡常数Ka=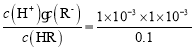 =1.0×10-5,故A正确;
=1.0×10-5,故A正确;
B.M点溶液的pH=7,则溶液呈中性,此时c(H+)= c(OH-),而HR与氢氧化钠反应完全生成的NaR溶液呈碱性,所以溶液显中性时氢氧化钠的体积应小于20ml,故B错误;
C.N点HR可能恰好完全反应,也可能氢氧化钠稍微过量,但无论何种情况,Q点溶液中氢氧化钠的浓度要大于N点,碱的电离抑制水的电离,则水的电离程度:N>Q,故C正确;
D.M点溶液中存在电荷守恒c(OH-)+c(R-)=c(H+)+(Na+),溶液显中性,则c(OH-)=c(H+),所以c(R-)=(Na+),故D正确;
故答案为B。


科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.在pH=7的溶液中:Fe3+、K+、Cl-、SO![]()
B.滴加KSCN溶液显红色的溶液中:NH![]() 、K+、Cl-、I-
、K+、Cl-、I-
C.c(OH-)/c(H+)=10-12的溶液中:NH![]() 、Cu2+、NO
、Cu2+、NO![]() 、SO
、SO![]()
D.水电离产生的c(OH-)=10-12 mol·L-1的溶液中:Na+、Al3+、Cl-、NO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】艾司洛尔(I )是预防和治疗手术期心动过速的一种药物,某合成路线如下:
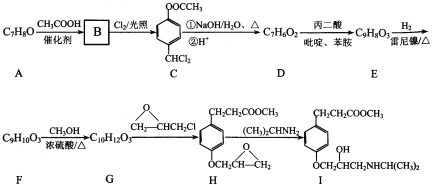
回答下列问题:
(1)A的结构简式为_____________________,D 的化学名称为__________________。
(2)G→H的反应类型为_______________,H中所含官能团的名称为______________。
(3)C→D中步骤①的化学反应方程式为_________________。
(4)已知:1 mol D 和1 mol 丙二酸在吡啶、苯胺中反应生成 1 mol E、1 mol H2O和1 molCO2,且E 能与溴水发生加成反应,则 E 的结构简式为 ____________。
(5)X是F的同分异构体,写出满足下列条件的 X 的结构简式________。①与碳酸氢钠溶液反应生成二氧化碳②与FeC13溶液发生显色反应③核磁共振氢谱有四组峰且峰面积之比为 6 : 2 : 1 : 1
(6)参照上述合成路线,设计以![]() 和
和![]() 为主要原料制备
为主要原料制备![]() 的合成路线______。
的合成路线______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂碘电池的正极材料是聚2-乙烯吡啶(简写为P2VP)和I2的复合物,电解质是熔融薄膜状的碘化锂,该电池发生的总反应为2Li+P2VP·nI2![]() P2VP·(n-1)I2+2LiI。下列说法正确的是 ( )
P2VP·(n-1)I2+2LiI。下列说法正确的是 ( )
A.该电池放电时,锂电极发生还原反应
B.该电池放电时,碘离子移向正极
C.P2VP和I2的复合物是绝缘体,不能导电,充电时与外电源的负极相连
D.放电时正极的电极反应式为P2VP·nI2+2e-+2Li+=P2VP·(n-1)I2+2LiI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g)2NH3(g)ΔH<0,下列各项能说明该反应已经达到平衡状态的是______
A.容器内气体密度保持不变
B.容器内温度不再变化
C.断裂1mol![]() 键的同时,生成6molN-H键
键的同时,生成6molN-H键
D.反应消耗N2、H2与产生NH3的速率之比1:3:2
(2)已知:①Zn(s)+1/2O2(g)=ZnO(s) △H=-348.3kJ·mol-1
②2Ag(s)+1/2O2(g)=Ag2O(s)△H=-31.0kJ·mol-1
则 Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s)的△H=_____kJ·mol-1
(3)已知两个热化学方程式
C(s)+O2(g)=CO2(g)△H=-393.5 kJ·mol-1
2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ·mol-1
现有0.2mol炭粉和H2组成悬浮气,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间的变化如图所示,如图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间的变化如图所示,如图可得出的正确结论是
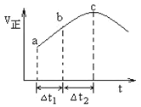
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量高于生成物的总能量
D.Δt1=Δt2时,SO2的转化率:a~b段大于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气因含有少量H2S等气体开采应用受限,TF菌在酸性溶液中可实现天然气的催化脱硫,其原理图如图所示。
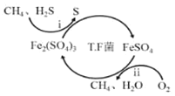
(1)写出涉及铁化合物的两个离子方程式:___;___。
(2)25℃时,向0.1mol·L-1的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,从平衡移动的角度解释主要原因是:___。
(3)室温下,如果将0.2molNH4Cl、0.1molNaOH全部溶于水,形成混合溶液(假设无损失)
①___和___两种粒子的物质的量之和等于0.2mol。
②___和____两种子的物质的量之和比OH-多0.1mol。
(4)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能如下四种关系。
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)=c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是__,上述离子浓度大小序中正确的是__(选填序号)。
②若上述关系中C是正确的,则该溶质的化学式是__。
③若该溶液是由体积相等的稀盐酸和氮永混含而成,且恰好呈中性,则混合前c(HCl)__(填“>”“<”或“=”,下同)c(NH3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)___c(Cl-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.01mol/L的这四种溶液pH与该元素原子半径的关系如下图所示。下列说法正确的是

A. 简单离子半径: X>Y>Z>W
B. W的单质在常温下是黄绿色气体
C. 气态氢化物的稳定性: Z>W>Y
D. X和Y的最高价氧化物对应的水化物恰好中和时,溶液中的微粒共有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com