
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在漂白液(次氯酸钠溶液)中:Ag+、K+、NO3-、SO32-
B.中性溶液:K+、NO3-、Br-、Fe3+
C.![]() =1012的溶液中,NH4+、Ca2+、Cl-、NO3-
=1012的溶液中,NH4+、Ca2+、Cl-、NO3-
D.由水电离的c(H+)=1×10-10mol/L的溶液中:K+、Na+、HCO3-、Al3+
科目:高中化学 来源: 题型:
【题目】图中是在实验室进行氨气快速制备与性质探究实验的组合装置,部分固定装置未画出。

(1)在组装好装置后,若要检验A~E装置的气密性,其操作是:首先______________,打开弹簧夹1,在E中装入水,然后微热A,观察到E中有气泡冒出,移开酒精灯,E中导管有水柱形成,说明装置气密性良好。
(2)装置B中盛放的试剂是______________________。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹1,从分液漏斗放出浓氨水至浸没烧瓶中固体后,关闭分液漏斗活塞,稍等片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时产生_____________(填现象)。从E中逸出液面的气体可以直接排入空气,写出C中反应的化学方程式:_______。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16 g,反应后固体质量减少2.4 g,通过计算确定该固体产物的化学式:______。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。写出产生白烟的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示800℃时,X、Y、Z三种气体物质的浓度随时间变化的情况.试回答:(保留一位小数)

(1)该反应的反应物为 ______ ;
(2)该反应的化学方程式为 ______ ;
(3)0~2minY物质的化学反应速率为 ______ ;
(4)Z物质的平衡转化率为 ______ ;
(5)800℃时,该反应的平衡常数K= ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫的催化氧化原理为2SO2(g)+O2(g)![]() 2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
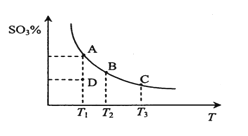
A. 反应2SO2(g)+O2(g)![]() 2SO3(g)的△H<0
2SO3(g)的△H<0
B. 在D点时v(正)<v(逆)
C. 若B、C点的平衡常数分别为KB、KC,则KB>KC
D. 恒温恒压下向平衡体系中通入氦气,平衡向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中![]() 和3mol
和3mol![]() 发生反应:
发生反应:![]()
![]()
![]() 。下列有关说法正确的是
。下列有关说法正确的是
A.降低温度可以加快反应速率
B.向容器中再加入![]() 可以加快反应速率
可以加快反应速率
C.达到化学反应限度时,生成2mol![]()
D.达到化学平衡时![]() 、
、![]() 、
、![]() 的物质的量之比为1:3:2
的物质的量之比为1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年10月9日,瑞典皇家科学院将诺贝尔化学奖授予古迪纳夫等三位科学家,表彰他们在锂离子电池方面的研究成果,钴酸锂电池是他们的研究成果之一,其工作原理为LixC6+Li1-xCoO2![]() C6+LiCoO2。下列说法正确的是
C6+LiCoO2。下列说法正确的是
A.放电时Li+从正极通过导线流向负极
B.放电时负极的电极反应式为:LixC6-xe-=C6+xLi+
C.充电时电池的负极与电源的正极相连
D.充电时阴极的电极反应式为:LiCoO2-xe-=Li1-xCoO2+xLi+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,若Ca(OH)2和CaWO4(钨酸钙)的沉淀溶解平衡曲线如图所示(已知![]() =0.58)。下列分析不正确的是
=0.58)。下列分析不正确的是

A. a点表示Ca(OH)2与CaWO4均未达到溶解平衡状态
B. 饱和Ca(OH)2溶液和饱和CaWO4溶液等体积混合: c(OH-)>c(H+)>c(Ca2+)>c(WO42-)
C. 饱和Ca(OH)2溶液中加入少量Na2O,溶液变浑浊
D. 石灰乳与0.1mol/LNa2WO4溶液混合后发生反应:Ca(OH)2+WO42-=CaWO4+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.浓度均为0.1 molL-1的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-)
B.pH相同的盐酸和硫酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH相等,则m>n
C.常温下,0.1 molL-1某一元酸HA在水中有0.1%发生电离,则该温度下HA的电离常数约为10-7
D.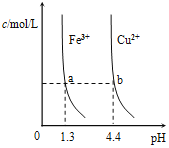 某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某2 L恒容密团容器中充入2 mol X(g)和1mol Y(g)发生反应:2X(g)+ Y(g)![]() 3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是( )
3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是( )

A.Q点时,Y的转化率最大
B.升高温度,平衡常数增大
C.W点Y的正反应速率等于M点Y的正反应速率
D.平衡时充入Y,达到新平衡时Y的体积分数比原平衡时小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com