
【题目】实验室配制氯化亚铁溶液时,为了防止其氧化,常加入的物质是
A.Zn B. Fe C.Al D.HCl
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于2L恒容密闭容器中,发生如下反应:3A(g) + B(g)![]() xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
A. A的转化率为40%
B. 2 min内B的反应速率为0.2 mol.L-l.min-1
C. x=2
D. 若混合气体的密度不变,则表明该反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧的烟气中含有SO2和NO,直接排放会形成酸雨、污染大气,因此对烟气进行脱硫、脱硝具有重要意义。
(1)选择性催化还原技术是目前成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NO反应生成N2和H2O。
①已知:4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g) ΔH = -905.5kJ/mol
4NO(g) + 6H2O(g) ΔH = -905.5kJ/mol
N2(g) + O2(g) ![]() 2NO(g) ΔH =+180 kJ/mol
2NO(g) ΔH =+180 kJ/mol
则该方法中主要反应的热化学方程式是(请补充完整):
4NH3(g) + 4NO(g) + O2(g)![]() 4N2(g) + 6H2O(g) ΔH =_________
4N2(g) + 6H2O(g) ΔH =_________
②该方法控制反应温度在315~400℃之间,反应不宜过低也不能过高的原因是_________。
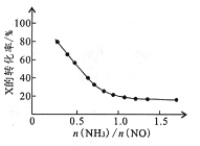
③氨氮比[n(NH3)/n(NO)]的大小会影响该方法的脱硝率。350℃时,只改变NH3的投放量,反应物X的转化率与氨氮比的关系如右图,则X是_____(填化学式)。氨氮比由0.5增加到1.0时,脱硝主要反应的平衡将向____________方向移动。当氨氮比大于1.0时,烟气中NO浓度反而增大,主要原因是___________。
(2)将烟气中的SO2、NO经O3处理后,再用CaSO3悬浊液吸收,可脱硫、脱硝。
已知:O3氧化烟气中SO2、NO的主要反应为:
NO + O3![]() NO2 + O2; 2NO + O2
NO2 + O2; 2NO + O2![]() 2NO2; SO2+ O3
2NO2; SO2+ O3![]() SO3 + O2
SO3 + O2
用CaSO3悬浊液(pH=8)吸收经O3处理后的烟气时,NO2转化为NO2-,离子方程式为
_____________。
② 在CaSO3悬浊液中加入Na2SO4溶液可提高NO2的吸收速率,请结合化学原理进行解释___________________________。
③烟气经处理后最终得到含Na+、NO2-、SO42-的吸收液。t℃时,向吸收液中加入AgNO3溶液至SO42-恰好完全沉淀(即SO42-浓度等于1.0×10-5 mol·L-1)时,c(NO2-)=_______mol/L。[t℃时,AgNO2(亚硝酸银)的 Ksp= 9.0×10-4、Ag2SO4的Ksp=4.0×10-5。]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,5-二甲氧基苯酚是重要的有机合成中间体,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33 ~36 |
| 易溶于甲醇、乙醚,微溶于水 |
(1)1mol间苯三酚完全燃烧需要______molO2。
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是的__________。
②萃取用到的分液漏斗使用前需____________并洗净,分液时有机层在分液漏斗的______填(“上”或“下”)层。
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是_________________________________________ ;
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____________(填字母)。
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)反应可能出现的副产物的结构简式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于铁及其化合物的叙述正确的是
A.铁是一种较活泼的金属 B.Fe2O3在常温下可以导电
C.Fe2O3溶于水生成Fe(OH)3 D.在常温下铁丝容易与水反应放出H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国药学家屠呦呦因发现青蒿素治疗疟疾新方法而获得2015年诺贝尔生理学奖。这是中国本土培养的科学家首次获得诺贝尔奖。请回答下列有关问题:
(1)青蒿素的分子式为C15H22O5,其组成中的三种元素的电负性有大大小排序是_______,其中第一电离能最大元素基态原子的核外电子排布式为______________。
(2)在确定青蒿素结构的过程中,可采用KBH4作为还原剂,其制备流程如下:

①已知金属晶体Na的配位数为8,则其晶胞结构图符合图1的_____________(选填字母编号),其堆积方式为_______(填名称)

②图2是NaH的晶胞结构,则NaH晶胞中Na+的数目为_________,若该晶体密度为ρg·cm-3,则晶胞中相距最近的两个Na+间的距离为________cm(用含ρ、NA的代数式表示)。
③化合物B(OCH3)3中C的杂化轨道类型为________,B(OCH3)3的空间构型为________,与其具有相同空间构型的分子和离子有________、_________(分子或离职各写一种)。
④KBH4的电子式__________,晶体结构中存在的作用力有______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对相应有机物的描述不正确的是( )
A. 甲烷:天然气的主要成分,能发生取代反应
B. 乙烯:一个国家石油化工发展水平的标志,可以发生加成反应
C. 苯:平面结构,每个分子中含有3个碳碳双键
D. 淀粉:属于糖类物质,遇碘单质变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列关于溶液的说法不正确的是
①加水稀释FeCl3溶液,c(Fe3+)/c(Cl-)的值减小
②浓度均为0.1 mol·L-l的Na2CO3和Na2HCO3的混合溶液中:2c(Na+)=3[c(CO32- )+c(HCO3-)]
③向0.1 mol/L的氨水中滴加等浓度的盐酸,恰好中和时溶液的pH=a,则溶液中由水电离产生的c(OH-) = 10-amol·L-1
④pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合.反应后所得溶液中: c(CH3COOH)>c(CH3COO-)>c(Na+)
⑤Na2S 稀溶液中:c(OH-) =c(H+)+c( H2S)+c( HS-)
A. ②⑤ B. ①②⑤ C. ②③④⑤ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如下:
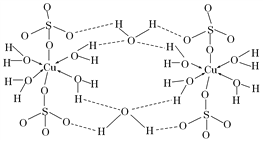
下列说法正确的是
A. 在上述结构示意图中,所有氧原子都采用sp3杂化
B. 在上述结构示意图中,存在配位键、共价键和离子键
C. 胆矾是分子晶体,分子间存在氢键
D. 胆矾中的结晶水,加热时不会分步失去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com