
【题目】从1.0 mol·L-1氢氧化钠溶液中取出100 mL,则这100 mL氢氧化钠溶液:
(1)物质的量浓度是________;
(2)所含氢氧化钠的质量是______。
科目:高中化学 来源: 题型:
【题目】烟气中SO2和NOx(NO及NO2)的脱除对于环境保护意义重大。
(1)湿式氨法烟气脱硫脱氮是通过氨水吸收烟气,得到含![]() 、
、![]() 、
、![]() 、
、![]() 和NO2的吸收液。
和NO2的吸收液。
①用离子方程式解释吸收液中含有![]() 的原因:_____________;
的原因:_____________;
②吸收液中的![]() 、
、![]() 均对NO2具有吸收作用,但
均对NO2具有吸收作用,但![]() 对NO2的吸收能力比
对NO2的吸收能力比![]() 弱,
弱,![]() 与NO2反应生成
与NO2反应生成![]() 的离子方程式是:___________;
的离子方程式是:___________;
(2)经测定,在烟气的吸收过程中,吸收液对NO2的吸收率随烟气通入量变化的曲线如下图所示。

结合化学用语解释产生上述结果的原因:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,△H1=-393.5 kJmol-1,△H2=-395.4 kJmol-1,下列说法或表示式正确的是( )

A. C(s、石墨)==C(s、金刚石)△H=+1.9kJmol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用一定浓度的盐酸滴定某浓度的氨水。滴定终点附近溶液的pH和导电能力的变化如图所示(利用溶液导电能力的变化可判断滴定终点,溶液总体积变化忽略不计)。下列说法错误的是( )

A.a点对应的溶液中:![]()
B.a→b过程中,![]() 不断增大
不断增大
C.c→d溶液导电性增强的主要原因是![]() 和
和![]() 增大
增大
D.根据溶液pH和导电能力的变化可判断:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(![]() )常用于晒制蓝图。某研究性学习小组对其进行了系列探究。
)常用于晒制蓝图。某研究性学习小组对其进行了系列探究。
I.纯净的草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究,小组成员采用如下装置(可重复选用)进行实验:

①E中盛装碱石灰的仪器名称为__________________。
②按照气流从左到右的方向,上述装置的接口顺序为![]() ___________尾气处理装置。
___________尾气处理装置。
③实验前先通入一段时间![]() ,其目的是________________________。
,其目的是________________________。
④实验证明气体产物中含有![]() ,依据的实验现象为_________________________________。
,依据的实验现象为_________________________________。
(2)![]() 受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,![]() 晶体受热分解的化学方程式_________________________。
晶体受热分解的化学方程式_________________________。

(3)晒制蓝图时,以![]() 溶液为显色剂,写出
溶液为显色剂,写出![]() 与
与![]() 溶液反应的化学方程式____________。
溶液反应的化学方程式____________。
Ⅱ.草酸亚铁晶体样品纯度的测定
(4)工业制得的草酸亚铁晶体中常含有![]() 杂质测定其纯度的步骤如下:
杂质测定其纯度的步骤如下:
步骤1:称取![]() 草酸亚铁晶体样品溶于稀
草酸亚铁晶体样品溶于稀![]() 中,配成
中,配成![]() 溶液;
溶液;
步骤2:取上述溶液![]() ,用
,用![]() ,标准液滴定至终点消耗标准液
,标准液滴定至终点消耗标准液![]() ;
;
步骤3:向反应后溶液中加入适量锌粉充分反应后加人适量稀![]() ,再用
,再用![]() 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液![]()
①步骤2中滴定终点的现象为_______________,,步骤3中加入锌粉的目的是__________________。
②草酸亚铁晶体样品的纯度为_________________(写出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气相条件下,立方烷能自发地发生热重排反应生成一系列化合物。下列说法正确的是
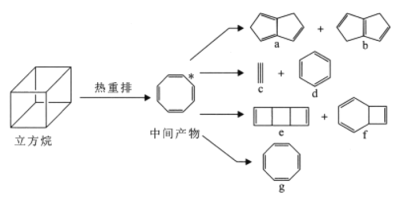
A.a、f中所有原子均可处于同一平面
B.1mol化合物e完全燃烧消耗12molO2
C.六硝基立方烷最多有3种结构(不考虑立体异构)
D.立方烷热重排产物均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】他米巴罗汀是一种对白血病、阿尔茨海默症等疾病具有较好治疗效果的药物,其一种合成路线:
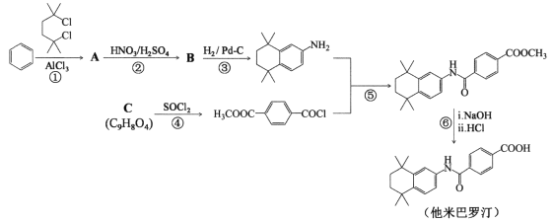
回答下列问题:
(1)A的结构简式是_________,C中含氧官能团的名称是_________
(2)①和③的反应类型分别是_________
(3)下列说法正确的是_________(填标号)。
a.A为苯的同系物b.B的一氯代物有5种
c.1molC最多可与2molNaOH反应d.弱碱性条件有利于反应⑤进行
(4)草酰氯![]() 与乙二胺(
与乙二胺(![]() )反应可得到一种六元环状化合物,该反应的化学方程式为_________
)反应可得到一种六元环状化合物,该反应的化学方程式为_________
(5)化合物W与C互为同分异构体,且满足下列条件:①属于芳香族化合物且能与NaHCO3反应:②能发生银镜反应;③酸性条件下可发生水解反应,其产物能之一与FeCl3发生显色反应,则W共有_________种,其中一种核磁共振氢谱为1:2:2:2:1,其结构简式为__________。
(6)参照上述合成路线,设计由苯和1,3-丁二烯合成![]() 的路线(其它无机试剂任选)。__________
的路线(其它无机试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应N2 +3H2![]() 2NH3 △H<0,达到平衡后,当单独改变下述条件时,有关叙述错误的是
2NH3 △H<0,达到平衡后,当单独改变下述条件时,有关叙述错误的是
A.加催化剂,υ正、υ逆都发生变化,且变化的倍数相等
B.加压,υ正、υ逆都增大,且υ正增大的倍数大于υ逆增大的倍数
C.降温,υ正、υ逆都减小,且υ正减小的倍数小于υ逆减小的倍数
D.增大氮气的浓度,υ正、υ逆都增大,且υ正增大倍数大于υ逆增大倍数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下表:
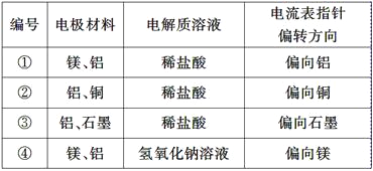
试根据表中的实验现象完成下列问题:
(1)实验①、②中铝所作的电极(指正极或负极)________(填“相同”或“不相同”)。
(2)实验③中铝为________极,电极反应式为_________________________________________;石墨为________极,电极反应式为______________;电池总反应式为____________________。
(3)实验④中铝作负极还是正极?____________,理由是_________________________,铝电极的电极反应式为__________________________________________________________。
(4)根据实验结果总结出影响铝在原电池中作正极或负极的因素为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com