
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| 高温 |
| ||
| 高温 |
| 4 |
| 7 |
| ||
| 高温 |
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:2010年重庆市南开中学高三10月月考(理综)化学部分 题型:填空题
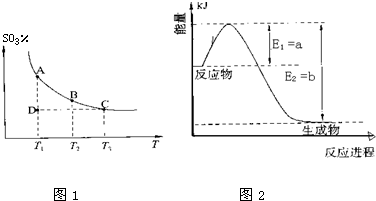
(14分)在密闭容器中进行如下反应:3m A(g)+m B(g) n C(g)+q D(s)。
n C(g)+q D(s)。
(一)
(1)若在起始容积相等的两个体积可变的容器中,充入物质的量相等的反应物(反应过程中保持体系的温度不变),建立如图所示的平衡,则由图可知:P1 P2(填“>”、“<”或“=”);m与n之间的关系为: (用含m的代数式表示n)。
(2)对(1)的反应而言,下列能够判断反应已达化学平衡状态的有 。
A.气体总的物质的量不变 B.固体D的物质的量一定
C.气体的密度不变 D.当气体A与B的物质的量之比为3:1时
E.气体A的浓度不变 F.反应速率v (A)=3m/nv(C)
(3)在一定的温度和压强下,将3moIA和1moIB充入体积可变的容器,达到平衡时,B的物质的量浓度为amol/L.现持续增大压强,有:
①当压强为平衡时的2.5倍时,B平衡时的物质的量浓度为C1 mol/L,测得C1=-2.5a;
②当压强为平衡时的10倍时, B平衡时的物质的量浓度为C2mol/L,测得C2= 5.5a;
试分析造成第②种结果的可能原因: 。
(二)若m=n=q,且保持原容器的体积不变,在一定温度下,将3molA和1mnolB充入该容器中,平衡时容器中B的转化率为W%。
(4)若在体积和温度不变的条件下,仅从生成物开始配料,要达到上述等数,则D的起始物质的量n(D)应满足的条件是____ (用含有W%的代数式表示,下同),平衡时C的转化率为 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年陕西省西安市高三第三次质检(理综)化学部分 题型:填空题
在元素周期表中处于相邻位置的元素在结构和性质上有许多相似的地方。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H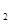 O外,还有H
O外,还有H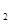 O
O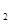 ;碳元素的氢化物除CH
;碳元素的氢化物除CH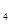 外,还有C
外,还有C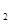 H
H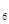 等;与之相似的氮元素的氢化物除外,还有N
等;与之相似的氮元素的氢化物除外,还有N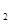 H
H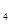 等。
等。
(1)碳原子之间可以结合成链状结构,氮原子之间也可以形成链状结构,假设氮原子间只以氮氮单键形式连接成链状,并形成氢化物,则该系列氢化物的通式为 。
(2)该系列中的N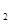 H
H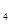 是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N
是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N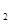 H
H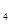 在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式:
。
在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式:
。
(3)该系列物中的NH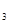 对农业、化学、国防工业具有重要意义。其合成原理为:
对农业、化学、国防工业具有重要意义。其合成原理为:
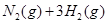

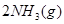
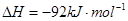
I.在一定温度下,将1.5molN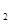 和6 molH
和6 molH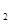 通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
此时反应放出的热量为 kJ.
H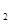 的转化率= 。
的转化率= 。
该温度下合成氨反应的平衡常数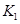 =
(只列数字表达式)
=
(只列数字表达式)
II.在保持温度不变,相同体积的密闭容器中,将起始的物质的量改为amolN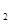 、bmolH
、bmolH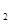 、cmolNH
、cmolNH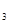 ,平衡时NH
,平衡时NH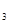 的物质的量分数为25%,则:
的物质的量分数为25%,则:
达到平衡时,I和II放出的热量 (填字母代号)
A。一定相等
B。前者一定小于后者
C。前者等于或小于后者
D。前者等于或大于后者
I和II合成氨的平衡常数分别为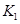 和
和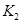 ,同
,同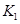
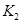 (填“﹥”、“﹤”或
“=”)
(填“﹥”、“﹤”或
“=”)
欲使开始时反应正向进行,a的取值范围为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应:3m A(g)+m B(g)![]() n C(g)+q D(s)。
n C(g)+q D(s)。

(一)
(1)若在起始容积相等的两个体积可变的容器中,充入物质的量相等的反应物(反应过程中保持体系的温度不变),建立如图所示的平衡,则由图可知:P1 P2(填“>”、“<”或“=”);m与n之间的关系为: (用含m的代数式表示n)。
(2)对(1)的反应而言,下列能够判断反应已达化学平衡状态的有 。
A.气体总的物质的量不变 B.固体D的物质的量一定
C.气体的密度不变 D.当气体A与B的物质的量之比为3:1时
E.气体A的浓度不变 F.反应速率v (A)=3m/nv(C)
(3)在一定的温度和压强下,将3moIA和1moIB充入体积可变的容器,达到平衡时,B的物质的量浓度为amol/L.现持续增大压强,有:
①当压强为平衡时的2.5倍时,B平衡时的物质的量浓度为C1 mol/L,测得C1=-2.5a;
②当压强为平衡时的10倍时, B平衡时的物质的量浓度为C2mol/L,测得C2= 5.5a;
试分析造成第②种结果的可能原因: 。
(二)若m=n=q,且保持原容器的体积不变,在一定温度下,将3molA和1mnolB充入该容器中,平衡时容器中B的转化率为W%。
(4)若在体积和温度不变的条件下,仅从生成物开始配料,要达到上述等数,则D的起始物质的量n(D)应满足的条件是____ (用含有W%的代数式表示,下同),平衡时C的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com