
【题目】实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤并转移
⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为____________________。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、______________。
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为________ g,要完成本实验该同学应称出________ g NaOH。
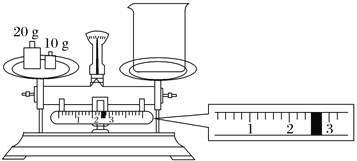
(3)使用容量瓶前必须进行的一步操作是____________________________________________。
(4)在配制过程中,其它操作都是正确的(按烧杯的实际质量),下列操作会引起误差偏低的是________。
A.转移溶液时不慎有少量洒到容量瓶外面
B.定容后塞上瓶塞反复倒转摇匀,静置后,液面低于刻度线,再加水至刻度线
C.称量时药品和砝码位置放反
【答案】 ②①③⑧⑤⑥⑨⑦④ 250 mL容量瓶、胶头滴管 27.4 10.0 检漏 ABC
【解析】(1)实验室中没有240mL的容量瓶,配制时需要选用250mL的容量瓶,配制250mL1.0mol/L的NaOH溶液的步骤为:计算→称量→溶解、冷却→移液→定容→摇匀→装瓶→贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,所以正确的操作顺序为:②①③⑧⑤⑥⑨⑦④;需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,还缺少250mL容量瓶、胶头滴管;(2)根据图示可知,游码的读数为2.6g,结合托盘天平的称量原理可知,图示中,砝码质量=烧杯质量+游码质量,所以烧杯质量=砝码质量-游码质量=20g+10g-2.6g=27.4g;配制250mL1.0mol/L的NaOH溶液,需要氢氧化钠的质量为:0.25L×1mol/L×40g/mol=10.0g;(3)容量瓶有瓶塞,配制过程中需要摇匀,为了避免液体流出,配制溶液之前需要检查此容量瓶是否漏水;(4)A、转移溶液时不慎有少量洒到容量瓶外面,导致配制的溶液中溶质的物质的量偏小,溶液浓度偏低,B、定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致配制的溶液体积偏大,溶液浓度偏低;C、称量时药品和砝码位置放反,由于需要游码所以实际称量的固体质量偏少,溶液浓度偏低,答案选ABC。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】如图表示人体细胞中各种化合物或主要元素占细胞鲜重的含量,以下按①②③④顺序排列正确的是( )
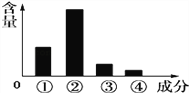
A. 蛋白质、水、脂质、糖类,C、O、H、N
B. 蛋白质、水、脂质、糖类,N、H、O、C
C. 水、蛋白质、脂质、糖类,H、O、N、C
D. 水、蛋白质、糖类、脂质,N、H、C、O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据以下背景资料,回答下列问题:
Ⅰ、不锈钢以其优异的抗腐蚀性能越来越受到人们的靑睐,它主要是由铁、铬、镍、铜、碳等元索所组成的合金。
Ⅱ、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。
Ⅲ、砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。
Ⅳ、K2Cr2O7曾用于检测司机是否酒后驾驶:
Cr2O72-(橙色)+CH3CH2OH![]() Cr3+(绿色)+CH3COOH (未配平)
Cr3+(绿色)+CH3COOH (未配平)
(1)镍元素基态原子的电子排布式为_________________。
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为___________,碳原子的轨道杂化类型为_________,所含σ键与π键的数目之比为______________________。
(3)AsCl3分子的立体构型为_____________,铁原子中有_________个未成对电子。
(4)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的原子是_____。
(5)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因____________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(6)某镍白铜合金的立方晶胞结构如图所示。
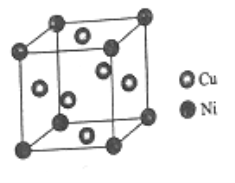
①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,有①0.112L水;②3.01×1023个氯化氢分子;③13.6gH2S气体;④0.2mol氨气。下列对这四种物质的关系由小到大排列正确的是( )
A. 氢原子数:①③④② B. 密度:④①③②
C. 质量:①④③② D. 体积:①④③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,将充有等体积混合而成的四组气体:①NO2+O2;②NO2+NO;③HCl+N2;④SO2+O2,分别通入体积相同的试管,并立即倒立于水槽中,如图所示,待试管内液面稳定后,剩余气体体积依次V1、V2、V3、V4,则剩余气体体积最多的是( )

A. V1 B. V2 C. V3 D. V4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应的化学实验,能达到相应的实验目的的是(有的夹持装置未画出)

A. 装置甲向左推动针筒活塞可检验该装置的气密性
B. 用装置乙进行喷泉实验
C. 用图丙所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验
D. 用图丁所示装置加热AlCl3饱和溶液然后利用余热蒸干制备AlCl3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离可达到平衡:H2O![]() H++OH- △H>0,下列叙述正确的是
H++OH- △H>0,下列叙述正确的是
A. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
B. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D. 将水加热,Kw增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个化学过程的示意图。
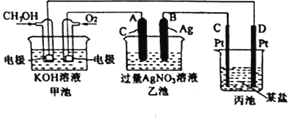
(1)C(Pt)电极的名称是__________。
(2)写出通入O2的电极上的电极反应式_______________________。
(3)写出通入CH3OH的电极上的电极反应式________________________。
(4)若丙池是电解饱和食盐水溶液,则阳极的电极反应为________________________。
(5)写出乙池中反应的化学方程式________________________。
(6)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2_________mL(标准状况下);若丙池中饱和食盐水溶液的体枳为500 mL,电解后,溶液的pH=________。(25℃,假设电解前后溶液的体积无变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量的蔗糖(C12H22O11)放入烧杯,滴入几滴水,搅拌均匀,然后加入适量的浓硫酸。可观察到固体变黑,片刻后,黑色物质急剧膨胀,同时产生大量刺激性气味的气体,放出大量的热。(如下图所示)

(1)固体变黑体现了浓硫酸的______性(填“吸水”、“脱水”或“强氧化”)。
(2)确定刺激性气味气体的成分。
① 将气体通入品红溶液后,溶液褪色,加热,颜色恢复。说明该气体中一定含有______。
② 将气体通入澄清石灰水,溶液变浑浊,______(填“能”或 “不能”)证明气体中含有二氧化碳,其理由是______。
③ 刺激性气味气体产生的原因可用如下化学方程式表示,完成化学方程式:
C+2H2SO4(浓) ![]() ______。
______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com