
【题目】一种工业制备SrCl6H2O的生产 流程如下:
已知:①M(SrCl26H2O)=267g/mol;
②Ksp(SrSO4)=3.3×10﹣7、Ksp(BaSO4)=1.1×10﹣10;
③经盐酸浸取后,溶液中除含有Sr2+和Cl﹣外,还含有少量Ba2+杂质.
(1)隔绝空气高温焙烧,若2mol SrSO4中只有S被还原,转移了16mol电子.写出该反应的化学方程式: .
(2)过滤2后还需进行的两步操作是、 .
(3)加入硫酸的目的是;为了提高原料的利用率,滤液中Sr2+的浓度应不高于 mol/L(注:此时滤液中Ba2+浓度为1×10﹣5 mol/L).
(4)产品纯度检测:称取1.000g产品溶解于适量水中,向其中加入含AgNO31.100×10﹣2 mol的AgNO3溶液(溶液中除Cl﹣外,不含其它与Ag+反应的离子),待Cl﹣完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000mol/L的NH4SCN标准溶液滴定剩余的AgNO3 , 使剩余的Ag+ 以AgSCN白色沉淀的形式析出.
①滴定反应达到终点的现象是 .
②若滴定过程用去上述浓度的NH4SCN溶液20.00mL,则产品中SrCl26H2O的质量百分含量为(保留4位有效数字).
【答案】
(1)SrSO4+4C ![]() SrS+4CO↑
SrS+4CO↑
(2)洗涤,干燥
(3)除去溶液中Ba2+杂质,0.03
(4)溶液由无色变为血红色,且30 s不褪色,93.45%
【解析】解:(1)SrSO4和碳隔绝空气高温焙烧,C发生氧化反应生成CO,设S元素在还原产物中化合价为x,根据电子转移守恒,则6mol×(6﹣x)=16mol,解得x=﹣2,故还原产物为CrS,反应方程式为:SrSO4+4C ![]() SrS+4CO↑,
SrS+4CO↑,
所以答案是:SrSO4+4C ![]() SrS+4CO↑;
SrS+4CO↑;
(2)将溶液蒸发浓缩、冷却结晶,然后从溶液中将晶体过滤出来,洗涤除去表面的杂质离子并进行干燥即获得SrCl26H2O,
所以答案是:洗涤、干燥;
(3)经盐酸浸取后的溶液中含有少量Ba2+杂质,加入硫酸的目的是除去溶液中Ba2+杂质,
由于在Ba2+浓度为1×10﹣5 mol/L,BaSO4的溶度积常数为1.1×10﹣10,所以c(SO42﹣)= ![]() mol/L=1.1×10﹣5mol/L,而SrSO4的溶度积常数为3.3×10﹣7,所以c(Sr2+)=
mol/L=1.1×10﹣5mol/L,而SrSO4的溶度积常数为3.3×10﹣7,所以c(Sr2+)= ![]() mol/L=0.03mol/L,
mol/L=0.03mol/L,
所以答案是:除去溶液中Ba2+杂质;0.03;
(4)①Ag+ 完全以AgSCN白色沉淀的形式析出后,再滴加KSCN溶液,就会与Fe3+产生络合物是溶液变为红色,因此滴定达到终点时溶液由无色变为血红色,且30 s不褪色,
所以答案是:溶液由无色变为血红色,且30 s不褪色;
②n(NH4SCN)=0.2000mol/L×0.02L=4.0×10﹣3mol,Ag+以AgSCN白色沉淀的形式析出,所以溶液中剩余的Ag+的物质的量为:n(Ag+)=4.0×10﹣3mol,则与Cl﹣反应的Ag+的物质的量为:n(Ag+)=1.100×10﹣2 mol﹣4.0×10﹣3mol=7.0×10﹣3mol,
1.000g产品中SrCl26H2O的物质的量为:n(SrCl26H2O)= ![]() ×n(Ag+)=3.5×10﹣3mol,
×n(Ag+)=3.5×10﹣3mol,
1.000g产品中SrCl26H2O的质量为:m(SrCl26H2O)=3.5×10﹣3mol×267 g/mol=0.9345g,
所以产品纯度为: ![]() ×100%=93.45%,
×100%=93.45%,
所以答案是:93.45%.


科目:高中化学 来源: 题型:
【题目】有机物F是有机合成工业中一种重要的中间体.以甲苯和丙烯为起始原料合成F的工艺流程如图: 
回答下列问题:
(1)化合物B中含氧官能团名称是F的结构简式
(2)写出C与银氨溶液共热的化学反应方程式:
(3)化合物D不能发生的反应有(填序号). ①加成反应 ②取代反应 ③消去反应 ④氧化反应 ⑤水解反应
(4)B的含苯环结构的同分异构体还有种,其中一种的核磁共振氢谱中出现4个峰且不与FeCl3溶液发生显色反应的是(填结构简式).
(5)B与D发生反应的类型 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的叙述中,正确的是
A. HCl电离产生H+和Cl-,可判断HCl分子中存在离子键
B. 不同元素组成的多原子分子中的化学键一定全是极性键
C. 化学键是指使原子或离子相互结合的静电吸引作用力
D. NaHSO4固体中含有的阴离子与阳离子的个数比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种微粒,它们的质子数和电子数相等。对这两种微粒关系的下列叙述不正确的是( )
A.它们可能是两种不同的分子B.它们可能是两种不同的原子
C.它们可能是两种不同的离子D.可能一种是分子,另一种是离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,下列说法正确的是( ) 
A.非金属性:Y>Z>M
B.离子半径:M﹣>Z2﹣>Y﹣
C.ZM2分子中各原子的最外层均满足8电子稳定结构
D.三种元素中,Y的最高价氧化物对应的水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前人们对环境保护、新能源开发很重视.
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体.4CO(g)+2NO2(g)4CO2(g)+N2(g)△H=﹣1200 kJmol﹣1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是(填代号). 
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)N2(g)+CO2(g)△H在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/mol.L﹣1/时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0~20min的平均反应速率v(CO2)=;计算该反应的平衡常数K= .
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是(填字母代号).
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率(填“升高”或“降低”),△H0(填“>”或“<”).
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2].已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=﹣159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol
③H2O(l)=H2O(g)△H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式 .
(4)一种氨燃料电池,使用的电解质溶液是2mol/L﹣1的KOH溶液.
电池反应为:4NH3+3O2=2N2+6H2O;
请写出通入a气体一极的电极反应式为;每消耗3.4g NH3转移电子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化对人类文明贡献巨大,古代文献中充分记载了古代化学研究成果。下列关于KNO3的古代文献,对其说明不合理的是
目的 | 古代文献 | 说明 | |
A | 性质 | “…凡研消(KNO3)不以铁碾入石臼,相激火生,祸不可测”一《天工开物》 | KNO3能自燃 |
B | 鉴别 | 区分硝石(KNO3)和朴消(Na2SO4):“以火烧之,紫青烟起,乃真硝石也” ——《本草经集注》 | 利用焰色反应 |
C | 提纯 | “…(KNO3)所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”——《开宝本草》 | 溶解、蒸发、结晶 |
D | 使用 | “(火药)乃焰消(KNO3)、硫磺、山木炭所合,以为烽燧铜诸药者"——《本草纲目》 | 利用KNO3的氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述:①我国科学家在世界上第一次人工合成结晶牛胰岛素;②最早发现电子的是英国科学家道尔顿;③创造联合制碱法的是我国著名科学家侯德榜;④首先制得氧气的是法国科学家拉瓦锡;⑤有机物的元素定量分析最早是由牛顿提出的,其中正确的是( )
A.只有①
B.①和③
C.①②③
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。
请填写下列空白:
[实验一]用如图所示装置,收集一试管甲烷和氯气的混合气体,光照后观察到,量筒内形成一段水柱,认为有氯化氢生成。
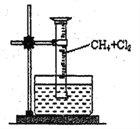
(1)该反应的反应类型为_____________________。
(2)该反应的化学方程式为(只写第一步)______________。
(3)水槽中盛放的液体应为_______。(填标号)
A.水 B.饱和石灰水 C.饱和食盐水 D.饱和NaHCO3溶液
(4)该实验的实验现象为:____________、_____________、试管壁上出现油状液滴
(5)该油状液滴中含有的有机产物共有_______种。
[实验二]收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO3溶液,看到有白色沉锭生成,认为有氯化氢生成。
(6)你认为该实验设计得出的结论是否正确的______,若不正确,理由是:_________________。
[实验三]步骤一:收集半试管氯气,加入10mL蒸馏水,充分振荡,采用DIS系统的pH传感器测溶液的pH(下同),测得pH=3.26
步骤二:收集一试管甲垸和氯气的混合气体(各占50%),在40W的日光灯下光照6min后,加入l0mL蒸馏水,充分振荡,测得pH=1.00。
(7)判断该反应中有氯化氢生成的依据是__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com