
【题目】根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算铜元素相对原子质量。提供的实验仪器及试剂如下(根据需要可重复选用,加入的氯化铵与氢氧化钙的量足以产生使氧化铜完全还原的氨气):
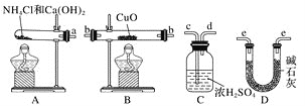
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________。
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________。
(3)在本实验中,若测得m(CuO)=ag,m(H2O)=bg,则Ar(Cu)=_____________________。
(4)在本实验中,使测定结果Ar(Cu)偏大的是________________(填序号)。
①氧化铜未完全起反应 ②氧化铜不干燥 ③氧化铜中混有不反应的杂质 ④ 碱石灰不干燥 ⑤氯化铵与氢氧化钙混合物不干燥
(5)在本实验中,还可通过测定________和________,或________和________达到实验目的。
【答案】2NH3+3CuO![]() 3Cu+3H2O+N2↑ e→b→e
3Cu+3H2O+N2↑ e→b→e ![]() -16 ①③ m(CuO) m(Cu) m(Cu) m(H2O)
-16 ①③ m(CuO) m(Cu) m(Cu) m(H2O)
【解析】
实验原理:2NH3+3CuO![]() 3Cu+3H2O+N2↑
3Cu+3H2O+N2↑
3[Ar(Cu)+16] 54
m(CuO) m(H2O)
则![]() =
=![]() 可解。
可解。
(1) 氨气还原炽热氧化铜,铜元素的化合价降低,氮元素化合价升高,化学方程式为2NH3+3CuO![]() 3Cu+3H2O+N2↑;
3Cu+3H2O+N2↑;
(2)连接装置顺序思路:制取氨气→干燥氨气→氨气与氧化铜反应装置→吸收反应生成的水(以便测铜相对分子质量),故答案为:e→b→e;
(3)由分析可得![]() =
=![]() ,将m(CuO)=ag,m(H2O)=bg代入,化简得Ar(Cu)=
,将m(CuO)=ag,m(H2O)=bg代入,化简得Ar(Cu)=![]() -16;
-16;
(4) (4)由(3)可知得Ar(Cu)=![]() -16,
-16,
①若Cu0未完全起反应,说明b偏小,结果偏大;
②若CuO不干燥,说明a偏小,b偏大,结果偏低;
③若Cu0中混有不反应的杂质,说明b偏小,结果偏大;
④若碱石灰不干燥,说明氨气干燥不彻底,b偏大,结果偏低;
⑤若NH4C1与Ca(OH)2混合物不干燥,但只要氨气干燥彻底,对结果不影响.
所以选项①③正确,故答案为:①③
(5)由分析中的实验原理可知,知道CuO或Cu的质量以及另一组可测数据即可求出Ar(Cu)。可知在本实验中,还可通过测定m(CuO)和m(Cu),或m(Cu)和m(H2O)达到实验目的。


科目:高中化学 来源: 题型:
【题目】以硼镁矿(2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3、A12O3)为原料生产硼酸的工艺流程如下:
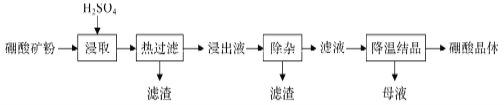
已知:表一:不同温度下H3BO3的溶解度
温度℃) | 20 | 40 | 60 | 100 |
溶解度(g) | 5.0 | 8.7 | 14.8 | 40.2 |
表二:不同物质沉淀完全时的pH
物质 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
pH | 3.2 | 5.2 | 9.7 | 12.4 |
(1)由于矿粉中含CaCO3,“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施为_________________________。
(2)“浸出液”显酸性,含有H3BO3、Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质。“除杂”时,向浸出液中依次加入适量H2O2和MgO,可以除去的杂质离子为_______________________,H2O2的作用为_____________________(用离子方程式表示)。
(3)“浸取”后,采用“热过滤”的目的为__________________________。
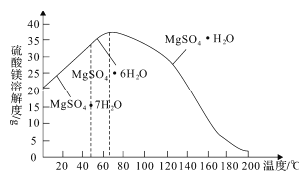
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图所示,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4·H2O,应采取的措施是将“母液”蒸发浓缩,____________________________________。
(5)己知25℃时,硼酸(H3BO3)溶液中存在如下平衡:H3BO3![]() [B(OH)4]-(aq)+H+(aq);K=5.7×10-10;25℃时,0.7mol·L-1硼酸溶液中c(H+)=__________mol·L-1。
[B(OH)4]-(aq)+H+(aq);K=5.7×10-10;25℃时,0.7mol·L-1硼酸溶液中c(H+)=__________mol·L-1。
(6)已知25℃时:
化学式 | H2CO3 | CH3COOH |
电离常数 | K1=4.4×10-7 K2=4.7×10-11 | K=1.75×10-5 |
下列说法正确的是________(填选项字母)。
a.碳酸钠溶液滴入硼酸溶液中能观察到有气泡产生
b.碳酸钠溶液滴入醋酸溶液中能观察到有气泡产生
c.等浓度碳酸溶液和硼酸溶液的pH:前者>后者
d.等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:


图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为__________________________________。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3晶体中B原子个数与极性键个数比为____________。
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用________理论。
(4)三种晶体中熔点最低的是________(填化学式),其晶体受热熔化时,克服的微粒之间的相互作用为____________________________________________________________。
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子一定能够大量共存的是
A. 氢氧化铁胶体中:Na+、K+、S2-、Br-
B. 饱和FeCl3溶液:K+、NH4+、I-、Cl-
C. 含MnO4-的溶液中:Fe3+、Mg2+、SO42-、NO3-
D. 与铝作用生成H2的溶液中:Mg2+、K+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是( )
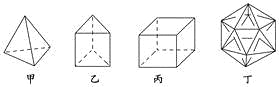
A. 1 mol甲分子内含有10 mol共价键
B. 由乙分子构成的物质不能发生氧化反应
C. 丙分子的二氯取代产物只有三种
D. 分子丁是不可能合成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 加水稀释0.01 mol·L-1的CH3COOH溶液,溶液中c(OH-)减小
B. 室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
C. 氨水加水稀释后,溶液中![]() 的值增大
的值增大
D. 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列两种有机物的描述正确的是
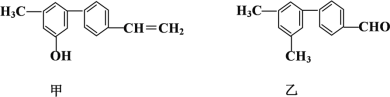
A. 苯环上的一氯代物种数相同
B. 分子中共面的碳原子数一定相同
C. 1 mol甲与浓溴水反应最多能消耗4 mol Br2
D. 甲、乙可用红外光谱区分,但不能用核磁共振氢谱区分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com