
【题目】复旦大学教授吴宇平研制的水溶液锂电池体系,最终能实现电动汽车充电10秒即可行驶400公里的目标,其结构如图所示,则下列说法不正确的是

A.b电极采用多孔电极的目的是易于吸附气体
B.a电极为电池的正极,金属锂发生氧化反应
C.b电极的电极反应为O2+2H2O+4e-=4OH-
D.装置中用导电隔离层将电极锂与水溶液隔开的目的是防止金属锂与水发生反应
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】铝土矿(主要成分为Al2O3,还有少量杂质)是提取氧化铝的原料。提取氧化铝的工艺流程如下:

(1)请用离子方程式表示以上工艺流程中第①步反应:__ _______。
(2)写出以上工艺流程中第③步反应的化学方程式:_ _____。
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应。该反应的化学方程式_____________。请举一例该反应的用途_____________。
(4)电解熔融氧化铝制取金属铝,若有0.9mol电子发生转移.理论上能得到金属铝的质量是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表述正确的是
A.惰性电极电解氯化镁溶液:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
B.钢铁吸氧腐蚀中的正极反应:4OH-- 4e-=2H2O+O2 ↑
C.用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH-
D.等体积、等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨在工业生产中具有重要意义。
(1)在合成氨工业中I2O5常用于定量测定CO的含量。己知2I2(s)+5O2(g)=2I2O5(s) △H=-76kJ·mol-1;2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1。则该测定反应的热化学方程式为____________________________________。
(2)不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数φ (CO2)随时间t变化曲线如图。
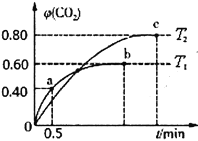
①温度T1时,0~0.5 min内的反应速率v(CO)=________________。
②b点CO的平衡转化率α为____________,c点的平衡常数K为________________。
③下列措施能提高该反应CO转化率的是________(填字母)
a.升高温度 b.增大压强 c.加入催化剂 d.移走CO2
(3)若氨水与SO2恰好生成正盐,则此时溶液呈_________(填“酸性”或“碱性”),向上述溶液中通入___________(填“NH3”或“SO2”)可使溶液呈中性,此时溶液中含硫微粒浓度的大小关系为________________。(已知常温下NH3·H2O的Kb=1.8×10-5mol·L-1,H2SO3的Ka1=1.5×10-2mol·L-1,Ka2=6.3×10-8mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组设计实验制取氨气并探究氨气的有关性质:
(1)实验室制备氨气,下列方法中适宜选用的是 ___________(填编号)
A . 氯化铵溶液与氢氧化钠溶液共热
B. 固体氢氧化钠中滴加浓氨水
C. 固态氯化铵加热分解
D. 固态硝酸铵加热分解
E. 固态氯化铵与熟石灰混合加热
(2)该小组成员设计实验制备氨气并探究氨气的还原性及产物,提供实验装置如图:
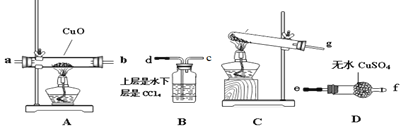
①装置C中发生反应的化学方程式为______________
②根据上述提供的装置正确的连接顺序为____________(用各接口序号表示)
③该装置在设计上有一定的缺陷,你对该装置的改进措施是___________。
(3)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式________
(4)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。请你设计一个简单的实验检验该红色物质中是否含有Cu2O__________。已知:Cu2O+2H+=Cu+Cu2+ +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家用某有机分子和球形笼状分子C60制成了“纳米车”(如图所示,整辆“纳米车”的对角线的长度仅为3至4纳米),每 辆“纳米车”是由一个有机分子和四个C60分子构成。“纳米车”可以用来运输单个的有机分子。下列说法不正确的是

A.人们用肉眼看不到“纳米车”的运动
B.“纳米车”的诞生说明人类操纵分子的技术进入了一个新阶段
C.C60是一种新型的化合物
D.C60的摩尔质量为720gmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24 L H2O中含有的原子数目为0.3NA
B.常温常压下,4.6 g NO2与N2O4混合气体中含有的氧原子数目为0.2 NA
C.0.1 molL-1 K2CO3溶液中含有的钾离子数目为0.2NA
D.0.lmol铁与足量氯气反应时,转移的电子数目为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝生产加工过程中产生大量的铝灰,直接掩埋造成铝资源浪费,还会带来严重的污染。某铝厂的铝灰经分析所含主要物质如下:Al、Al2O3、AlN、SiO2、Fe2O3,其他杂质均不溶于稀硫酸。如图是酸浸法用该铝灰生产高纯氧化铝的生产流程:
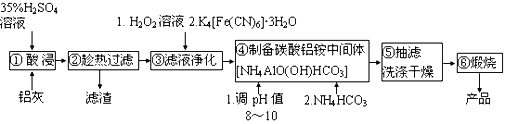
已知:i.Fe3+ +K++ [Fe(CN)6]4-=K[Fe(CN)6Fe]↓
ii.AlN常温下与水缓慢反应,酸性或碱性条件下反应较快
iii.NH4AlO(OH)HCO3难溶于碱性溶液和乙醇
请回答:
(1)实验室模拟工业生产①酸浸步骤的装置如图,该装置的不合理之处为____。
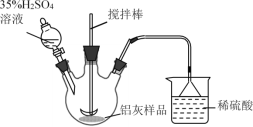
(2)步骤③加入H2O2溶液的目的是________________。
(3)步骤④调节pH最合适的试剂是________________。
A.NaOH B.H2SO4 C.NH3·H2O D.Ca(OH)2
(4)步骤⑤吸滤瓶内液体高度快达到支管口位置时应拔掉瓶上橡皮管,_______,洗涤沉淀操作为_______________。
(5)写出煅烧碳酸铝铵中间体得到高纯氧化铝的化学方程式______________。
(6)已知Al3+对光的吸收与其浓度成线性关系,色度计传感器可以测量某种波长的光穿过溶液的透射率确定溶液浓度。如图是红色光照下透光率(T)对应c(Al3+)的标准曲线。为测定铝灰中铝元素的回收率,准确称取0.5000g铝灰(折合铝元素含量60.00%)进行制备高纯氧化铝的实验,将所制得的粉末与固体NaOH反应后加水溶解、过滤,滤液定容到250mL容量瓶中。用移液管移取25.00mL到锥形瓶中,加2滴指示剂,滴加稀盐酸至溶液体积变为50.00mL,NaAlO2恰好反应生成AlCl3。取该溶液于比色皿中进行色度检测,测得溶液透光率为97.5,则铝元素的回收率=_________。
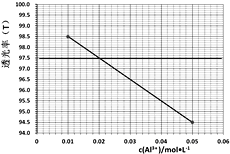
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近几年具有超常性能的铝离子电池成为研究热点,某化学研究所研发出了以新型石墨烯(Cn) 作正极材料的铝离子电池,可在一分钟内完成充电,其放电时的工作原理如图所示。下列说法不正确的是
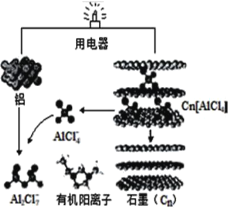
A.充电时,铝电极连接电源负极,该电极有Cn[AlCl4]生成
B.放电时,每生成 1molAl2Cl7-转移电子数目为0.75NA
C.充电时,阴极的电极反应式为4Al2Cl7–+3e–=Al+7AlCl4 –
D.放电时,正极的电极反应式为 Cn[AlCl4]+e–═Cn+AlCl4–
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com