
 材料的不断发展可以促进社会进步.
材料的不断发展可以促进社会进步.
| ||
| ||


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:

| A、易溶于水 |
| B、与澄清石灰水反应产生白色沉淀 |
| C、与足量盐酸反应放出气体 |
| D、属于碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
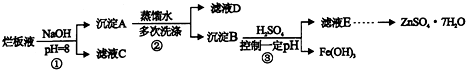
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2和O3互为同素异形体 |
| B、O3是由3个氧原子构成的化合物 |
| C、O2和O3相互转化属于化学变化 |
| D、O3的摩尔质量为48g.mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0mol?L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- | ||
B、
| ||
| C、pH=0的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- | ||
| D、c(ClO-)=1.0 mol?L-1的溶液:Na+、SO32-、S2-、SO42- | ||
| E、与铝反应产生H2的溶液中:NO3-、Na+、Cl-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
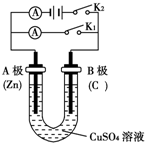 请按要求回答下列问题.
请按要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| A、445.15kJ/mol |
| B、607.3kJ/mol |
| C、890.3kJ/mol |
| D、802.3kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com