

| H2O |
| △ |
| NaOH |
| △ |
| H2O |
| △ |
| NaOH |
| △ |


科目:高中化学 来源: 题型:
| A、金属X能与NaOH溶液反应放出H2,但金属Y不能,则Y的金属性一定比X弱 |
| B、在合成氨反应达到平衡时,只增加N2的物质的量,达新平衡后N2的百分含量增大 |
| C、在铁件上镀铜时,铁和电源负极相连,铜和正极相连,电解质溶液是CuSO4溶液 |
| D、Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2与NaOH溶液:SiO2+2Na++2OH-═Na2SiO3↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
| C、向含有0.4mol FeBr2的溶液中通入0.1mol Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
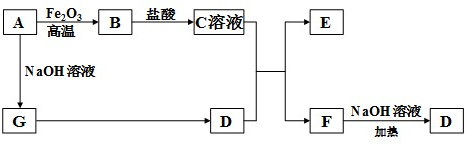
查看答案和解析>>
科目:高中化学 来源: 题型:
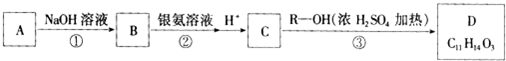 C在一定条件下可发生反应,生成一种高分子化合物E,E的结构简式为
C在一定条件下可发生反应,生成一种高分子化合物E,E的结构简式为 ,其中R、R′为烃基.请回答以下问题:
,其中R、R′为烃基.请回答以下问题: ,且属于酯的所有同分异构体的结构简式
,且属于酯的所有同分异构体的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
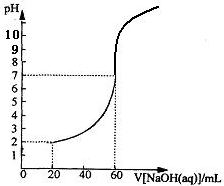 20.00mL一定物质的量浓度的盐酸X,用一定浓度的NaOH溶液Y滴定,滴定过程中溶液pH和所加NaOH溶液的体积的关系如图所示.(体积变化忽略不计)
20.00mL一定物质的量浓度的盐酸X,用一定浓度的NaOH溶液Y滴定,滴定过程中溶液pH和所加NaOH溶液的体积的关系如图所示.(体积变化忽略不计)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中滴加盐酸,无现象,再加氯化钡溶液有白色沉淀,则该溶液中一定含SO42- |
| B、若向氯水中加入少量CaCO3固体,会使溶液的pH减小,HClO浓度增大 |
| C、将某气体通入溴水中,溴水颜色褪去,该气体一定是二氧化硫 |
| D、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com