
1.0 mol KNO3 氧化的碳的质量是15 g。
解析:本题由给出的化学反应方程式主要考查氧化还原反应的概念及有关计算。
首先分析给出的化学反应方程式,化合价降低的反应物在反应中作氧化剂,它们是KNO3和S,即N和S两种元素反应前后化合价由高变低。不少学生考虑不全,误认为氧化剂只有KNO3或只有S。本题是两种元素N和S氧化一种元素C。根据得失电子关系,C的化合价升高4价,即1 mol 碳单质在反应中失去4 mol e-,3 mol碳单质共失去 12 mol e-,而2 mol KNO3 共得到 10 mol e- ,1 mol硫单质只得到2 mol e-。由反应方程式分析可知,被2 mol KNO3 氧化的碳占总物质的量的![]() ,即
,即![]() ,而反应中总共被氧化的碳的物质的量为3 mol,所以被 2 mol KNO3氧化的碳的物质的量=
,而反应中总共被氧化的碳的物质的量为3 mol,所以被 2 mol KNO3氧化的碳的物质的量=![]() mol=2.5 mol,故被 1.0 mol KNO3 氧化的碳的物质的量为
mol=2.5 mol,故被 1.0 mol KNO3 氧化的碳的物质的量为![]() mol 。
mol 。
2KNO3 + S + 3C====K2S+N2↑+3CO2↑
2 ![]()
1 mol n(C) ![]()
n(C)=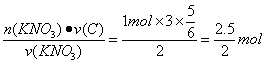 =1.25 mol
=1.25 mol
m(C)=n(C)·M(C)=1.25 mol×12 g·mol-1=15 g


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:022
据新华社报道:从2004年5月11日16日记者发稿时为止,广州市白云区“假酒中毒”事件中的死亡人数已增加到9人,住院人数增加到33人,其中10人病危.目前广州市有关部门查明:“毒酒”窝点有5桶工业酒精,每桶工业酒精的质量为165 kg,其中甲醇的质量分数为10%.饮用甲醇5 g-15 g即可使人中毒甚至死亡.据此消息:
(1)5桶工业酒精共含甲醇________kg这些甲醇若全被酒客饮用,死亡人数将继续上升,后果不堪设想.
(2)已知工业制备甲醇的方程式为:CO+2H2=x(x即为甲醇)由此可推断甲醇的化学式为________
(3)已知甲醇的分子结构和乙醇相似,根据结构决定性质的规律,请推测甲醇的一种化学性质:________
(4)认识到掌握化学知识能帮助人们抵御有害物质的侵害,由此我们联想到误食其它有害物质使人中毒的事件还有(请举一例)________
查看答案和解析>>
科目:高中化学 来源: 题型:
已知电石与水能发生剧烈反应,反应的方程式为:CaC![]() +2H
+2H![]() O→Ca(OH)
O→Ca(OH)![]() +C
+C![]() H
H![]() ↑,产生的C
↑,产生的C![]() H
H![]() (乙炔)是一种易燃的气体,电石遇水起火实质上是电石与水反应产生的C
(乙炔)是一种易燃的气体,电石遇水起火实质上是电石与水反应产生的C![]() H
H![]() 在燃烧。根据以上信息完成下列问题:
在燃烧。根据以上信息完成下列问题:
(1)电石遇水起火,产生浓烈的黑烟,说明C![]() H
H![]() 燃烧_______(填“充分”或“不充分”),黑烟的主要成分是______________________。
燃烧_______(填“充分”或“不充分”),黑烟的主要成分是______________________。
(2)根据题给信息,推测电石与水反应是_____(填“放热”或“吸热”)反应,理由是_________。
(3)这起事故对水源地水质最直接的影响是____________________________。
查看答案和解析>>
科目:高中化学 来源:同步题 题型:计算题
 K2S+N2↑+3CO2↑ 求此反应中被1.0 mol KNO3氧化的碳的质量是多少克?
K2S+N2↑+3CO2↑ 求此反应中被1.0 mol KNO3氧化的碳的质量是多少克? 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com