
| A. | 4 | B. | 5 | C. | 6 | D. | 7 |
分析 ①干冰为固体二氧化碳,升华吸收大量的热,具有制冷作用;
②Si为良好的半导体材料;
③依据制玻璃用到的原料解答;
④依据侯氏制碱法原理解答;
⑤耐火材料应具有较高的熔点;
⑥NaClO具有强的氧化性,能够使蛋白质变性;
⑦Fe2O3-消毒净水
⑦耐火材料应具有较高的熔点;
⑧Fe2O3为红棕色固体.
解答 解:①干冰是固体的二氧化碳,干冰升华(由固态变成气态)时会吸收大量热,使空气中的水蒸气液化成水滴降落,就是人工降雨,故①正确;
②Si为良好的半导体材料,是制造太阳能电池主要原料,故②错误;
③工业上制造玻璃的主要原料是碳酸钠、碳酸钙和二氧化硅,故③正确;
④工业上用氨气、二氧化碳、饱和氯化钠溶液反应制备纯碱,即侯氏制碱法,故④正确;
⑤氧化铝熔点高,可以做耐火材料,故⑤正确;
⑥NaClO具有强的氧化性,能够使蛋白质变性,具有杀菌消毒作用,故⑥正确;
⑦氧化镁熔点高,可以做耐火材料,故⑦正确;
⑧Fe2O3为红色固体常用来做红色油漆或涂料,故⑧正确;
故选:D.
点评 本题考查了物质的用途,明确物质的性质即可解答,侧重对基础知识点的考查,会运用化学知识解释生活常识,题目难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
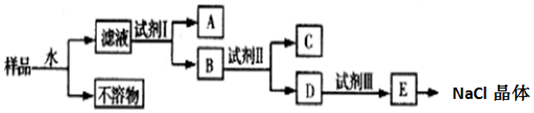
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
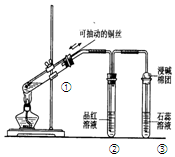
| A. | 上下移动①中铜丝可控制SO2的量 | |
| B. | ②中品红溶液褪色 | |
| C. | ③中石蕊溶液变红色 | |
| D. | 为确认CuSO4生成,向①中加水,观察溶液颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2 L N2含有的分子数为0.5NA | |
| B. | 在标准状况下,11.2 L H2O所含的分子数为0.5NA | |
| C. | 在常温常压下,1 mol O2含有的原子数为2NA | |
| D. | 只有在标准状况下的气体摩尔体积才是22.4L/mol. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子中的6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键 | |
| B. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 | |
| C. | 乙烷和丙烯的物质的量共1 mol,其混合物完全燃烧生成3 mol H2O | |
| D. | 将溴水加入苯中,溴水的颜色变浅,这是由于发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2既是氧化剂,又是还原剂 | |
| B. | NaNO2是氧化剂,氧化产物、还原产物都是N2 | |
| C. | NH4Cl中的氮元素被还原 | |
| D. | 每生成1 mol N2时,转移电子的物质的量为6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该分散系是纯净物 | |
| B. | 可用过滤的方法将黑色金属氧化物与Na+分离开 | |
| C. | 加入NaOH时发生的反应可能为:Fe2++2Fe3++8OH-═Fe3O4+4H2O | |
| D. | 在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液与氢氧化钠溶液反应的离子方程式为H++OH-═H2O | |
| B. | H2O的电离方程式:H2O+H2O?H3O++OH- | |
| C. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O (g)△H=-890.3 kJ•mol-1 | |
| D. | 双氧水中加入稀硫酸和KI溶液:H2O2+2I-+H+═I2+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com