
【题目】下列分离方法与溶质的溶解度无关的是
A.萃取B.重结晶C.纸上层析法D.蒸馏
科目:高中化学 来源: 题型:
【题目】若除酶外所有试剂均已预保温,则在测定酶活力的试验中,下列操作顺序合理的是
A.加入酶→加入底物→加入缓冲液→保温并计时→一段时间后检测产物的量
B.加入底物→加入酶→计时→加入缓冲液→保温→一段时间后检测产物的量
C.加入缓冲液→加入底物→加入酶→保温并计时→一段时间后检测产物的量
D.加入底物→计时→加入酶→加入缓冲液→保温并计时→一段时间后检测产物的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲型H1N1流感患者体内,糖类不含有,脂质不一定有,蛋白质也不一定有,而核酸一定有的元素是( )
A. N B. P C. S D. P、S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纤维素为主要原料制备乙酸乙酯的路线如下:
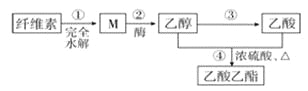
下列说法正确的是( )
A. 若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯
B. M虽然分子结构中无醛基,但仍然可以发生银镜反应
C. 步骤②,1molM完全反应可以生成3mol乙醇
D. ③和④都发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于动物内蛋白质合成与去向的叙述,正确的是( )
A.所有蛋白质的合成都需要能量
B.合成的蛋白质都运到细胞外
C.合成的蛋白质都不能进入细胞核内
D.合成的蛋白质都用于细胞膜蛋白的更新
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年10月初,雾霾天气多次肆虐河北、天津、北京等地区。其中,燃煤和汽车尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g) ![]() 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
①该反应的平衡常数表达式_______________________________________。
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____________________________________(填代号)。
![]()
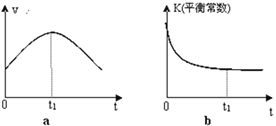
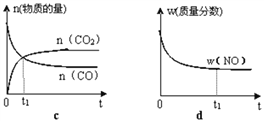
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g)![]() N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:______________________。
(3)在一定条件下,也可以用NH3处理NOx。已知NO与NH3发生反应生成N2和H2O,现有NO和NH3的混合物1mol,充分反应后得到的还原产物比氧化产物多1.4 g,则原反应混合物中NO的物质的量可能是_____________。
(4)以甲烷为原料制取氢气是工业上常用的制氢方法。则2 molCH4与足量H2O(g)反应最多可生成_______mol H2,写出该反应的化学方程式_______________________。
(5)上述方法制得的H2可以和CO在一定条件下合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者以物质的量1:1催化反应,其原子利用率达100%,合成的物质可能是______________________。
a.汽油 b.甲醇 c.甲醛 d.乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有NO、CO2、N2O4三种气体,它们分别都含有0.5 mol氧原子,则三种气体的物质的量之比为
A. 1∶1∶2 B. 1∶1∶1 C. 4∶2∶1 D. 1∶2∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Cu片放入0.1molL﹣1FeCl3溶液中,反应一定时间后取出Cu片,溶液中的C(Fe3+):C(Fe2+)=2:3,则Cu2+与Fe2+的物质的量之比为( )
A.3:4
B.4:3
C.1:2
D.5:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com