
某气态烃A与H2的相对密度为14,其产量可以用来衡量一个国家的石油化工发展水平。以该化合物为原料合成化合物G、E和I的流程如下:
已知:Ⅰ.芳香族化合物F为C、H、O化合物,其相对分子质量为166,环上的一氯代物有一种,1 mol F与足量NaHCO3溶液反应能生成2 mol CO2,F与足量B反应生成G。
Ⅱ.H为二元醇,其蒸气密度折算成标准状况为2.77 g/L,H与足量D反应生成I。

(1)A中官能团的名称为 ,E的结构简式 。
(2)G的分子式为 ,反应⑤的反应类型为 。
(3)写出下列化学方程式:
② ;
⑥ ;
(4)F与H可生成高分子化合物J,写出生成J的化学反应方程式:
。
(5)I有多种同分异构体,其中一类同分异构体有如下特征:
①分子中含有五元环结构;②1 mol该有机物与足量NaHCO3溶液反应,能生成1 mol CO2;③1 mol该有机物与足量Na反应,能生成1.5 mol H2;④环上的一氯代物只有三种。则满足以上条件的有机物的所有可能的结构简式为:
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。
已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应的过程中放出热量。温度较高时,氯气和碱还能发生如下反应:
6Cl2 + 6Ca(OH)2  5CaCl2 + Ca(ClO3)2 + 6H2O
5CaCl2 + Ca(ClO3)2 + 6H2O
该兴趣小组设计了下列实验装置,进行实验。
 |
甲 乙 丙 丁
请回答下列问题:
(1)①甲装置中发生反应的化学方程式是 。
②乙装置中的试剂是 ,作用是 。
③该兴趣小组用300mL 12mol/L盐酸与17.4g MnO2制备氯气,并将所得氯气与过量的石灰乳反应。则理论上最多可制得标况下氯气 L,Ca(ClO)2 g。
 (2)小组成员发现,产物中Ca(ClO)2的质量明显小于
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于
理论值。他们讨论后认为,部分氯气未与石灰乳
反应而逸出,以及温度升高是可能原因。为了探
究反应条件对产物的影响,他们另取一定量的石
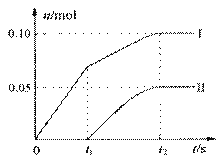
灰乳,缓慢、匀速地通入足量氯气,得出了ClO—、
ClO3— 两种离子的物质的量(n)与反应时间(t)
的关系曲线,粗略表示为右图(不考虑氯气和水
的反应)。
①图中曲线Ⅱ表示 离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为 mol。
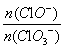 ③另取一份与②等物质的量Ca(OH)2的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl—的物质的量为0.35mol,则产物中 = 。
③另取一份与②等物质的量Ca(OH)2的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl—的物质的量为0.35mol,则产物中 = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D
顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;E的单
质可做半导体材料;C与E两元素形成的化合物可与A、C、D形成的化合物Y发生反应;
B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M。1molM中含
有42mol电子。回答下列问题:
(1) E元素在周期表中的位置 ;化合物M中含有的化学键类型有
(2)比较B、C、E形成的气态氢化物的稳定性由强到弱的顺序是
(用化学式表示);写出C与A形成的18e-化合物的电子式 ,
该化合物类型为 (填“共价化合物”或“离子化合物”)
(3)写出C与E两元素形成的化合物与Y溶液反应的离子方程式
;写出题中生成M的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素在周期表中位置的叙述正确的是
A.原子的最外层有2个电子的元素一定是ⅡA族元素
B.元素所在的主族序数与最外层电子数之比为1的元素都是金属元素
C.俄罗斯专家首次合成了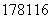 X原子,116号元素位于元素周期表中第七周期ⅥA族
X原子,116号元素位于元素周期表中第七周期ⅥA族
D.原子最外层电子数大于3(小于8)的元素一定是非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬酸的结构简式如图,下列说法正确的是
A.柠檬酸中能发生酯化反应的官能团有2种
B.1 mol柠檬酸可与4 mol NaOH发生中和反应
C.1 mol柠檬酸与足量金属Na反应生成生成1.5 mol H2
D.柠檬酸与O2在Cu作催化剂,加热的条件下,能发生氧化反应
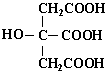 |
查看答案和解析>>
科目:高中化学 来源: 题型:
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海 水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
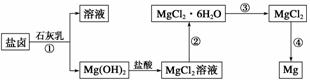
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是________________________________________________________________________。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有________溶液的烧杯中,充分搅拌后经________、______(填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:
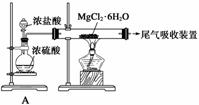
其中装置A的作用是____________________________________________________。
(4)写出过程④中发生反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是
A.铜铸塑像上出现铜绿[Cu2(OH) 2CO3] B.灶具大理石板被食醋腐蚀变得不光滑
C.含亚铁离子的补血药丸采用糖衣包裹 D.用煤气灶燃烧天然气为炒菜提供热量
查看答案和解析>>
科目:高中化学 来源: 题型:
在 K2Cr2O7 + 14HCl = 2KCl + 2CrCl3 + 3Cl2?+ 7H2O反应中。
(1) 是氧化剂,氧化产物是 ;
(2)此反应若转移了0.3mol的电子,则生成氯气 L(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属键的叙述不正确的是
A.金属键没有饱和性和方向性
B.金属键中的电子属于整块金属
C.将铁制品做成炊具,金属键没有被破坏
D.金属导电的过程实质就是金属键被破坏的过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com