
| A. | 0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合:c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) | |
| D. | Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+) |
分析 A.反应溶质为等浓度的NaCl和CH3COOH,醋酸是弱电解质存在电离平衡,溶液呈酸性,甲醇判断离子浓度大小;
B.混合液的pH>7,说明溶液中一水合氨电离大于铵根离子水解溶液呈碱性,则:(NH4+)>c(NH3•H2O),根据物料守恒可得:(NH4+)>c(Cl-)>c(NH3•H2O);
C.混合液中n(Na):n(C)=3:2,根据溶液中的物料守恒判断;
D.根据混合液中的电荷守恒判断.
解答 解:A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合反应生成NaCl和CH3COOH,醋酸是弱电解质存在电离平衡,溶液呈酸性,溶液中离子浓度c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-),故A正确;
B.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),说明溶液中一水合氨电离大于铵根离子水解溶液呈碱性,则:(NH4+)>c(NH3•H2O),根据物料守恒可得:(NH4+)>c(Cl-)>c(NH3•H2O),溶液中浓度大小为:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-),故B错误;
C.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:n(Na):n(C)=3:2,溶液中物料守恒得到:2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],故C正确;
D.0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸)反应生成氯化钠、NaHC2O4,溶液中存在电荷守恒为:c(Cl-)+2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+),故D正确;
故选B.
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理的含义及应用方法,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:多选题

| A. | 双氢青蒿素属于酯类物质 | |
| B. | 青蒿素的分子式为C15H22O5 | |
| C. | 青蒿素环上的一氢取代物有11种 | |
| D. | 青蒿素通过加成反应可以转化为双氢青蒿素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
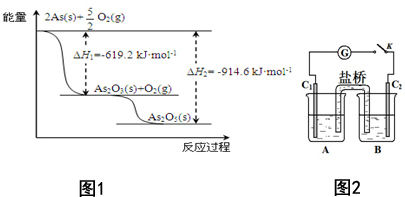 对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 测试时间(H) | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH: | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③② | C. | ③① | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 1 mol/L氯化钠溶液 | B. | 75mL 2 mol/L氯化镁溶液 | ||
| C. | 50mL 3 mol/L氯化钾溶液 | D. | 50mL 1 mol/L氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定不存在的离子是Fe3+、Cu2+、NH4+、SO42-、CO32-、MnO4- | |
| B. | 肯定存在的离子是SO32-、Br-;Na+、K+离子至少有一种存在 | |
| C. | 无法确定原溶液中是否存在Cl- | |
| D. | 若步骤④改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断有影响. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com