

| 197x |
| 106 |
| 197y |
| 84 |
|
|
| 10.6g |
| 19g |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
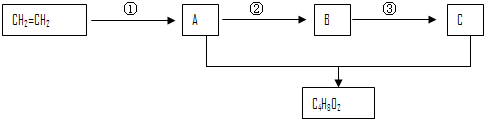
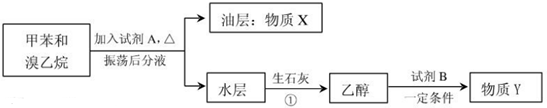
查看答案和解析>>
科目:高中化学 来源: 题型:
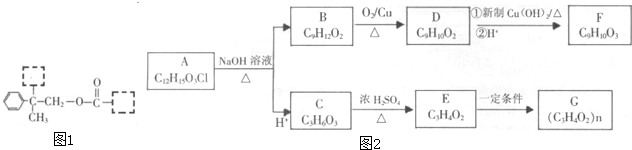
查看答案和解析>>
科目:高中化学 来源: 题型:
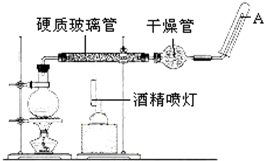 在高温下,Fe与水蒸气可发生反应.应用右边装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在高温下,Fe与水蒸气可发生反应.应用右边装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
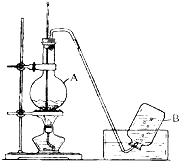 实验室用乙醇制取乙烯的装置如图,回答下列问题.
实验室用乙醇制取乙烯的装置如图,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第三周期非金属元素含氧酸的酸性从左到右依次增强(除Ar外) |
| B、形成离子键的阴阳离子间只存在静电吸引力 |
| C、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| D、元素周期律是元素原子核内核外电子排布周期性变化的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com