
【题目】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出下列元素的名称:A________,B________,C________,D________。
(2)写出C2B2的电子式:________
(3)写出AB2与C2B2反应的化学方程式:________________________________________。
(4)用电子式表示化合物C2D的形成过程:_____________________________________。
(5)A与D的最高价氧化物对应的水化物的浓溶液反应的化学方程式为:________
【答案】碳 氧 钠 硫 ![]() 2CO2+2Na2O2=2Na2CO3+O2
2CO2+2Na2O2=2Na2CO3+O2 ![]() C+2H2SO4(浓)
C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
【解析】
A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大。A和B原子有相同的电子层数,则A、B处于同一周期,A的L层电子数是K层电子数的两倍,则A有2个电子层,L层电子数为4,故A为碳元素;C单质燃烧时呈现黄色火焰,则C为钠元素;C的单质在点燃时与足量的B单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,淡黄色固态化合物为Na2O2,则B为氧元素,D为硫元素,据此解答。
(1)由上面分析可知,A为碳,B为氧,C为钠,D为硫;答案为碳,氧,钠,硫。
(2)B为O元素,C为Na元素,C2B2为Na2O2,含离子键和非极性共价键,属于离子化合物,其电子式为![]() ;答案为
;答案为![]() 。
。
(3)AB2为CO2,CO2与Na2O2反应生成碳酸钠和氧气,该反应的化学方程式为:2CO2+2Na2O2=2Na2CO3+O2;答案为2CO2+2Na2O2=2Na2CO3+O2。
(4)C2D为Na2S,属于离子化合物,用电子式表示形成过程可为![]() ;答案为:
;答案为:![]() 。
。
(5)A为C元素,D为S元素,它的最高价氧化物对应的水化物为H2SO4,C与浓H2SO4反应,生成CO2、SO2和H2O,其化学方程式为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;答案为C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;答案为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。


科目:高中化学 来源: 题型:
【题目】下列对有机物结构或性质的描述,错误的是( )
A. 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
B. 苯酚钠溶液中通入少量CO2,可以生成苯酚和碳酸钠
C. 乙烷和丙烯的物质的量共1 mol,完全燃烧生成3 mol H2O
D. 光照下2,2─二甲基丙烷与Br2反应,其一溴取代物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为0.5L的恒容密闭容器中发生反应:CO(g)+Cl2(g)COCl2(g),其中容器Ⅰ中5min时到达平衡。
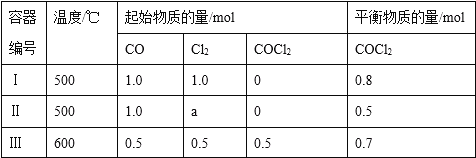
下列说法中正确的是( )
A. 容器Ⅰ中前5min的平均反应速率v(CO)=0.16molL﹣1min﹣1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁钉放入纯水中,一段时间后,铁钉表面有铁锈生成,下列说法正确的是
![]()
A.铁钉与水面交接处最易腐蚀
B.铁钉发生吸氧腐蚀,铁做阴极
C.铁发生的反应是:Fe-3e→Fe3+
D.水上和水下部分的铁钉不发生电化腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.54g氧化铜与石墨的混合粉末隔绝空气加热,充分反应后,生成的气体用足量的NaOH溶液吸收,溶液增重1.32g。则原混合粉末中氧化铜的质量可能是
A.2.4gB.4.8gC.6gD.6.18g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图装置制备HCl气体。

(1)推压注射器活塞将浓盐酸慢慢注入到浓硫酸中,可制备少量干燥HCl气体,其原理是___(选填编号)。
a.浓硫酸吸收了盐酸中水分
b.混合时放热使HCl溶解度减小
c.浓盐酸中HCl以分子形式存在
d.浓盐酸密度小于浓硫酸
(2)为测定制备气体后残留混合酸中盐酸和硫酸的浓度,进行如下实验:取5.00mL混合酸,加水稀释至500mL,完成此操作,用到的精确定量仪器有____;称量4.7880gBa(OH)2固体,溶于水配成250mL标准溶液,装入洗净的细口试剂瓶,并贴上标签。装瓶前用标准溶液对试剂瓶进行润洗的目的是___,请你填写标签上的空白。____
![]()
(3)从500mL稀释液中取出20.00mL,滴加几滴酚酞作指示剂,用标准Ba(OH)2溶液滴定至溶液由无色变为红色才停止滴定,出现这种情况的补救措施除重做外,还有可以采取的措施是__。
(4)为完成全部测定,接下来对锥形瓶中混合物进行的操作是___、称量、___。
(5)若固体Ba(OH)2中混有少量的NaOH,会导致混合酸中硫酸浓度的测定结果___(选填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A.19g羟基(-18OH)所含中子数为10NA
B.标准状况下,44.8 L HF含有2NA个极性键
C.1 mol NaHSO4晶体含有的离子数为3NA
D.0.1 mol·L-1 KAl(SO4)2溶液中SO42-的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据框图分析,下列说法不正确的是
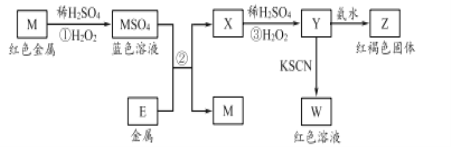
A. 我国是世界上最早使用反应②冶炼金属M的国家
B. M2+的氧化性比E2+的氧化性强
C. 在反应③中若不加稀硫酸,可能观察到红褐色沉淀
D. 在反应①中稀硫酸既表现出氧化性又表现出酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com